仔细阅读下列问题,完成下列问题
(1)一定条件下,在体积为10L的密闭容器中,A、B、C三种气体的物质的量 随时间
随时间 的变化如图1所示。已知达到平衡后,降低温度,A的体积分数将减小。
的变化如图1所示。已知达到平衡后,降低温度,A的体积分数将减小。
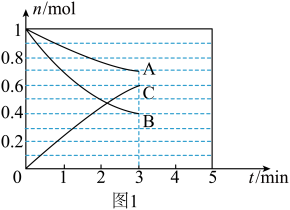
①该反应的化学方程式为___________ ,此反应平衡常数表达式为
___________ 。
②该反应的
___________ 0(填“>”“<”或“=”)。
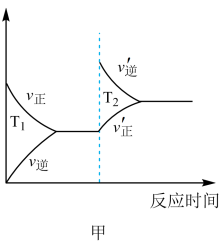
③该反应的反应速率v随时间t的变化关系如图2所示:根据图2判断,在 时刻改变的外界条件是
时刻改变的外界条件是___________ 。在恒温恒容密闭容器中发生该反应,下列能作为达到平衡状态的判断依据是___________ (填标号)。
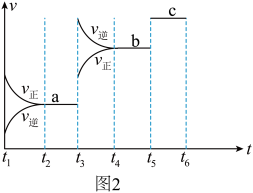
a.体系压强不变 b.A的消耗速率等于B的生成速率气体
c.气体的密度保持不变 d.气体的平均摩尔质量保持不变
(2)消除含氮、硫、氯等化合物对大气和水体的污染对建设美丽家乡,打造宜居环境具有重要意义。 和
和 是常见的环境污染气体,汽车尾气中
是常见的环境污染气体,汽车尾气中 、
、 在一定条件下可以发生反应:
在一定条件下可以发生反应: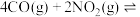
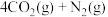
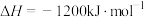 ,在一定温度下,向容积固定为
,在一定温度下,向容积固定为 的密闭容器中充入一定量的
的密闭容器中充入一定量的 和
和 ,
, 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。
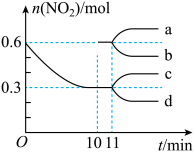
①从反应开始到 的平衡状态,
的平衡状态, 的平均反应速率为
的平均反应速率为___________ 。从 起,其他条件不变,压缩容器的容积为
起,其他条件不变,压缩容器的容积为 ,则
,则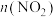 的变化曲线可能为图中的
的变化曲线可能为图中的___________ (填字母)。
②对于该反应,温度不同(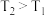 )、其他条件相同时,下列图像表示正确的是
)、其他条件相同时,下列图像表示正确的是___________ (填序号)。

(1)一定条件下,在体积为10L的密闭容器中,A、B、C三种气体的物质的量
 随时间
随时间 的变化如图1所示。已知达到平衡后,降低温度,A的体积分数将减小。
的变化如图1所示。已知达到平衡后,降低温度,A的体积分数将减小。
①该反应的化学方程式为

②该反应的

③该反应的反应速率v随时间t的变化关系如图2所示:根据图2判断,在
 时刻改变的外界条件是
时刻改变的外界条件是
a.体系压强不变 b.A的消耗速率等于B的生成速率气体
c.气体的密度保持不变 d.气体的平均摩尔质量保持不变
(2)消除含氮、硫、氯等化合物对大气和水体的污染对建设美丽家乡,打造宜居环境具有重要意义。
 和
和 是常见的环境污染气体,汽车尾气中
是常见的环境污染气体,汽车尾气中 、
、 在一定条件下可以发生反应:
在一定条件下可以发生反应: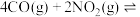
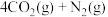
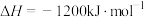 ,在一定温度下,向容积固定为
,在一定温度下,向容积固定为 的密闭容器中充入一定量的
的密闭容器中充入一定量的 和
和 ,
, 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。
①从反应开始到
 的平衡状态,
的平衡状态, 的平均反应速率为
的平均反应速率为 起,其他条件不变,压缩容器的容积为
起,其他条件不变,压缩容器的容积为 ,则
,则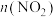 的变化曲线可能为图中的
的变化曲线可能为图中的②对于该反应,温度不同(
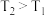 )、其他条件相同时,下列图像表示正确的是
)、其他条件相同时,下列图像表示正确的是

更新时间:2023-07-29 10:30:27
|
相似题推荐
【推荐1】氮的氧化物在生产、生活中有广泛应用。
Ⅰ.已知汽车气缸中氮及其化合物发生如下反应:
 (常温下平衡常数为K1)
(常温下平衡常数为K1)
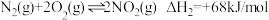 (常温下平衡常数为K2)
(常温下平衡常数为K2)
(1)则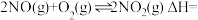
_______  ;常温下平衡常数K=
;常温下平衡常数K=_______ (用K1、K2来表示)
Ⅱ.四氧化二氮(N2O4)可作为运载火箭的推进剂,将4 mol N2O4放入2 L恒容密闭容器中发生反应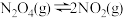 ,平衡体系中N2O4的体积分数(
,平衡体系中N2O4的体积分数( )随温度的变化如图所示:
)随温度的变化如图所示:
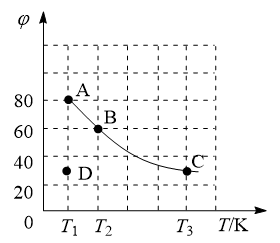
(2)D点v(正)_______ v(逆)(填“>”“=”或“<”)。
(3)A、B、C点中平衡常数K的值最大的是_______ 点。T2时,N2O4的平衡转化率为_______ ;若达平衡时间为5 s,则此时间内的N2O4平均反应速率为_______ 。
(4)若其条件不变,在 原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数
原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数_______ (填“增大”“不变”或“减小”)。
Ⅲ.碳的很多化合物在生产、生活中有广泛应用,对其进行综合利用是目前研究的热点之一。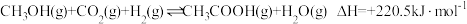 ;中科院化学所研究了该反应的反应历程,如图所示:
;中科院化学所研究了该反应的反应历程,如图所示:
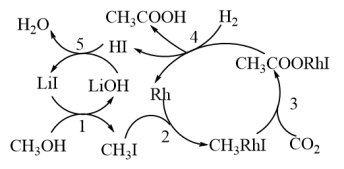
(5)反应历程中,能降低反应活化能的物质有_______ (填化学式);中间产物有_______ 种。
(6)第4步反应的化学方程式为_______ 。
Ⅰ.已知汽车气缸中氮及其化合物发生如下反应:
 (常温下平衡常数为K1)
(常温下平衡常数为K1)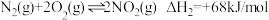 (常温下平衡常数为K2)
(常温下平衡常数为K2)(1)则
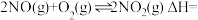
 ;常温下平衡常数K=
;常温下平衡常数K=Ⅱ.四氧化二氮(N2O4)可作为运载火箭的推进剂,将4 mol N2O4放入2 L恒容密闭容器中发生反应
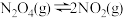 ,平衡体系中N2O4的体积分数(
,平衡体系中N2O4的体积分数( )随温度的变化如图所示:
)随温度的变化如图所示:
(2)D点v(正)
(3)A、B、C点中平衡常数K的值最大的是
(4)若其条件不变,在
 原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数
原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数Ⅲ.碳的很多化合物在生产、生活中有广泛应用,对其进行综合利用是目前研究的热点之一。
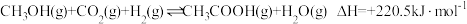 ;中科院化学所研究了该反应的反应历程,如图所示:
;中科院化学所研究了该反应的反应历程,如图所示:
(5)反应历程中,能降低反应活化能的物质有
(6)第4步反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】在某一容积为5L的体积不变的密闭容器内,加入0.3mol的CO和0.3mol的 ,在催化剂存在和800℃的条件下,发生反应:
,在催化剂存在和800℃的条件下,发生反应:
 ,
, 的浓度随时间变化情况如图:
的浓度随时间变化情况如图:

(1)可以说明该反应已达平衡的是_______ (填序号)。
①体系内压强不再改变 ② 的浓度不再改变
的浓度不再改变
③容器内气体的密度不再改变 ④
⑤
(2)根据图上数据,该温度(800℃)下的平衡常数
_______ 。若保持温度和容器的体积不变,在上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后, 的转化率
的转化率_______ (填升高、降低或不变)。
(3)在体积不变的条件下,改变下列条件能增大平衡常数K的有_______ (填字母)。
A.升高温度 B.降低温度 C.增大压强 D.加入一氧化碳气体 E.加入催化剂
(4)在800℃下,改变其他条件,测得在某一时刻
 mol⋅L-1;
mol⋅L-1;
 mol⋅L-1,则此时正、逆反应速率的大小:
mol⋅L-1,则此时正、逆反应速率的大小:
_______ (填“>”“<”或“=”) 。
。
 ,在催化剂存在和800℃的条件下,发生反应:
,在催化剂存在和800℃的条件下,发生反应:
 ,
, 的浓度随时间变化情况如图:
的浓度随时间变化情况如图:
(1)可以说明该反应已达平衡的是
①体系内压强不再改变 ②
 的浓度不再改变
的浓度不再改变③容器内气体的密度不再改变 ④

⑤

(2)根据图上数据,该温度(800℃)下的平衡常数

 的转化率
的转化率(3)在体积不变的条件下,改变下列条件能增大平衡常数K的有
A.升高温度 B.降低温度 C.增大压强 D.加入一氧化碳气体 E.加入催化剂
(4)在800℃下,改变其他条件,测得在某一时刻
 mol⋅L-1;
mol⋅L-1; mol⋅L-1,则此时正、逆反应速率的大小:
mol⋅L-1,则此时正、逆反应速率的大小:
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】在VL容积恒定的密闭容器中,一定量的SO2与1.1molO2发生反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0。反应进行3min时,气体的物质的量减少0.36mol时,反应达到平衡,SO2的平衡转化率是90%。
2SO3(g) ΔH<0。反应进行3min时,气体的物质的量减少0.36mol时,反应达到平衡,SO2的平衡转化率是90%。
(1)反应开始时,向容器中通入的SO2的物质的量是______ 。
(2)开始和平衡时的压强之比为______ 。
(3)用SO2表示该反应的速率是______ 。
(4)该反应的逆反应速率随时间变化情况如图所示。
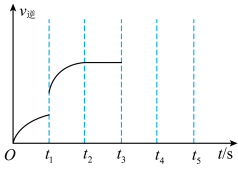
①从图可知,在t1时改变了某种反应条件,反应在t2时达到平衡,改变的条件可能是______ (选填编号)。
a.升高温度 b.增大SO2的浓度 c.减小SO3的浓度 d.使用催化剂 e加压
②如果在t3时增加SO2的量,t4时反应又处于新平衡状态,请在图中画出t3~t5时间段的v逆变化曲线______ 。
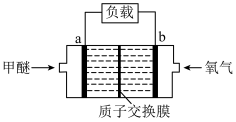
(5)某甲醚(CH3OCH3)燃料电池的工作原理如图所示,质子交换膜两侧的溶液均为1L2mol•L-1H2SO4溶液。当电路中有1.2mol电子发生转移时,左右两侧溶液的质量差为______ g(假设反应物耗尽,忽略气体的溶解)。
 2SO3(g) ΔH<0。反应进行3min时,气体的物质的量减少0.36mol时,反应达到平衡,SO2的平衡转化率是90%。
2SO3(g) ΔH<0。反应进行3min时,气体的物质的量减少0.36mol时,反应达到平衡,SO2的平衡转化率是90%。(1)反应开始时,向容器中通入的SO2的物质的量是
(2)开始和平衡时的压强之比为
(3)用SO2表示该反应的速率是
(4)该反应的逆反应速率随时间变化情况如图所示。

①从图可知,在t1时改变了某种反应条件,反应在t2时达到平衡,改变的条件可能是
a.升高温度 b.增大SO2的浓度 c.减小SO3的浓度 d.使用催化剂 e加压
②如果在t3时增加SO2的量,t4时反应又处于新平衡状态,请在图中画出t3~t5时间段的v逆变化曲线
(5)某甲醚(CH3OCH3)燃料电池的工作原理如图所示,质子交换膜两侧的溶液均为1L2mol•L-1H2SO4溶液。当电路中有1.2mol电子发生转移时,左右两侧溶液的质量差为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】利用天然气为原料的一种工业合成氨简式流程如图:

(1)步骤II中制氢气的原理如下:
I.CH4(g)+H2O(g) CO(g)+3H2(g) K1
CO(g)+3H2(g) K1
II.CO(g)+H2O(g) CO2(g)+H2(g) K2
CO2(g)+H2(g) K2
则反应CH4(g)+2H2O(g) CO2(g)+4H2(g);K=
CO2(g)+4H2(g);K=____ (用含K1、K2的代数式表示)。
(2)合成氨的反应原理为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.2kJ•mol-1。在容积为10L的密闭容器中进行,起始时充入0.2molN2、0.6molH2反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
2NH3(g) ΔH=-92.2kJ•mol-1。在容积为10L的密闭容器中进行,起始时充入0.2molN2、0.6molH2反应在不同条件下进行,反应体系总压强随时间的变化如图所示。

①实验a从开始至平衡时的反应速率v(H2)____ ;实验c中N2的平衡转化率αc为____ 。
②与实验a相比,其他两组改变的实验条件是:b____ ,c___ 。
③M点的逆反应速率v逆____ N点的正反应速率v正(填“>”、“<”或“=”);N点时再加入一定量NH3,平衡后H2的体积分数____ (填“增大”、“减小”或“不变”)。

(1)步骤II中制氢气的原理如下:
I.CH4(g)+H2O(g)
 CO(g)+3H2(g) K1
CO(g)+3H2(g) K1II.CO(g)+H2O(g)
 CO2(g)+H2(g) K2
CO2(g)+H2(g) K2则反应CH4(g)+2H2O(g)
 CO2(g)+4H2(g);K=
CO2(g)+4H2(g);K=(2)合成氨的反应原理为:N2(g)+3H2(g)
 2NH3(g) ΔH=-92.2kJ•mol-1。在容积为10L的密闭容器中进行,起始时充入0.2molN2、0.6molH2反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
2NH3(g) ΔH=-92.2kJ•mol-1。在容积为10L的密闭容器中进行,起始时充入0.2molN2、0.6molH2反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
①实验a从开始至平衡时的反应速率v(H2)
②与实验a相比,其他两组改变的实验条件是:b
③M点的逆反应速率v逆
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
(1)处理NOx的一种方法是利用甲烷催化还原NOx.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为________________________ .
(2)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g) N2(g)+2CO2(g);△H<0.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K=
N2(g)+2CO2(g);△H<0.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K=_______ .

若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将______ 移动(填“向左”、“向右”或“不”).
20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是_________ (填序号).
①加入催化剂 ②降低温度
③缩小容器体积 ④增加CO2的量
(3)肼(N2H4)用亚硝酸氧化可生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977.写出肼与亚硝酸反应的化学方程式_______________ .
(4)如图所示装置可用于制备N2O5,则生成N2O5的那一极电极反应式为_________________ .

(1)处理NOx的一种方法是利用甲烷催化还原NOx.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为
(2)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)
 N2(g)+2CO2(g);△H<0.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K=
N2(g)+2CO2(g);△H<0.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K=
若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将
20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是
①加入催化剂 ②降低温度
③缩小容器体积 ④增加CO2的量
(3)肼(N2H4)用亚硝酸氧化可生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977.写出肼与亚硝酸反应的化学方程式
(4)如图所示装置可用于制备N2O5,则生成N2O5的那一极电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢的方法之一,在1L固定容积密闭容器中投入1.8molCH4和3.6molH2O(g),若只发生反应:CH4(g)+2H2O(g) CO2(g)+4H2(g) △H1=+165.0kJ•mol-1,测得CH4、H2O及某一生成物X的物质的量浓度随反应时间的变化如图1所示(反应中条件有变化时,只考虑改变一个条件)。
CO2(g)+4H2(g) △H1=+165.0kJ•mol-1,测得CH4、H2O及某一生成物X的物质的量浓度随反应时间的变化如图1所示(反应中条件有变化时,只考虑改变一个条件)。

(1)金属氢化物是一类储氢材料,如MgH2,该物质能与水反应:MgH2+2H2O=Mg(OH)2+2H2↑。上述反应涉及的物质中含有离子键的是_______ 。
(2)①CH4(g)+2H2O(g) CO2(g)+4H2(g),说明该反应自发进行的原因
CO2(g)+4H2(g),说明该反应自发进行的原因_______ 。
②反应在10min时的平衡常数K=_______ (列出数学计算式,不必算出结果)。
(3)第6min时改变的条件是_______ 。
(4)画出X物质4min~9min之间的变化图像_______ 。
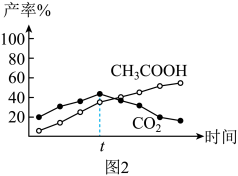
(5)反应的过程中发生副反应CO2(g)+CH4(g)=CH3COOH(g) △H2=-32.2kJ•mol-1,反应所用的时间和CO2、CH3COOH的产率如图2所示,t时刻后,CO2的产率下降,其原因是_______ 。
(6)将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s) 2NH3(g)+CO2(g)。下列各项:
2NH3(g)+CO2(g)。下列各项:
①2v(NH3)正=c(CO2)逆;
②密闭容器中总压强不变;
③密闭容器中混合气体的密度不变;
④密闭容器中氨气的体积分数不变;
⑤密闭容器中c(NH3)不变。
能判断该反应已经达到化学平衡状态的是_______ 。
 CO2(g)+4H2(g) △H1=+165.0kJ•mol-1,测得CH4、H2O及某一生成物X的物质的量浓度随反应时间的变化如图1所示(反应中条件有变化时,只考虑改变一个条件)。
CO2(g)+4H2(g) △H1=+165.0kJ•mol-1,测得CH4、H2O及某一生成物X的物质的量浓度随反应时间的变化如图1所示(反应中条件有变化时,只考虑改变一个条件)。
(1)金属氢化物是一类储氢材料,如MgH2,该物质能与水反应:MgH2+2H2O=Mg(OH)2+2H2↑。上述反应涉及的物质中含有离子键的是
(2)①CH4(g)+2H2O(g)
 CO2(g)+4H2(g),说明该反应自发进行的原因
CO2(g)+4H2(g),说明该反应自发进行的原因②反应在10min时的平衡常数K=
(3)第6min时改变的条件是
(4)画出X物质4min~9min之间的变化图像
(5)反应的过程中发生副反应CO2(g)+CH4(g)=CH3COOH(g) △H2=-32.2kJ•mol-1,反应所用的时间和CO2、CH3COOH的产率如图2所示,t时刻后,CO2的产率下降,其原因是

(6)将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s)
 2NH3(g)+CO2(g)。下列各项:
2NH3(g)+CO2(g)。下列各项:①2v(NH3)正=c(CO2)逆;
②密闭容器中总压强不变;
③密闭容器中混合气体的密度不变;
④密闭容器中氨气的体积分数不变;
⑤密闭容器中c(NH3)不变。
能判断该反应已经达到化学平衡状态的是
您最近一年使用:0次



