铋酸钠(NaBiO3)在酸性条件下可将Mn2+氧化成MnO ,在钢铁工业中可用于锰元素的分析测定。NaBiO3的制备过程为:①将试剂级Bi(NO3)3溶解于稀HNO3溶液中,滤去不溶物;②依次加入水和30%的NaOH溶液至溶液呈中性;③再依次加入30%的NaOH溶液和NaClO溶液,加热至95℃并维持1h;④反应结束后,静置冷却,分去上层清液,用水洗涤沉淀至洗涤液中不含Cl-,在80℃下干燥,即得成品。下列说法正确的是
,在钢铁工业中可用于锰元素的分析测定。NaBiO3的制备过程为:①将试剂级Bi(NO3)3溶解于稀HNO3溶液中,滤去不溶物;②依次加入水和30%的NaOH溶液至溶液呈中性;③再依次加入30%的NaOH溶液和NaClO溶液,加热至95℃并维持1h;④反应结束后,静置冷却,分去上层清液,用水洗涤沉淀至洗涤液中不含Cl-,在80℃下干燥,即得成品。下列说法正确的是
 ,在钢铁工业中可用于锰元素的分析测定。NaBiO3的制备过程为:①将试剂级Bi(NO3)3溶解于稀HNO3溶液中,滤去不溶物;②依次加入水和30%的NaOH溶液至溶液呈中性;③再依次加入30%的NaOH溶液和NaClO溶液,加热至95℃并维持1h;④反应结束后,静置冷却,分去上层清液,用水洗涤沉淀至洗涤液中不含Cl-,在80℃下干燥,即得成品。下列说法正确的是
,在钢铁工业中可用于锰元素的分析测定。NaBiO3的制备过程为:①将试剂级Bi(NO3)3溶解于稀HNO3溶液中,滤去不溶物;②依次加入水和30%的NaOH溶液至溶液呈中性;③再依次加入30%的NaOH溶液和NaClO溶液,加热至95℃并维持1h;④反应结束后,静置冷却,分去上层清液,用水洗涤沉淀至洗涤液中不含Cl-,在80℃下干燥,即得成品。下列说法正确的是| A.常温下,NaBiO3和Bi(NO3)3均可溶于水 |
B.制备NaBiO3的化学方程式为Bi(NO3)3+4NaOH+NaClO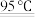 NaBiO3↓+NaCl+3NaNO3+2H2O NaBiO3↓+NaCl+3NaNO3+2H2O |
| C.将Bi(NO3)3溶解于稀HNO3溶液中的目的是增强酸性 |
| D.用NaBiO3分析测定锰元素的过程中,NaBiO3发生氧化反应 |
更新时间:2023-08-15 11:07:50
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
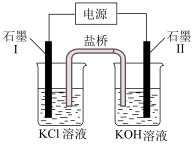
【推荐1】某同学通过“化学—电解法”探究 (高铁酸钾)的合成,其原理如图所示,接通电源,调节电压,将一定量
(高铁酸钾)的合成,其原理如图所示,接通电源,调节电压,将一定量 通入KOH溶液,然后滴入含
通入KOH溶液,然后滴入含 的溶液,控制温度,可制得
的溶液,控制温度,可制得 ,下列说法不正确的是
,下列说法不正确的是
 (高铁酸钾)的合成,其原理如图所示,接通电源,调节电压,将一定量
(高铁酸钾)的合成,其原理如图所示,接通电源,调节电压,将一定量 通入KOH溶液,然后滴入含
通入KOH溶液,然后滴入含 的溶液,控制温度,可制得
的溶液,控制温度,可制得 ,下列说法不正确的是
,下列说法不正确的是
| A.石墨Ⅰ连接电源负极,发生还原反应 |
B.“化学法”得到 的离子方程式为: 的离子方程式为: |
C.合成 ,阴极可以生成3mol KOH ,阴极可以生成3mol KOH |
| D.盐桥中的阴离子向KOH溶液中迁移 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】工业上可用次氯酸盐将氨氮废水转化为 实现绿色处理。实验室模拟如下:取等量氨水分别和不同量的
实现绿色处理。实验室模拟如下:取等量氨水分别和不同量的 混合(混合溶液体积为
混合(混合溶液体积为 ),测得溶液中氨氮(氨、
),测得溶液中氨氮(氨、 )和总氮(氨氮和
)和总氮(氨氮和 的总和)的去除率及
的总和)的去除率及 的浓度与
的浓度与 的加入量关系如图所示。
的加入量关系如图所示。
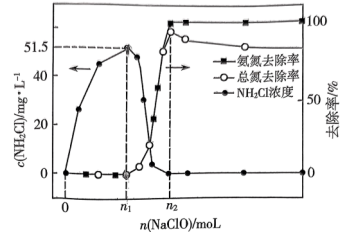
在此过程中发生的反应为:
①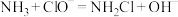
②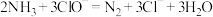
③
已知: 中氮元素为
中氮元素为 价。下列说法正确的是
价。下列说法正确的是
 实现绿色处理。实验室模拟如下:取等量氨水分别和不同量的
实现绿色处理。实验室模拟如下:取等量氨水分别和不同量的 混合(混合溶液体积为
混合(混合溶液体积为 ),测得溶液中氨氮(氨、
),测得溶液中氨氮(氨、 )和总氮(氨氮和
)和总氮(氨氮和 的总和)的去除率及
的总和)的去除率及 的浓度与
的浓度与 的加入量关系如图所示。
的加入量关系如图所示。
在此过程中发生的反应为:
①
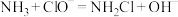
②
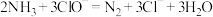
③

已知:
 中氮元素为
中氮元素为 价。下列说法正确的是
价。下列说法正确的是A.当 时,反应①中转移电子的物质的量为 时,反应①中转移电子的物质的量为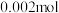 |
B.当 时, 时, |
C. |
D.当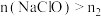 时, 时,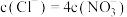 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】1.52g铜镁合金完全溶解于50mL密度为1.40g•mL﹣1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体 1 120mL(标准状况),向反应后的溶液中加入1.0mol•L﹣1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是
| A.得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol•L﹣1 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.该合金中铜与镁的物质的量之比是1:2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】将41.2g由Al、Fe、Cu组成的合金等分为两份,将其中一份合金溶于足量的NaOH溶液中,产生气体6.72L(标准状况);另一份合金溶于过量的稀硝酸中,得到VL(标准状况下)NO气体,向反应后的溶液中加入过量的NaOH溶液,过滤得到滤液X和25.4g的沉淀Y(HNO3的还原产物仅为NO),则下列说法正确的是
| A.41.2g的合金中含铁5.6g | B.滤液X中的溶质只有硝酸钠 |
| C.V为8.96 | D.沉淀Y中含氢氧化铜9.8g |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/c(HCO )的比值保持增大
)的比值保持增大
②浓度均为0.lmol·L-1的 Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO )+c(HCO
)+c(HCO )]
)]
③在0.l mol·L-1氨水中滴加0.l mol·L-1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(H+)=10-a mol·L-1
④向0.lmol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO )均增大
)均增大
⑤浓度相等的a、NH4HSO4溶液、b、NH4HCO3溶液、c、NH4Cl溶液中的c(NH ):a>b>c
):a>b>c
⑥NaHSO3溶液显酸性,c(Na+)>c(HSO )>c(H+)>c(OH-)>c(SO
)>c(H+)>c(OH-)>c(SO )
)
⑦常温下,CH3COONa 和 CH3COOH 混合溶液[pH=7,c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
⑧pH=3.6的0.lmol/LHX与0.lmol/LNaX的混合溶液中,c(H+)-c(OH-)=c(X-)-c(HX)
①NaHCO3溶液加水稀释,c(Na+)/c(HCO
 )的比值保持增大
)的比值保持增大②浓度均为0.lmol·L-1的 Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO
 )+c(HCO
)+c(HCO )]
)]③在0.l mol·L-1氨水中滴加0.l mol·L-1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(H+)=10-a mol·L-1
④向0.lmol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO
 )均增大
)均增大⑤浓度相等的a、NH4HSO4溶液、b、NH4HCO3溶液、c、NH4Cl溶液中的c(NH
 ):a>b>c
):a>b>c⑥NaHSO3溶液显酸性,c(Na+)>c(HSO
 )>c(H+)>c(OH-)>c(SO
)>c(H+)>c(OH-)>c(SO )
)⑦常温下,CH3COONa 和 CH3COOH 混合溶液[pH=7,c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
⑧pH=3.6的0.lmol/LHX与0.lmol/LNaX的混合溶液中,c(H+)-c(OH-)=c(X-)-c(HX)
| A.②③④⑤ | B.②⑤⑦⑧ | C.①③⑤⑥ | D.②⑤⑥⑧ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,向1L0.1mol·L-1NH4Cl溶液中,不断加入固体NaOH后, 与NH3·H2O的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是( )
与NH3·H2O的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是( )

 与NH3·H2O的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是( )
与NH3·H2O的变化趋势如图所示(不考虑溶液体积的变化和氨的挥发),下列说法正确的是( )
| A.M点溶液中水的电离程度比原溶液大 |
| B.a=0.05 |
| C.当n(NaOH)=0.05mol时溶液中有:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) |
| D.在M点时,n(OH-)-n(H+)=(a-0.05)mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】 溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓
溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓 ,黄色加深(b)。
,黄色加深(b)。
已知: (黄色);浓度较小时
(黄色);浓度较小时 (用
(用 表示)几乎无色
表示)几乎无色
取溶液进行如下实验,对现象的分析不正确 的是
 溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓
溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓 ,黄色加深(b)。
,黄色加深(b)。已知:
 (黄色);浓度较小时
(黄色);浓度较小时 (用
(用 表示)几乎无色
表示)几乎无色取溶液进行如下实验,对现象的分析
A.测溶液a的 ,证明 ,证明 发生了水解 发生了水解 |
B.将溶液a滴入沸水中并加热,有丁达尔效应,说明加热能促进 水解 水解 |
C.加入浓 , , 与 与 对溶液颜色变化、 对溶液颜色变化、 浓度大小的影响是一致的 浓度大小的影响是一致的 |
D.向b中加入 后,黄色褪至几乎无色,说明 后,黄色褪至几乎无色,说明 能抑制 能抑制 水解 水解 |
您最近一年使用:0次

 )氧化,其原理为
)氧化,其原理为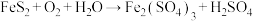 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是


