一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知: pX=-lgc(X)。下列说法正确的是
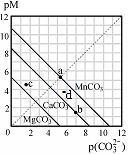

| A.在该温度下,MgCO3、MnCO3的溶解度依次增大 |
| B.d点可表示MnCO3的过饱和溶液,且c(Mn2+)>c(CO32-) |
| C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO32-) |
13-14高三·上海·阶段练习 查看更多[2]
更新时间:2016-12-09 05:41:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,Ksp[Pd(OH)2]=1.0×10-30。向物质的量浓度相同的NaOH和Na2S的混合溶液中滴加Pd(NO3)2溶液产生Pd(OH)2、PdS两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。图中的p(Pd)=-lgc(Pd2+),p(B)=-lgc(OH-)或-lgc(S2-)。下列说法错误的是( )
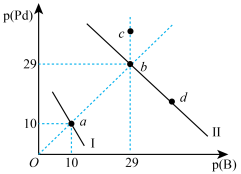

| A.曲线Ⅰ表示的是Pd2+与OH-浓度关系的曲线 |
| B.该温度下,Ksp(PdS)=1.0×10 -58 |
| C.升高温度时,b点可能会向c点移动 |
| D.该温度下,向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐2】根据下列图示所得出的结论不正确的是
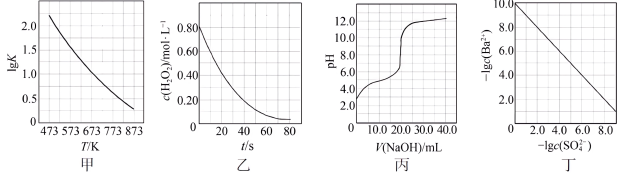

| A.图甲是CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0 |
| B.图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小 |
| C.图丙是室温下用0.1000 mol·L−1NaOH溶液滴定20.00 mL 0.1000 mol·L−1某一元酸HX的滴定曲线,说明HX是一元强酸 |
| D.图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO42−)的关系曲线,说明溶液中c(SO42− )越大c(Ba2+ )越小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列方案设计、现象和结论都正确的是
目的 | 方案设计 | 现象和结论 | |
A | 探究食品脱氧剂中还原铁粉是否变质 | 取少量样品溶于盐酸,滴加 溶液 溶液 | 溶液未变红,说明铁粉未变质 |
B | 证明乙烯的氧化反应 | 将乙烯通入盛有溴水的试管中 | 溴水褪色,说明乙烯被溴水氧化 |
C | 检验某气体是否为 | 将该气体通入到品红溶液中 | 品红溶液褪色,说明该气体是 |
D | 比较 、 、 的 的 大小 大小 | 向 溶液中滴加2滴同浓度 溶液中滴加2滴同浓度 溶液,振荡后再加入4滴同浓度 溶液,振荡后再加入4滴同浓度 溶液 溶液 | 先产生白色沉淀,后产生黄色沉淀,说明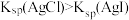 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知:常温下,①Ksp(NiCO3)=1.6×10-7、Ksp(PbCO3)=1.6×10-13;②NiCl2可溶于水PbCl2最大浓度为25mol/L,则向浓度均为0.1mol/L的Ni(NO3)2和Pb(NO3)2混合溶液中逐滴加入Na2CO3溶液,下列说法不正确的是
| A.常温下PbCO3的溶解度约为1.1×10-4g |
| B.逐滴加入Na2CO3溶液,先生成PbCO3沉淀,后生成NiCO3沉淀 |
| C.常温下NiCO3沉淀可转化为PbCO3沉淀,PbCO3沉淀也可转化为NiCO3沉淀 |
| D.逐滴加入Na2CO3溶液,当两种沉淀共存时,溶液中c(Ni2+):c(Pb2+)=106:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象和结论均正确的是
| 实验操作和现象 | 结论 | |
| A | 向等体积等浓度的盐酸中分别加入ZnS和CuS,ZnS溶解而CuS不溶解 |  |
| B | 向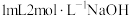 溶液中加入2滴 溶液中加入2滴 溶液,再滴加2滴 溶液,再滴加2滴 溶液,观察到先生成白色沉淀,后生成红褐色沉淀 溶液,观察到先生成白色沉淀,后生成红褐色沉淀 | 证明在相同温度下,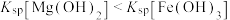 |
| C | 加热盛有少量 固体的试管,试管口处润湿的红色石蕊试纸变蓝 固体的试管,试管口处润湿的红色石蕊试纸变蓝 |  显碱性 显碱性 |
| D | 常温下,测得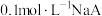 溶液的pH小于 溶液的pH小于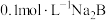 溶液的pH 溶液的pH | 酸性: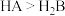 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下,AgCl(s)⇌Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)的关系如图所示。下列说法正确的是


| A.a、b、c三点对应的Ksp不相等 |
| B.AgCl在c点的溶解度比b点的大 |
| C.AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl-) |
| D.b点的溶液中加入AgNO3固体,c(Ag+)沿曲线向c点方向变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】牙形石(一种微型古生物遗体)主要成分为Ca3(PO4)2,存在于灰岩(主要成分为CaCO3)中。可以通过合适的酸除去灰岩显示出牙形石的形态,进而分析当时的地层环境。根据以下数据,有关合适的酸分析错误的是
已知:(1)酸的电离平衡常数
(2)Ksp[Ca3(PO4)2]=2.07×10-33
(3)钙的磷酸盐中只有磷酸二氢钙可溶于水,其余难溶于水
已知:(1)酸的电离平衡常数
| 弱酸 | H3PO4 | CH3COOH | H2CO3 |
| 电离平衡常数(25℃) | Ka1=6.9×10-3 Ka2=6.2×10-8 Ka3=4.8×10-13 | Ka=1.8×10-5 | Ka1=4.5×10-7 Ka2=4.7×10-11 |
(3)钙的磷酸盐中只有磷酸二氢钙可溶于水,其余难溶于水
A.当加入过量的盐酸时与牙形石反应为:Ca3(PO4)2+2H+=H2PO +3Ca2+ +3Ca2+ |
| B.过量的醋酸可以溶解灰岩:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
C.过量醋酸与牙形石:Ca3(PO4)2+4CH3COOH=3Ca2++4CH3COO-+2H2PO ,该反应K≈2.5×10-13 ,该反应K≈2.5×10-13 |
| D.醋酸能溶解灰岩,不溶解牙形石,可用于除去灰岩显示出牙形石 |
您最近一年使用:0次
【推荐1】常温下,难溶物Y2X与ZX在水中的沉淀溶解平衡曲线如图所示,若定义其坐标图示:p(A)=-lgc(A),Mn+表示Y+或Z2+。下列说法错误的是


| A.M表示Y2X的溶解平衡曲线 |
| B.常温下,Y2X的分散系在c点时为悬浊液 |
| C.向b点溶液中加入Na2X饱和溶液,析出ZX固体 |
| D.ZX(s)+2Y+(aq)⇌Y2X(s)+Z2+(aq)的平衡常数K=1014 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度时,氯化银和碘化银的溶解平衡曲线如图所示。图中pAg+= -lgc(Ag+),PX- = -lgc(X-)。 已知Ksp (AgCl) >Ksp( AgI)。下列说法正确的是


| A.该温度下,Ksp(AgI)为1×10-9.75 |
| B.d点溶液可能是AgCl的过饱和溶液 |
| C.加适量KI固体可使溶液由a点变到b点 |
| D.c点溶液的氯离子浓度是b点溶液碘离子浓度的106.25倍 |
您最近一年使用:0次





 AgI(s)+Cl-(aq)
AgI(s)+Cl-(aq)
 ZS(s) +Y2+ (aq) K=1 ×108
ZS(s) +Y2+ (aq) K=1 ×108

