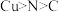Cu2+可以与乙二胺(H2N—CH2CH2—NH2)形成配离子(如图),下列说法正确的是

| A.乙二胺中含有σ、π键 |
| B.该配离子中,中心原子的配位数为2 |
C.基态铜原子的价电子排布图为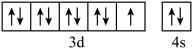 |
| D.沸点:乙二胺>Cl—CH2CH2—Cl |
更新时间:2023/08/26 08:45:19
|
相似题推荐
【推荐1】下列说法或有关化学用语的表达正确的是


| A.[Co(NH3)3Cl3]中Co3+的配位数为6,该配合物中的配位原子只有N原子 | ||||||||||||||
B.基态Fe原子的核外电子轨道表示式为: | ||||||||||||||
| C.氮化锂是一种新型无机贮氢材料,其晶胞结构如图所示,该晶体的化学式为Li3N | ||||||||||||||
D.某主族元素的电离能I1~I7数据如表所示(单位:kJ/mol),可推测该元素位于元素周期表第IIA族
|
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列化学用语不正确的是
A.果糖、脱氧核糖的分子式: |
B.甲醛中π键的电子云轮廓图: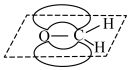 |
C. 的VSEPR模型: 的VSEPR模型: |
D.氨气分子中氮原子的杂化轨道表示式: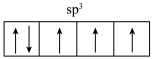 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】配合物在许多方面有着广泛的应用.下列叙述不正确的是
 、
、
 、
、
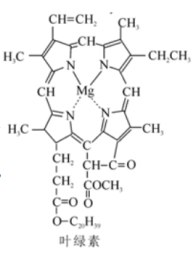
| A.以Mg2+为中心的大环配合物叶绿素能催化光合作用 |
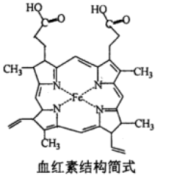
| B.Fe2+的卟啉配合物是输送O2的血红素 |
| C.[Ag(NH3)2]+是化学镀银的有效成分 |
| D.向溶液中逐滴加入氨水,可除去硝酸银溶液中的Cu2+ |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
解题方法
【推荐2】某电池材料的结构如图,M、W、X、Y、Z是原子序数依次增大的同周期主族元素,Y元素原子的价电子数是W的两倍。下列说法正确的是
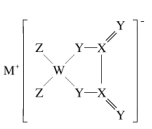
| A.氢化物沸点:X>Y | B.第一电离能:M<W<Y<X<Z |
| C.该物质中的X原子采用sp2杂化 | D.该材料的阴离子中不存在配位键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列事实的解释不正确 的是
| 事实 | 微观解释 | |
| A | 碳原子2p能级有2个未成对电子,甲烷分子式为CH4而非CH2,且为正四面体结构 | 甲烷分子中碳原子的2s和2p轨道进行了sp3杂化,形成了4个能量相等的杂化轨道 |
| B | H3O+中H-O-H键角比H2O中的大 | H3O+和H2O中心原子的孤电子对数分别是1和2,孤电子对之间的斥力<孤电子对与成键电子对之间的斥力<成键电子对之间的斥力 |
| C | 冬季河流中,冰浮于水面 | 水结成冰时,每个水分子通过氢键与周围4个紧邻的水分子相互作用,使冰晶体中水分子之间留有相当大的空隙,从而体积变大,密度变小 |
| D | 单质I2易溶于CCl4中,在水中的溶解度较小 | I2和CCl4属于非极性分子,H2O属于极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】VA族氮、磷、砷(As)、锑(Sb)元素及其化合物应用广泛。氨是重要的化工原料,广泛用于生产铵盐、硝酸、纯碱、医药等;白磷( )晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸(
)晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸( )为一元弱酸,
)为一元弱酸, 为三元中强酸。下列说法正确的是
为三元中强酸。下列说法正确的是
 )晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸(
)晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸( )为一元弱酸,
)为一元弱酸, 为三元中强酸。下列说法正确的是
为三元中强酸。下列说法正确的是
A. 是由极性键形成的非极性分子 是由极性键形成的非极性分子 |
B. 易液化是由于 易液化是由于 与 与 分子间形成氢键 分子间形成氢键 |
C.次磷酸与足量NaOH溶液反应: |
D.白磷晶体中1个 分子周围有12个紧邻的 分子周围有12个紧邻的 分子 分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上利用炭和水蒸气反应:C(s)+H2O(g) CO(g)+H2(g) △H1;CO(g)+H2O(g)=CO2(g)+H2(g) △H2。生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO
CO(g)+H2(g) △H1;CO(g)+H2O(g)=CO2(g)+H2(g) △H2。生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO 能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关NaHCO3的说法正确的是
能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关NaHCO3的说法正确的是
 CO(g)+H2(g) △H1;CO(g)+H2O(g)=CO2(g)+H2(g) △H2。生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO
CO(g)+H2(g) △H1;CO(g)+H2O(g)=CO2(g)+H2(g) △H2。生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO 能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关NaHCO3的说法正确的是
能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关NaHCO3的说法正确的是| A.NaHCO3属于共价化合物 |
B.HCO 能形成多聚体是因为氢键的作用 能形成多聚体是因为氢键的作用 |
| C.C原子的杂化类型为sp3杂化 |
| D.析出NaHCO3的反应属于氧化还原反应 |
您最近一年使用:0次




 )催化剂高效电催化还原
)催化剂高效电催化还原 制备
制备 。催化剂(T)结构如图所示。下列叙述正确的是
。催化剂(T)结构如图所示。下列叙述正确的是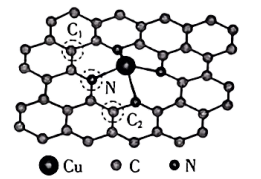
 、
、 的碳原子形成的共价键类型完全相同
的碳原子形成的共价键类型完全相同