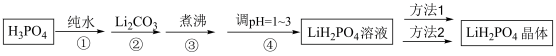
磷酸二氢锂作为锂电池正极新型材料磷酸铁锂的原料,还能用于有机反应的催化剂。某研究小组制备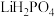 ,设计如下流程:
,设计如下流程:
已知: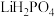 在20℃时溶解度为126g,且随温度变化不大,难溶于醇。
在20℃时溶解度为126g,且随温度变化不大,难溶于醇。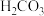 :
: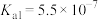 ,
, ;
; :
: ,
,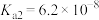 ,
,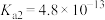 。
。
请回答:
(1)第②步中 反应完全的现象是
反应完全的现象是___________ 。
(2)第③步中煮沸的目的是___________ 。
(3)第④步调pH适合的物质是___________ (填化学式)。
(4)请给出方法l的操作顺序(从下列选项选择合适操作并按序排列):_________
活性炭脱色→(___________)→(___________)→(___________)→(___________)→干燥。
a.趁热过滤 b.蒸发至溶液出现晶膜,停止加热 c.冷却 d.减压过滤
e.蒸发至溶液中出现大量晶体,停止加热 f.乙醇洗涤 g.冷水洗涤
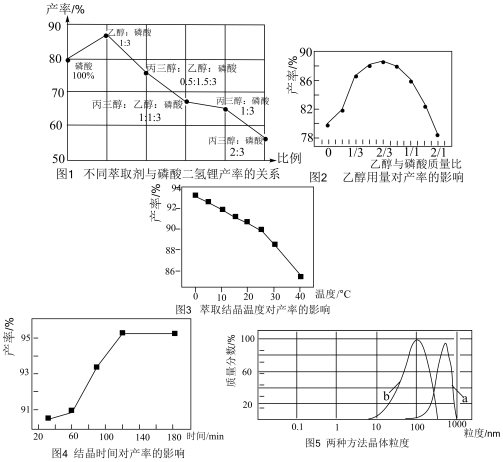
(5)方法2包括醇盐析、过滤、洗涤、干燥等步骤。根据以下图表判断,下列说法不正确 的是___________。
(6)若按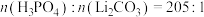 的比例,将98.0%的高纯碳酸锂50.0g加入到磷酸溶液中,应用方法2得到104.0g
的比例,将98.0%的高纯碳酸锂50.0g加入到磷酸溶液中,应用方法2得到104.0g 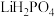 ,则
,则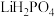 的产率为
的产率为___________ (保留三位有效数字)。
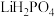 ,设计如下流程:
,设计如下流程:
已知:
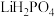 在20℃时溶解度为126g,且随温度变化不大,难溶于醇。
在20℃时溶解度为126g,且随温度变化不大,难溶于醇。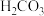 :
: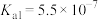 ,
, ;
; :
: ,
,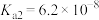 ,
,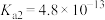 。
。请回答:
(1)第②步中
 反应完全的现象是
反应完全的现象是(2)第③步中煮沸的目的是
(3)第④步调pH适合的物质是
(4)请给出方法l的操作顺序(从下列选项选择合适操作并按序排列):
活性炭脱色→(___________)→(___________)→(___________)→(___________)→干燥。
a.趁热过滤 b.蒸发至溶液出现晶膜,停止加热 c.冷却 d.减压过滤
e.蒸发至溶液中出现大量晶体,停止加热 f.乙醇洗涤 g.冷水洗涤
(5)方法2包括醇盐析、过滤、洗涤、干燥等步骤。根据以下图表判断,下列说法

| A.由图1可知,丙三醇的加入会使磷酸二氢锂的产率下降,加入量越多,产率越低,原因是丙三醇粘度很大,严重影响产物的过滤 |
| B.由图2至图4可知,最佳控制条件是乙醇与磷酸质量比为2∶3,结晶温度0℃,结晶时间120min |
C.图5可知,方法1(a曲线)蒸发浓缩结晶时易得到大颗粒晶体,原因是水溶液中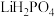 溶解度随温度变化较小,形成的晶核较少,晶体长大过程缓慢 溶解度随温度变化较小,形成的晶核较少,晶体长大过程缓慢 |
| D.图5可知,方法2(b曲线)乙醇盐析方法得到的晶体可用滤纸过滤 |
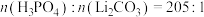 的比例,将98.0%的高纯碳酸锂50.0g加入到磷酸溶液中,应用方法2得到104.0g
的比例,将98.0%的高纯碳酸锂50.0g加入到磷酸溶液中,应用方法2得到104.0g 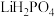 ,则
,则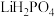 的产率为
的产率为
23-24高三上·浙江·开学考试 查看更多[2]
更新时间:2023-09-01 20:11:06
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可用于生产颜料铁红和补血剂乳酸亚铁。其生产工艺流程如图:(已知乳酸酸性强于碳酸)
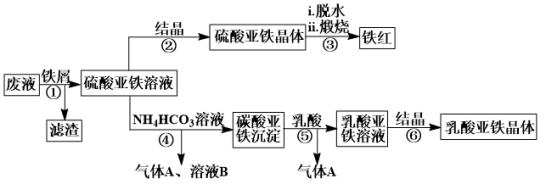
已知:①TiOSO4可溶于水,在水中可以电离为TiO2+和SO ;
;
②TiOSO4水解的反应为:TiOSO4+(x+1)H2O→TiO2•xH2O↓+H2SO4。
请回答:
(1)步骤①所得滤渣的主要成分为___ ,分离硫酸亚铁溶液和滤渣的操作中所用的玻璃仪器是___ ;步骤②中得到纯净硫酸亚铁晶体的操作为蒸发浓缩、___ 、___ 。
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为___ 。
(3)步骤④的离子方程式是___ 。
(4)实验室中常用KMnO4滴定法测定晶体中FeSO4·7H2O的质量分数,取步骤②中所得FeSO4·7H2O晶体样品ag,配成500.00mL溶液,取出25.00mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000mol•L-1KMnO4溶液25.00mL,所得晶体中FeSO4·7H2O的质量分数为(用a表示)__ 。

已知:①TiOSO4可溶于水,在水中可以电离为TiO2+和SO
 ;
;②TiOSO4水解的反应为:TiOSO4+(x+1)H2O→TiO2•xH2O↓+H2SO4。
请回答:
(1)步骤①所得滤渣的主要成分为
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为
(3)步骤④的离子方程式是
(4)实验室中常用KMnO4滴定法测定晶体中FeSO4·7H2O的质量分数,取步骤②中所得FeSO4·7H2O晶体样品ag,配成500.00mL溶液,取出25.00mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000mol•L-1KMnO4溶液25.00mL,所得晶体中FeSO4·7H2O的质量分数为(用a表示)
您最近一年使用:0次
【推荐2】综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如下图所示

(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解;②加过量的BaCl2溶液;③加过量的NaOH溶液;④加过量的Na2CO3溶液;⑤______ ;⑥加适量的盐酸;⑦蒸发结晶。
(2)碳酸氢钠固体受热分解的化学方程式是:_____ 。
(3)Mg(OH)2沉淀中因混有Ca(OH)2,可选用______ 溶液进行洗涤以除之。
(4)高温灼烧六水合氯化镁晶体(MgCl2·6H2O)所得固体是氧化镁,试写出该反应的化学方程式:______ 。
(5)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为:______ 。

(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解;②加过量的BaCl2溶液;③加过量的NaOH溶液;④加过量的Na2CO3溶液;⑤
(2)碳酸氢钠固体受热分解的化学方程式是:
(3)Mg(OH)2沉淀中因混有Ca(OH)2,可选用
(4)高温灼烧六水合氯化镁晶体(MgCl2·6H2O)所得固体是氧化镁,试写出该反应的化学方程式:
(5)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】天宫二号空间实验室已于2016 年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:

(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是______ (填化学式)
(2)“碳纤维复合材料制品”应用于“天宫二号”的推进系统。碳纤维复合材料具有重量轻、可设计强度高的特点。碳纤维复合材料由碳纤维和合成树脂组成,其中合成树脂是高分子化合物,则制备合成树脂的反应类型是_____________ 。
(3)太阳能电池帆板是“天宫二号”空间运行的动力源泉,其性能直接影响到“天宫二号”的运行寿命和可靠性。
① 天宫二号使用的光伏太阳能电池,该电池的核心材料是_____ ,其能量转化方式为_____ 。
② 下图是一种全天候太阳能电池的工作原理:
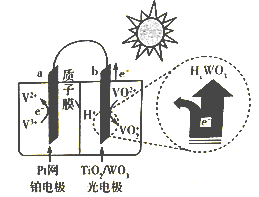
太阳照射时的总反应为V3++ VO2++ H2O=V2++VO2++2H+,则负极反应式为__________ ;夜间时,电池正极为______ (填“a”或“b”)。
(4)太阳能、风能发电逐渐得到广泛应用,下列说法中,正确的是______ ( 填字母序号)。
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(5)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+,Fe3+等)进行综合处理可实现钒资源的回收利用,流程如下:
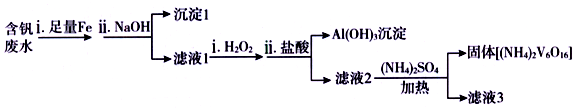
已知溶液pH 范围不同时,钒的存在形式如下表所示:
①加入NaOH 调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH 后生成沉淀1的反应过程为_______ 、_______ ;所得滤液1中,铝元素的存在形式为__________ 。
②向碱性的滤液1 ( V的化合价为+4 )中加入H2O2的作用是________ (用离子方程式表示)。

(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是
(2)“碳纤维复合材料制品”应用于“天宫二号”的推进系统。碳纤维复合材料具有重量轻、可设计强度高的特点。碳纤维复合材料由碳纤维和合成树脂组成,其中合成树脂是高分子化合物,则制备合成树脂的反应类型是
(3)太阳能电池帆板是“天宫二号”空间运行的动力源泉,其性能直接影响到“天宫二号”的运行寿命和可靠性。
① 天宫二号使用的光伏太阳能电池,该电池的核心材料是
② 下图是一种全天候太阳能电池的工作原理:

太阳照射时的总反应为V3++ VO2++ H2O=V2++VO2++2H+,则负极反应式为
(4)太阳能、风能发电逐渐得到广泛应用,下列说法中,正确的是
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(5)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+,Fe3+等)进行综合处理可实现钒资源的回收利用,流程如下:

已知溶液pH 范围不同时,钒的存在形式如下表所示:
| 钒的化合价 | pH<2 | pH>11 |
| +4价 | VO2+,VO(OH)+ | VO(OH)3- |
| +5价 | VO2+ | VO43- |
①加入NaOH 调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH 后生成沉淀1的反应过程为
②向碱性的滤液1 ( V的化合价为+4 )中加入H2O2的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】“侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某学习小组模拟“侯氏制碱法”开展如下项目化学习:
项目一、粗盐(含Ca2+、Mg2+、 等杂质)提纯氯化钠
等杂质)提纯氯化钠
粗盐提纯的流程如下:

(1)试剂X为___________ 。
(2)“操作1”所需玻璃仪器为烧杯、___________ 。
(3)“沉淀”的成分为CaCO3、Mg(OH)2、___________ 。
(4)“滤液”中加入稀盐酸生成气泡的离子方程式为___________ 。
项目二、模拟“侯氏制碱法”制备纯碱

(5)气体A为___________ 。
(6)“悬浊液”过滤所得滤液中含有的主要离子有___________ 。
(7)写出晶体转化为纯碱的化学方程式___________ 。
项目一、粗盐(含Ca2+、Mg2+、
 等杂质)提纯氯化钠
等杂质)提纯氯化钠粗盐提纯的流程如下:

(1)试剂X为
(2)“操作1”所需玻璃仪器为烧杯、
(3)“沉淀”的成分为CaCO3、Mg(OH)2、
(4)“滤液”中加入稀盐酸生成气泡的离子方程式为
项目二、模拟“侯氏制碱法”制备纯碱

(5)气体A为
(6)“悬浊液”过滤所得滤液中含有的主要离子有
(7)写出晶体转化为纯碱的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】在过滤、蒸发、蒸馏、萃取的操作过程中,有哪些注意事项呢?___
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
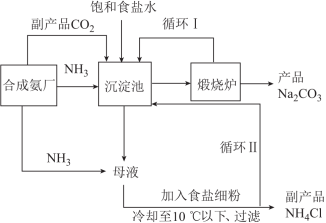
【推荐3】海洋是巨大的资源宝库,从海水得到纯碱的生产工艺如图所示:

回答下列问题:
(1)海水晒盐一般不直接蒸干,蒸发至大部分 析出后将苦卤从排水渠中排出,苦卤可用于制备多种化工原料。
析出后将苦卤从排水渠中排出,苦卤可用于制备多种化工原料。
①晒盐不直接蒸干的原因是_______ ,减少精制的步骤和成本。
②不直接用海水制备 、
、 等化工原料,而用苦卤的原因是
等化工原料,而用苦卤的原因是_______ 。
(2)粗盐中含少量 和泥沙,精制过程是将大量粗盐溶于水,依次加入
和泥沙,精制过程是将大量粗盐溶于水,依次加入 溶液和
溶液和 溶液,过滤后加入稀盐酸中和。已知:常温下,
溶液,过滤后加入稀盐酸中和。已知:常温下, 。测得加入
。测得加入 溶液后,
溶液后, ,此时溶液中
,此时溶液中
_______ 。
(3)向饱和食盐水中通入 和
和 时,应先通入
时,应先通入_______ (填化学式),写出生成晶体A总反应的离子方程式:_______ 。
(4)“操作1”是_______ ,“加热”时能产生一种可循环利用的物质是_______ ,(填化学式)。
(5)工业利用饱和食盐水制纯碱一般采用侯氏制碱法(如图所示),关于该制碱法,下列说法正确的是_______(填选项字母)。
(6)写出纯碱的一种用途:_______ 。

回答下列问题:
(1)海水晒盐一般不直接蒸干,蒸发至大部分
 析出后将苦卤从排水渠中排出,苦卤可用于制备多种化工原料。
析出后将苦卤从排水渠中排出,苦卤可用于制备多种化工原料。①晒盐不直接蒸干的原因是
②不直接用海水制备
 、
、 等化工原料,而用苦卤的原因是
等化工原料,而用苦卤的原因是(2)粗盐中含少量
 和泥沙,精制过程是将大量粗盐溶于水,依次加入
和泥沙,精制过程是将大量粗盐溶于水,依次加入 溶液和
溶液和 溶液,过滤后加入稀盐酸中和。已知:常温下,
溶液,过滤后加入稀盐酸中和。已知:常温下, 。测得加入
。测得加入 溶液后,
溶液后, ,此时溶液中
,此时溶液中
(3)向饱和食盐水中通入
 和
和 时,应先通入
时,应先通入(4)“操作1”是
(5)工业利用饱和食盐水制纯碱一般采用侯氏制碱法(如图所示),关于该制碱法,下列说法正确的是_______(填选项字母)。

| A.理论上侯氏制碱法的原子利用率为100%,无污染 |
B.循环Ⅱ进入沉淀池, 利用率大大增加 利用率大大增加 |
C.母液加食盐细粉是为了提高 ,促进 ,促进 析出 析出 |
| D.制碱过程利用了物质溶解度的差异 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
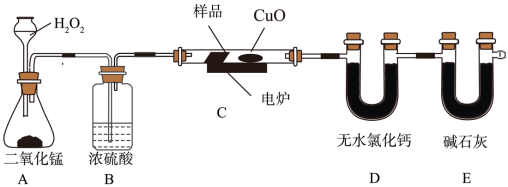
【推荐1】下列装置中有机物样品在电炉中充分燃烧,通过测定生成的CO2和H2O的质量,来确定有机物分子式。
(1)A装置是提供实验所需的O2,则A装置中二氧化锰的作用是______ ,B装置中浓硫酸的作用是_______ ;C中CuO的作用是____________ 。
(2)D装置中无水氯化钙的作用是___________ ;E装置中碱石灰的作用是________ 。
(3)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.44 g样品,经充分反应后,D管质量增加0.36g,E管质量增加0.88 g,已知该物质的相对分子质量为44,则该样品的化学式为_________ 。
(4)若该有机物的核磁共振氢谱如下图所示,峰面积之比为1:3则其结构简式为__________________ ;
若符合下列条件,则该有机物的结构简式为_____________________ 。①环状化合物②只有一种类型的氢原子
(5)某同学认E和空气相通,会影响测定结果准确性,应在E后再增加一个装置E,其主要目的是_________ 。
(1)A装置是提供实验所需的O2,则A装置中二氧化锰的作用是
(2)D装置中无水氯化钙的作用是
(3)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.44 g样品,经充分反应后,D管质量增加0.36g,E管质量增加0.88 g,已知该物质的相对分子质量为44,则该样品的化学式为
(4)若该有机物的核磁共振氢谱如下图所示,峰面积之比为1:3则其结构简式为

若符合下列条件,则该有机物的结构简式为
(5)某同学认E和空气相通,会影响测定结果准确性,应在E后再增加一个装置E,其主要目的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】含氮化合物是重要的化工原料。存在如下转化关系:
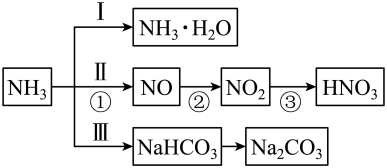
(1)转化Ⅱ中发生的系列反应,在工业上可以用来制备硝酸,写出①中反应的化学方程式为___________ 。
(2)①工业上常用浓氨水检验氯气管道是否泄漏,若泄露可看到白烟,用方程式解释检验原理___________ 。
②向固体氧化钙中滴加浓氨水,可用于实验室制取少量氨气,请结合化学用语简述原理___________ 。
(3)现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱。
①向一水合氨中通入过量的 CO2,该反应的离子方程式为___________ 。
②某工业纯碱样品中含少量 NaCl 和 NaHCO3,为测定该样品中 NaHCO3的质量分数, 某同学设计方案如下:准确称取 100.00 g 样品,反复加热、冷却、称量,直至所称量的固体质量几乎不变为止, 此时所得固体的质量为 99.38 g 。样品中 NaHCO3的质量分数为___________ 。
(4)以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高、无污染等特点。工作原理如图所示:

①固体氧化物电池工作的电解质,O2-移向___________ (填字母)。
A.电极a B.电极b
②该电池工作时, 电极a上发生的电极反应为___________ 。

(1)转化Ⅱ中发生的系列反应,在工业上可以用来制备硝酸,写出①中反应的化学方程式为
(2)①工业上常用浓氨水检验氯气管道是否泄漏,若泄露可看到白烟,用方程式解释检验原理
②向固体氧化钙中滴加浓氨水,可用于实验室制取少量氨气,请结合化学用语简述原理
(3)现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱。
①向一水合氨中通入过量的 CO2,该反应的离子方程式为
②某工业纯碱样品中含少量 NaCl 和 NaHCO3,为测定该样品中 NaHCO3的质量分数, 某同学设计方案如下:准确称取 100.00 g 样品,反复加热、冷却、称量,直至所称量的固体质量几乎不变为止, 此时所得固体的质量为 99.38 g 。样品中 NaHCO3的质量分数为
(4)以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高、无污染等特点。工作原理如图所示:

①固体氧化物电池工作的电解质,O2-移向
A.电极a B.电极b
②该电池工作时, 电极a上发生的电极反应为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】莫尔盐[ ,相对分子质量为392]能溶于水,难溶于无水乙醇,是一种重要的还原剂,在空气中比一般的亚铁盐稳定。某兴趣小组欲制备莫尔盐并测定其纯度,采用的方法是先在封闭体系中利用铁和稀硫酸制备硫酸亚铁溶液,再用制得的硫酸亚铁溶液和硫酸铵饱和溶液反应制得。实验装置如图所示,回答下列问题:
,相对分子质量为392]能溶于水,难溶于无水乙醇,是一种重要的还原剂,在空气中比一般的亚铁盐稳定。某兴趣小组欲制备莫尔盐并测定其纯度,采用的方法是先在封闭体系中利用铁和稀硫酸制备硫酸亚铁溶液,再用制得的硫酸亚铁溶液和硫酸铵饱和溶液反应制得。实验装置如图所示,回答下列问题:

(1)仪器a的名称为_______ 。配制硫酸铵饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是_______ 。
(2)待C中逸出 较为纯净后,
较为纯净后,_______ (填具体操作),A中液体会自动流入B中。此时B中发生的主要反应的化学方程式为_______ 。
(3)制备结束后,将B中固液混合物过滤,所得莫尔盐可用_______ (填试剂名称)进行洗涤。
(4)装置C的作用为_______ 。
(5)实验小组对样品进行纯度检测,取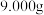 样品配成
样品配成 溶液,从中取出
溶液,从中取出 溶液,用
溶液,用 的酸性
的酸性 溶液滴定,消耗酸性
溶液滴定,消耗酸性 溶液
溶液 ,该样品的纯度为
,该样品的纯度为_______ (保留至0.1%),写出计算过程。
 ,相对分子质量为392]能溶于水,难溶于无水乙醇,是一种重要的还原剂,在空气中比一般的亚铁盐稳定。某兴趣小组欲制备莫尔盐并测定其纯度,采用的方法是先在封闭体系中利用铁和稀硫酸制备硫酸亚铁溶液,再用制得的硫酸亚铁溶液和硫酸铵饱和溶液反应制得。实验装置如图所示,回答下列问题:
,相对分子质量为392]能溶于水,难溶于无水乙醇,是一种重要的还原剂,在空气中比一般的亚铁盐稳定。某兴趣小组欲制备莫尔盐并测定其纯度,采用的方法是先在封闭体系中利用铁和稀硫酸制备硫酸亚铁溶液,再用制得的硫酸亚铁溶液和硫酸铵饱和溶液反应制得。实验装置如图所示,回答下列问题:
(1)仪器a的名称为
(2)待C中逸出
 较为纯净后,
较为纯净后,(3)制备结束后,将B中固液混合物过滤,所得莫尔盐可用
(4)装置C的作用为
(5)实验小组对样品进行纯度检测,取
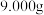 样品配成
样品配成 溶液,从中取出
溶液,从中取出 溶液,用
溶液,用 的酸性
的酸性 溶液滴定,消耗酸性
溶液滴定,消耗酸性 溶液
溶液 ,该样品的纯度为
,该样品的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】稀土金属是我国战略性资源。氟碳铈矿主要化学成分为CeFCO3,它是提取铈族稀土元素的重要矿物原料。其中一种提取铈的工艺流程如下:
已知:焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物;+ 4价的铈的氧化物有很强的氧化性,通常在酸性条件下易被还原剂还原成+3价而溶于水。请回答下列问题
(1)酸浸l中所用的酸A为(用字母表示)________ (a.盐酸 b.稀硫酸),原因是_______ 。
(2)酸浸Ⅱ后,为避免三价铈以四氟硼酸盐形式损失,需用可溶性钾盐将四氟硼酸根离子沉淀除去,该反应的离子方程式为___________ 。
(3)实验室中进行萃取操作所用到的主要玻璃仪器名称是________ ;在操作I后的溶液中加入NaOH溶液是为了调节溶液pH 获得Ce(OH)3和_______ ,测定该溶液pH的操作是_______ 。
(4)写出氧化步骤的化学方程式_______________ 。
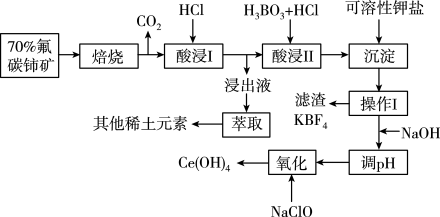
已知:焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物;+ 4价的铈的氧化物有很强的氧化性,通常在酸性条件下易被还原剂还原成+3价而溶于水。请回答下列问题
(1)酸浸l中所用的酸A为(用字母表示)
(2)酸浸Ⅱ后,为避免三价铈以四氟硼酸盐形式损失,需用可溶性钾盐将四氟硼酸根离子沉淀除去,该反应的离子方程式为
(3)实验室中进行萃取操作所用到的主要玻璃仪器名称是
(4)写出氧化步骤的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】以软锰矿(主要成分是MnO2,还含有Fe2O3、SiO2、CuO、CaO等少量杂质)为主要原料制备硫酸锰晶体的工艺流程如图所示,回答下列问题: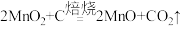 ;
;
② 在酸性条件下比较稳定,pH高于5.5时易被
在酸性条件下比较稳定,pH高于5.5时易被 氧化;
氧化;
③ ,
, ;离子浓度
;离子浓度 时,可认为完全沉淀。
时,可认为完全沉淀。
④ 溶于1份冷水、0.6份沸水,不溶于乙醇;
溶于1份冷水、0.6份沸水,不溶于乙醇;
(1)基态Mn原子的价电子排布式为___________ ,“过滤Ⅰ”得到的滤渣主要成分除了C、Cu、SiC,还有___________ (填化学式)。
(2)“氧化”时发生反应的离子方程式为___________ 。
(3)“调pH”时溶液中 的浓度约为
的浓度约为 ,常温下,调节pH的合理范围是
,常温下,调节pH的合理范围是___________ 。
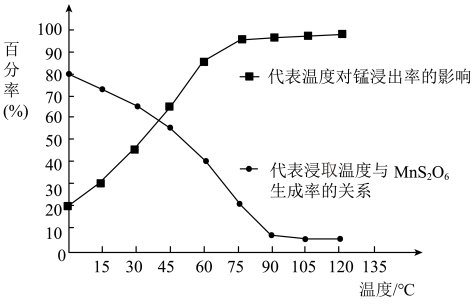
(4)“浸取”时,反应中往往有副产物MnS2O6生成,温度对浸取反应的影响如图所示,为减少MnS2O6的生成,“浸取”的适宜温度是___________ ;向过滤Ⅱ所得的“滤液”中加入NH4HCO3溶液时温度不宜太高的原因是___________ 。___________ 。
(6)获得MnSO4·H2O后常用乙醇洗涤,主要目的是___________ 。
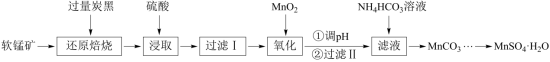
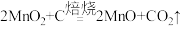 ;
;②
 在酸性条件下比较稳定,pH高于5.5时易被
在酸性条件下比较稳定,pH高于5.5时易被 氧化;
氧化;③
 ,
, ;离子浓度
;离子浓度 时,可认为完全沉淀。
时,可认为完全沉淀。④
 溶于1份冷水、0.6份沸水,不溶于乙醇;
溶于1份冷水、0.6份沸水,不溶于乙醇;(1)基态Mn原子的价电子排布式为
(2)“氧化”时发生反应的离子方程式为
(3)“调pH”时溶液中
 的浓度约为
的浓度约为 ,常温下,调节pH的合理范围是
,常温下,调节pH的合理范围是(4)“浸取”时,反应中往往有副产物MnS2O6生成,温度对浸取反应的影响如图所示,为减少MnS2O6的生成,“浸取”的适宜温度是
(6)获得MnSO4·H2O后常用乙醇洗涤,主要目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氮化锂在电池、光电子、化学合成、催化剂和材料科学等领域有重要应用。在空气中即发生化学变化,可在高温下短时间内用锂和氮气直接反应进行合成。实验室制备氮化锂的反应装置如图所示。

(1)氮化锂遇水立即反应,反应的方程式为___________ 。
(2)在制备氮化锂实验开始时,应该先点燃___________ (填“装置A”或“装置D”)处的酒精灯,原因是___________ 。
(3)为测定 (主要杂质为
(主要杂质为 )产品纯度,按如图所示装置进行实验。实验开始前需要检查该装置的气密性,操作方法及现象为
)产品纯度,按如图所示装置进行实验。实验开始前需要检查该装置的气密性,操作方法及现象为___________ 。

(4)接上题,在操作得当的前提下,将ag产品置于装置Ⅰ中反应,待反应完毕并冷却之后,量气管①测得气体体积为 (已换算成标准状况,下同),将bg产品置于装置Ⅱ中反应,待反应完毕并冷却之后,量气管②测得气体体积为
(已换算成标准状况,下同),将bg产品置于装置Ⅱ中反应,待反应完毕并冷却之后,量气管②测得气体体积为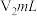 。则该样品的纯度为
。则该样品的纯度为___________ 。与其他分析法相比,该法所测得样品纯度均偏小,其可能原因是___________ 。
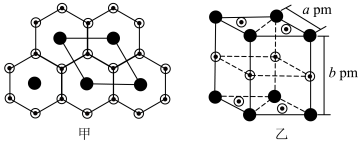
(5)氮化锂晶体属于混合型晶体。在一层中 原子以石墨晶体中的C原子方式排布,N原子则处在六元环的中心,如图甲所示,则该层中锂、氮的原子个数比为
原子以石墨晶体中的C原子方式排布,N原子则处在六元环的中心,如图甲所示,则该层中锂、氮的原子个数比为___________ ;氮化锂的晶胞如图乙所示,同层 间距为apm,两层间距为bpm,阿伏加德罗常数为
间距为apm,两层间距为bpm,阿伏加德罗常数为 ,该物质的密度为
,该物质的密度为___________  (用含a、b的式子表示)。
(用含a、b的式子表示)。

(1)氮化锂遇水立即反应,反应的方程式为
(2)在制备氮化锂实验开始时,应该先点燃
(3)为测定
 (主要杂质为
(主要杂质为 )产品纯度,按如图所示装置进行实验。实验开始前需要检查该装置的气密性,操作方法及现象为
)产品纯度,按如图所示装置进行实验。实验开始前需要检查该装置的气密性,操作方法及现象为
(4)接上题,在操作得当的前提下,将ag产品置于装置Ⅰ中反应,待反应完毕并冷却之后,量气管①测得气体体积为
 (已换算成标准状况,下同),将bg产品置于装置Ⅱ中反应,待反应完毕并冷却之后,量气管②测得气体体积为
(已换算成标准状况,下同),将bg产品置于装置Ⅱ中反应,待反应完毕并冷却之后,量气管②测得气体体积为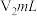 。则该样品的纯度为
。则该样品的纯度为(5)氮化锂晶体属于混合型晶体。在一层中
 原子以石墨晶体中的C原子方式排布,N原子则处在六元环的中心,如图甲所示,则该层中锂、氮的原子个数比为
原子以石墨晶体中的C原子方式排布,N原子则处在六元环的中心,如图甲所示,则该层中锂、氮的原子个数比为 间距为apm,两层间距为bpm,阿伏加德罗常数为
间距为apm,两层间距为bpm,阿伏加德罗常数为 ,该物质的密度为
,该物质的密度为 (用含a、b的式子表示)。
(用含a、b的式子表示)。
您最近一年使用:0次



