设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.常温常压下,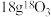 所含的质子数为 所含的质子数为 |
B. 液态水完全转化为固态冰,则最多新形成的氢键数为 液态水完全转化为固态冰,则最多新形成的氢键数为 |
C.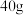 的金刚砂( 的金刚砂( )中,所含的碳硅键个数为: )中,所含的碳硅键个数为: |
D.标准状况下 的乙炔与氢气完全加成,共有 的乙炔与氢气完全加成,共有 的共价键发生断裂 的共价键发生断裂 |
更新时间:2023-09-02 14:57:28
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】NA代表阿伏加 德罗常数的值。下列说法正确的是
| A.标准状况下,11.2L CO2中含有的共用电子对数为NA |
| B.2g由D2O与 20Ne组成的混合气体中含有的质子数为NA |
| C.常温下, 27g铝投入足量的浓硫酸中,生成的SO2分子数为NA |
| D.100mL 1mol·L−1 FeCl3溶液中所含Fe3+的数目为0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA为阿伏伽德罗常数的值。下列叙述正确的是
| A.标准状况下,11.2 L的SO3中含有的电子数为20NA |
| B.88g CO2和N2O组成的混合气体中所有的原子数为6NA |
| C.2mol NO和 1mol O2充分反应后所得气体分子数为2NA |
| D.常温下,1L 0.1mol•L-1的 Na2S 的溶液中,阴离子的总数小于0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】聚乙酸乙烯酯广泛用于制备乳胶漆和粘合剂,一种以乙炔为原料制备聚乙酸乙烯酯的有机合成路线如下图所示:
HC≡CH
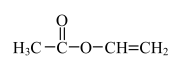

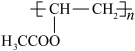
下列有关说法正确的是
HC≡CH

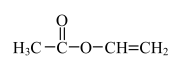

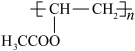
下列有关说法正确的是
| A.物质A为CH3COOH |
| B.反应1为加成反应,反应2为缩聚反应 |
| C.聚乙酸乙烯酯在碱性环境下的水解产物之一可以直接参与该合成路线实现循环利用 |
D.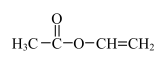 的同分异构体中,能与NaHCO3溶液发生反应的有2种 的同分异构体中,能与NaHCO3溶液发生反应的有2种 |
您最近一年使用:0次
【推荐2】 溶液可用于除去乙炔
溶液可用于除去乙炔 中的杂质气体
中的杂质气体 、
、 发生的反应:
发生的反应:
①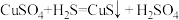
②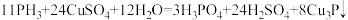
下列分析正确的是
 溶液可用于除去乙炔
溶液可用于除去乙炔 中的杂质气体
中的杂质气体 、
、 发生的反应:
发生的反应:①
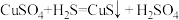
②
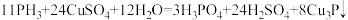
下列分析正确的是
| A.反应①可说明硫酸的酸性弱于硫化氢的酸性 |
B.反应②中 作还原剂,被还原 作还原剂,被还原 |
C.可用溴水除去乙炔中的杂质气体 和 和 |
D.反应②中每生成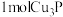 ,转移电子的物质的量为 ,转移电子的物质的量为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计 | 现象和结论 |
| A | 探究乙炔是否含不饱和键 | 将电石与饱和食盐水反应生成的气体通入溴水 | 溶液褪色,说明乙炔含不饱和键 |
| B | 验证苯和液溴在 的催化下发生取代反应 的催化下发生取代反应 | 将反应产生的混合气体通入 溶液中 溶液中 | 有淡黄色沉淀生成,说明发生取代反应 |
| C | 探究有机物基因之间的相互影响 | 取三支试管各加入等量的己烷、苯、甲苯,分别加入几滴等量的酸性 溶液(必要时可稍稍加热) 溶液(必要时可稍稍加热) | 加入甲苯中的溶液褪色,其他两支试管中溶液不褪色,说明苯环对甲基有影响,使甲基更易被氧化 |
| D | 研究淀粉的水解程度 | 取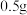 淀粉于试管,加入适量20%的硫酸溶液后沸水浴加热 淀粉于试管,加入适量20%的硫酸溶液后沸水浴加热 ,再滴加过量氢氧化钠溶液,再加入适量碘水 ,再滴加过量氢氧化钠溶液,再加入适量碘水 | 若溶液没有变成蓝色,则淀粉已经水解完全 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各种说法中不正确的是



| A.在水中氢、氧原子间均以共价键相结合 |
| B.离子键是阳离子、阴离子的静电作用 |
C. 和 和 的反应过程涉及了共价键的断裂和形成 的反应过程涉及了共价键的断裂和形成 |
| D.金属具有金属光泽及良好的导电性和导热性,这些性质均与金属键有关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法不正确的是
A. 、 、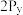 、 、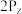 轨道相互垂直,但能量相等 轨道相互垂直,但能量相等 |
| B.最外层电子数为2的元素都分布在s区 |
C.“ ”中三原子不在一条直线上时,也能形成氢键 ”中三原子不在一条直线上时,也能形成氢键 |
D.价层电子对互斥模型中, 键电子对数不计入中心原子的价层电子对数 键电子对数不计入中心原子的价层电子对数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.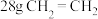 和 和 的混合气体中所含原子数可能为 的混合气体中所含原子数可能为 |
B.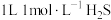 溶液中含有的 溶液中含有的 数目为 数目为 |
C.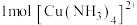 中所含σ键的数目为 中所含σ键的数目为 |
D.18g冰晶体中含有的氢键数目为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 是原子序数依次增大的短周期主族元素。基态
是原子序数依次增大的短周期主族元素。基态 原子核外电子有3种空间运动状态;
原子核外电子有3种空间运动状态; 是自然界中形成化合物最多的元素;
是自然界中形成化合物最多的元素; 的简单氢化物与其最高价氧化物对应水化物可发生反应;与
的简单氢化物与其最高价氧化物对应水化物可发生反应;与 同周期的元素中,第一电离能大于
同周期的元素中,第一电离能大于 的有三种;
的有三种; 与
与 同主族。下列说法正确的是
同主族。下列说法正确的是
 是原子序数依次增大的短周期主族元素。基态
是原子序数依次增大的短周期主族元素。基态 原子核外电子有3种空间运动状态;
原子核外电子有3种空间运动状态; 是自然界中形成化合物最多的元素;
是自然界中形成化合物最多的元素; 的简单氢化物与其最高价氧化物对应水化物可发生反应;与
的简单氢化物与其最高价氧化物对应水化物可发生反应;与 同周期的元素中,第一电离能大于
同周期的元素中,第一电离能大于 的有三种;
的有三种; 与
与 同主族。下列说法正确的是
同主族。下列说法正确的是| A.P元素形成的单质在常温下为固态,属于分子晶体 |
B.化合物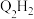 中, 中, 键与 键与 键的数目之比为 键的数目之比为 |
C. 最高价氧化物对应的水化物可与氨水发生复分解反应 最高价氧化物对应的水化物可与氨水发生复分解反应 |
D.简单离子半径: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】不久前,科学家研发了一种能让人如鱼那样从水中持续不断吸收氧气的水晶材料——“海王水晶”,其吸收氧气的能力依靠的是钴离子。下列有关说法正确的是
| A.氧气在水中溶解度小是因为O2是非极性分子 |
| B.H2O分子内存在的化学键按分类有极性键、σ键和氢键 |
| C.矿物水晶的结构式为O=Si=O |
| D.钴元素位于元素周期表VIIIB族 |
您最近一年使用:0次


 键的个数为
键的个数为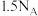
 中所含的离子总数为
中所含的离子总数为
 含有
含有 键的个数为
键的个数为 个
个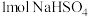 晶体中,含阳离子数目为
晶体中,含阳离子数目为

