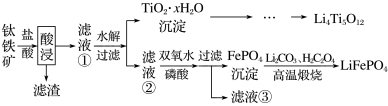
大力推广锂电池新能源汽车对实现“碳达峰”和“碳中和”具有重要意义。Li4Ti5O12与LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还有少量MgO、SiO2等杂质)来制备,工艺流程如图:
已知:“酸浸”后,钛主要以TiOCl 好形式存在,
好形式存在,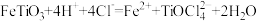 。下列说法不正确的是
。下列说法不正确的是

已知:“酸浸”后,钛主要以TiOCl
 好形式存在,
好形式存在,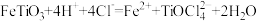 。下列说法不正确的是
。下列说法不正确的是| A.在制备TiO2·xH2O时需要加入水,同时加热,促使水解反应趋于完全 |
| B.高温煅烧反应中氧化产物与还原产物物质的量之比为3:2 |
| C.滤液②中的阳离子有Fe2+、Mg2+、H+ |
| D.在制备Li4Ti5O12的过程中会生成Li5Ti5O15(Ti为+4价),则Li2Ti5O15中过氧键的数目为4 |
23-24高三上·安徽·阶段练习 查看更多[2]
更新时间:2023-10-08 09:40:44
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】PbO2是褐色固体,受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将一定量的PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2。反应中生成的O2和Cl2 的物质的量之比为3:2,分解释放O2后固体的组成及物质的量比是
| A.1:1混合的Pb3O4, PbO | B.1:2混合的PbO2, Pb3O4 |
| C.2:1:4混合的PbO2, Pb3O4, PbO | D.1:2:4混合的PbO2, Pb3O4, PbO |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知氮氧化物(可用NOx表示)能与NH3发生反应NOx+NH3→N2+H2O(方程式为配平)。现有NO、NO2的混合气体3L,用同温同压下3.6LNH3使其恰好完全转化为N2,则混合气体中NO、NO2的物质的量之比为
| A.1:1 | B.2:1 | C.1:3 | D.1:4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】某同学用表格中的试剂和操作除去下列物质中的杂质,不合理的是
| 选项 | 物质及杂质 | 试剂和操作 |
| A | 乙醇中混有少量的乙酸 | NaOH溶液,蒸馏 |
| B | 甲烷中混有乙烯 | 酸性KMnO4溶液,洗气 |
| C | 溴苯中混有溴 | NaOH溶液,分液 |
| D | 乙醇中混有少量的水 | 生石灰,蒸馏 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】工业上应用两矿法漫出软锰矿(主要成分MnO2)和方铅矿(主要成分PbS、FeS2)制备PbSO4和Mn3O4转化流程如图:
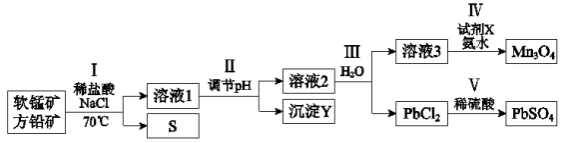
已知:PbCl2微溶于水,溶液中存在可逆反应:PbCl2+2Cl-
 。下列说法正确的是
。下列说法正确的是

已知:PbCl2微溶于水,溶液中存在可逆反应:PbCl2+2Cl-

 。下列说法正确的是
。下列说法正确的是| A.I中可使用浓盐酸代替稀盐酸和NaCl的混合溶液 |
| B.II中生成的沉淀Y是Fe(OH)3 |
| C.IV中试剂X可能作氧化剂 |
D.V中发生反应:Pb2++ = PbSO4 = PbSO4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】氧化锆是一种高级耐火材料,氧化钇主要用作制造微波用磁性材料。一种利用玻璃窑炉替换下的锆废砖(主要成分ZrO2、Y2O3、CaO等)提纯氧化锆和氧化钇的工艺流程如下:
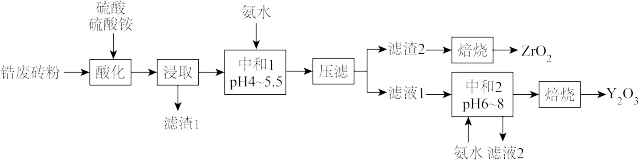
下列说法正确的是

下列说法正确的是
| A.“酸化”是锆废砖粉和硫酸在硫酸铵催化作用下进行的焙烧反应,硫酸适宜用盐酸代替 |
| B.“中和1”发生反应的离子方程式为Zr4+ +4OH- =Zr(OH)4 ↓ |
| C.实验室模拟“焙烧”时使用的硅酸盐仪器只有烧杯和酒精灯 |
| D.滤液2可以处理后返回“酸化”使用,实现循环 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
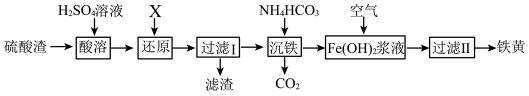
【推荐2】高铁酸钾(K2FeO4)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成Fe(OH)3胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下其氧化性强于Cl2、KMnO4等。工业上湿法制备K2FeO4的流程如下:
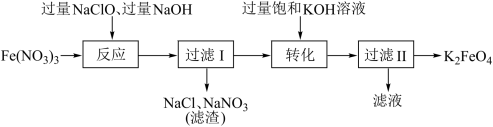
下列关于K2FeO4的工业湿法制备工艺,说法正确的是

下列关于K2FeO4的工业湿法制备工艺,说法正确的是
| A.“反应”中,参加反应的氧化剂和还原剂的物质的量之比为3:2 |
B.“过滤I”所得滤液中大量存在的离子有:Na+、Fe3+、Cl-、NO |
| C.“过滤Ⅱ”所得滤液进行焰色试验火焰呈黄色,说明滤液中不含有K+ |
| D.“过滤Ⅱ”后用乙醇洗涤K2FeO4,可降低其溶解损失并有利于K2FeO4快速干燥 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】以红土镍镉矿( 、
、 ,含
,含 、
、 、
、 、
、 等杂质)为原料回收部分金属单质,其工艺流程如图所示:
等杂质)为原料回收部分金属单质,其工艺流程如图所示:
下列说法错误的是
 、
、 ,含
,含 、
、 、
、 、
、 等杂质)为原料回收部分金属单质,其工艺流程如图所示:
等杂质)为原料回收部分金属单质,其工艺流程如图所示: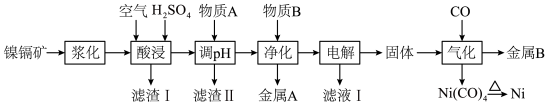
| 电对 | 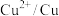 | 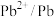 | 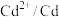 | 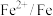 | 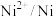 |
电极电位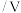 | +0.337 | -0.126 | -0.402 | -0.442 | -0.257 |
| A.“浆化”的目的是增大接触面积,加快酸浸反应速率,提高某些金属元素浸取率 |
B.“物质A”可以是 ,“调 ,“调 ”后,经加热得 ”后,经加热得 沉淀 沉淀 |
C.“金属A”是 和 和 混合物,“金属B”是 混合物,“金属B”是 |
D.该工艺流程中可以循环利用的物质有 、 、 、 、 等 等 |
您最近一年使用:0次

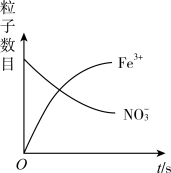
 、Fe3+、
、Fe3+、 、H+和H2O六种粒子,在反应过程中测得Fe3+、
、H+和H2O六种粒子,在反应过程中测得Fe3+、