取0.1mol∙L−1NaOH溶液100mL,然后向其通入一定量的CO2气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的CO2气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。下列说法正确的是


| A.通入CO2气体体积(标准状况)约为100mL |
| B.溶液A中所含溶质为Na2CO3 |
| C.0-25mL段:反应的离子方程式主要是:OH−+H+=H2O |
| D.完全反应后溶液中溶质的物质的物质的量浓度约为:0.7mol·L−1 |
更新时间:2023-09-17 08:28:09
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,2.24LCCl4与1.8gH2O含有相同的原子数 |
| B.常温常压下,1.6g氧气所含的分子数是0.05NA |
| C.1.8gD2O含有的电子数为0.1NA |
D.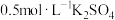 溶液中含有的钾离子数是NA 溶液中含有的钾离子数是NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上制备硫酸的流程: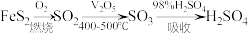 ,设
,设 为阿伏伽德罗常数,下列有关说法正确的是
为阿伏伽德罗常数,下列有关说法正确的是
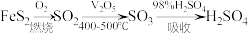 ,设
,设 为阿伏伽德罗常数,下列有关说法正确的是
为阿伏伽德罗常数,下列有关说法正确的是A. 中 中 的未成对电子数目为6 的未成对电子数目为6 |
B. 的中心原子孤对电子数为1,其空间构型为V型 的中心原子孤对电子数为1,其空间构型为V型 |
C.标准状况下,22.4L 中含有氧原子数目为 中含有氧原子数目为 |
D. 作催化剂,能降低该反应的活化能,提高 作催化剂,能降低该反应的活化能,提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于阿伏加德罗常数 的说法中正确的是
的说法中正确的是
 的说法中正确的是
的说法中正确的是A. 和足量水完全反应,转移电子数为 和足量水完全反应,转移电子数为 |
B.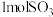 溶于足量水,所得溶液中 溶于足量水,所得溶液中 分子数为 分子数为 |
C. 乙烯 乙烯 和甲烷 和甲烷 的混合气中含有 的混合气中含有 键个数为 键个数为 |
D.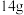 乙烯 乙烯 和丙烯 和丙烯 的混合气中,碳原子个数为 的混合气中,碳原子个数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的是
A.在标准状况下,22.4L水中含有 分子 分子 |
B. 在 在 中充分燃烧,生成 中充分燃烧,生成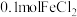 |
C.在标准状况下, 和CO2的混合气体中含氧原子共0.2mol 和CO2的混合气体中含氧原子共0.2mol |
D.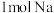 与一定量 与一定量 完全反应,生成 完全反应,生成 和 和 混合物,钠失去电子总数大于 混合物,钠失去电子总数大于 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.0.1 mol甲基中所含电子总数为NA |
| B.5.6 g铁粉与硫完全反应转移的电子总数为0. 3 NA |
| C.标准状况下,11.2 L HF中含有的原子数为NA |
| D.9.2 g甘油中所含C-H键的数目为0. 5 NA |
您最近一年使用:0次
【推荐1】将26.3g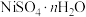 样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随温度变化的曲线)如图所示。已知:L→N时失掉全部的结晶水。下列说法错误的是
样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随温度变化的曲线)如图所示。已知:L→N时失掉全部的结晶水。下列说法错误的是
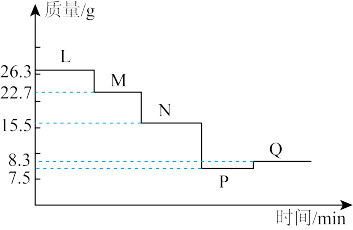
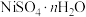 样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随温度变化的曲线)如图所示。已知:L→N时失掉全部的结晶水。下列说法错误的是
样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随温度变化的曲线)如图所示。已知:L→N时失掉全部的结晶水。下列说法错误的是
A. |
B.固体M的化学式为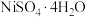 |
| C.生成固体P时,样品的失重率约为71.5% |
| D.固体Q的化学式为NiO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各项叙述中错误的是
| A.小苏打是面包发酵粉的主要成分之一 |
| B.用酚酞溶液可鉴别饱和食盐水和饱和纯碱溶液 |
C.等质量的 与 与 与足量盐酸反应, 与足量盐酸反应, 放出的二氧化碳气体多 放出的二氧化碳气体多 |
D.等物质的量的 和 和 与足量盐酸反应,相同状况下产生的二氧化碳体积相等 与足量盐酸反应,相同状况下产生的二氧化碳体积相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】将一定质量的镁和铝的固体混合物投入200mL稀盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示。

下列有关说法错误的是

下列有关说法错误的是
A.加入NaOH溶液的体积为200~240mL时反应的离子为Al(OH)3+OH-= +2H2O +2H2O |
| B.在反应过程中放出的气体在标准状况下的体积为11.76L |
| C.原固体混合物的质量为9g |
| D.所用NaOH溶液中NaOH的物质的量浓度为5mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列指定反应的离子方程式正确的是
A.向氢氧化钠溶液中通入足量的 气体: 气体: |
B.NaClO将污水中的 氧化成 氧化成 : : |
C.酸性条件下,用 将 将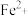 转化为 转化为 |
D.用醋酸除水垢: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关离子方程式书写正确的是
A.铅蓄电池放电时的正极反应: |
B. (二元弱酸)溶液中滴加少量的 (二元弱酸)溶液中滴加少量的 溶液: 溶液: |
C.“侯氏制碱法”中制备 : :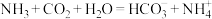 |
D.向明矾溶液中滴加 溶液至沉淀质量最大: 溶液至沉淀质量最大: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】向两份等体积、等浓度,pH不同的FeSO4溶液中逐滴加入NaClO溶液,实验测得溶液pH随加入NaClO(NaClO溶液pH>7)溶液体积变化曲线如下图,实验现象如下表。下列说法不正确 的是
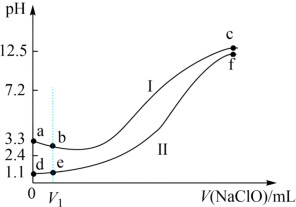
| 实验 | 实验现象 |
| Ⅰ | 滴入V1mLNaClO溶液产生大量红褐色沉淀 |
| Ⅱ | 滴入V1mLNaClO溶液,溶液变黄,未见沉淀,继续滴加出现红褐色沉淀 |

| A.a~b段主要反应的离子方程式为:2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+ |
| B.d~e段主要反应的离子方程式为:ClO-+H+=HClO |
| C.c、f点溶液呈碱性的原因是NaClO溶液过量 |
| D.向c点溶液中加入过量的浓盐酸,沉淀溶解并有刺激性气味的气体放出 |
您最近一年使用:0次



