工业上制备硫酸的流程: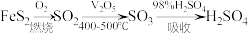 ,设
,设 为阿伏伽德罗常数,下列有关说法正确的是
为阿伏伽德罗常数,下列有关说法正确的是
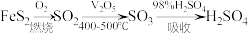 ,设
,设 为阿伏伽德罗常数,下列有关说法正确的是
为阿伏伽德罗常数,下列有关说法正确的是A. 中 中 的未成对电子数目为6 的未成对电子数目为6 |
B. 的中心原子孤对电子数为1,其空间构型为V型 的中心原子孤对电子数为1,其空间构型为V型 |
C.标准状况下,22.4L 中含有氧原子数目为 中含有氧原子数目为 |
D. 作催化剂,能降低该反应的活化能,提高 作催化剂,能降低该反应的活化能,提高 的平衡转化率 的平衡转化率 |
更新时间:2023-04-28 06:45:53
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】把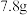 镁铝合金的粉末放入过量的盐酸中,得到
镁铝合金的粉末放入过量的盐酸中,得到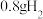 。下列说法错误的是
。下列说法错误的是
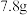 镁铝合金的粉末放入过量的盐酸中,得到
镁铝合金的粉末放入过量的盐酸中,得到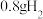 。下列说法错误的是
。下列说法错误的是A.合金中铝的质量分数约为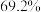 | B.合金中镁和铝的物质的量之比为 |
C.镁和铝还原出的 体积之比为 体积之比为 | D.在标准状况下,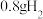 的体积为 的体积为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值。下列叙述正确的是
A.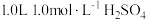 溶液中含有的氢原子总数为2NA 溶液中含有的氢原子总数为2NA |
| B.11.2L由甲烷和乙烯组成的混合物中含有的氢原子数为2NA |
C.光照条件下,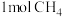 与足量的 与足量的 充分反应后,得到 充分反应后,得到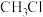 分子的总数为NA 分子的总数为NA |
D.常温常压下,11g由 和 和 组成的混合气体中含有的原子总数为0.75NA 组成的混合气体中含有的原子总数为0.75NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值。下列说法正确的是
A.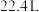 (标准状况)臭氧气体中所含的质子数为18NA (标准状况)臭氧气体中所含的质子数为18NA |
B.  和 和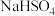 的固体混合物中含有的离子总数为0.4NA 的固体混合物中含有的离子总数为0.4NA |
C.实验室制得  转移的电子数不一定为2NA 转移的电子数不一定为2NA |
D. 氮气与足量金属镁反应,转移的电子数为0.4NA 氮气与足量金属镁反应,转移的电子数为0.4NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】“轨道”2px与3py上电子一定相同的方面是
| A.能量 | B.呈哑铃形 | C.自旋方向 | D.空间的伸展方向 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法中正确的是
| A.Br-的核外电子排布式:[Ar]4s24p6 |
| B.乙烯分子中,碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键 |
| C.键长:H-F<H-Cl<H-Br<H-I,因此稳定性:HF<HCl<HBr<HI |
| D.PH3分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】铁氰化钾(又名六氰合铁酸钾,化学式为 )和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为
)和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为 )是两种灵敏的可用于检验
)是两种灵敏的可用于检验 和
和 的物质:铁氰化钾可在酸性环境下被羟胺
的物质:铁氰化钾可在酸性环境下被羟胺 等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。下列对相关物质的说法,正确的一项是
等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。下列对相关物质的说法,正确的一项是
 )和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为
)和亚铁氰化钾(又名六氰合亚铁酸钾,化学式为 )是两种灵敏的可用于检验
)是两种灵敏的可用于检验 和
和 的物质:铁氰化钾可在酸性环境下被羟胺
的物质:铁氰化钾可在酸性环境下被羟胺 等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。下列对相关物质的说法,正确的一项是
等强还原剂还原为亚铁氰化钾,亚铁氰化钾也可被氯气氧化为铁氰化钾,可用于两者间的互相转化。合理应用含铁的化合物,在生产生活中有重要意义。下列对相关物质的说法,正确的一项是A. 的价层电子排布式为 的价层电子排布式为 |
B. 中含有离子键、共价键和配位键 中含有离子键、共价键和配位键 |
C.羟胺分子为平面结构,中心氧原子为 杂化 杂化 |
D.铁的两种常见离子 和 和 相比较, 相比较, 更稳定 更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】普通玻璃的主要成分为Na2SiO3、CaSiO3和SiO2,它是以纯碱、石灰石和石英砂(主要成分为SiO2)为原料,经混合,粉碎,在玻璃窑中熔融,发生复杂的物理变化和化学变化制得的。下列说法正确的是
| A.沸点:SiO2<Na2CO3 |
| B.SiO2的VSEPR模型与空间结构均为平面三角形 |
| C.Na2SiO3和CaCO3分别与足量的稀盐酸反应,反应后均无新的沉淀产生 |
| D.0.1 mol SiO2的质量为6 g |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】氮元素形成的单质和化合物在化工和能源领域占有重要地位,如 、
、 、苯胺等。其中
、苯胺等。其中 分子的结构示意图如图所示,每个N原子均满足最外层
分子的结构示意图如图所示,每个N原子均满足最外层 结构。下列说法错误的是
结构。下列说法错误的是

 、
、 、苯胺等。其中
、苯胺等。其中 分子的结构示意图如图所示,每个N原子均满足最外层
分子的结构示意图如图所示,每个N原子均满足最外层 结构。下列说法错误的是
结构。下列说法错误的是
A. 难溶于水 难溶于水 |
B. 中 中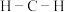 键角大于 键角大于 键角 键角 |
C. 中C、N的杂化方式相同 中C、N的杂化方式相同 |
D. 分子间以范德华力结合,故其热稳定性较差 分子间以范德华力结合,故其热稳定性较差 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、Q、E、M六种元素中,X的原子的基态价电子排布式为2s2,Y的基态原子核外有5种运动状态不同的电子,Z元素的两种同位素原子通常作为示踪原子研究生物化学反应和测定文物的年代,Q是元素周期表中电负性最大的元素,E的阳离子通常存在于硝石、明矾和草木灰中,M的原子序数比E大1。下列说法正确的是
| A.EYQ4中阴离子中心原子的杂化方式为sp3杂化 |
| B.X、Y元素的第一电离能大小关系:X<Y |
C.ZO 的空间构型为三角锥形 的空间构型为三角锥形 |
| D.MZ2含离子键和非极性共价键,阴阳离子之比为1∶2 |
您最近一年使用:0次



