在水的电离平衡中, 和
和 的关系如图所示:
的关系如图所示: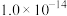 ,B点水的离子积为
,B点水的离子积为___________ 。造成水的离子积变化的原因是___________ 。
(2)下列说法正确的是___________ (填字母)。
a.图中A、B、D三点处 的大小关系:
的大小关系: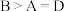
b.在 温度下,向水中加入少量的
温度下,向水中加入少量的 可实现由A点向D点移动
可实现由A点向D点移动
c.AB线上任意点的溶液均呈中性
d.图中温度
(3)①在 温度下,浓度为的
温度下,浓度为的 的
的 溶液中由水电离的
溶液中由水电离的
___________  。
。
②保持 温度不变,将
温度不变,将 的
的 溶液
溶液 与
与 的
的 溶液
溶液 混合后溶液
混合后溶液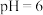 (忽略混合时溶液体积变化),则
(忽略混合时溶液体积变化),则
___________ 。
③曲线A所对应的温度下, 的
的 溶液和
溶液和 的某
的某 溶液中,若水的电离程度分别用
溶液中,若水的电离程度分别用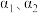 表示,则
表示,则
___________ (填“>”“=”或“<”) 。
。
 和
和 的关系如图所示:
的关系如图所示: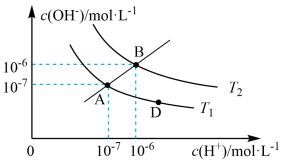
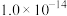 ,B点水的离子积为
,B点水的离子积为(2)下列说法正确的是
a.图中A、B、D三点处
 的大小关系:
的大小关系: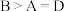
b.在
 温度下,向水中加入少量的
温度下,向水中加入少量的 可实现由A点向D点移动
可实现由A点向D点移动c.AB线上任意点的溶液均呈中性
d.图中温度

(3)①在
 温度下,浓度为的
温度下,浓度为的 的
的 溶液中由水电离的
溶液中由水电离的
 。
。②保持
 温度不变,将
温度不变,将 的
的 溶液
溶液 与
与 的
的 溶液
溶液 混合后溶液
混合后溶液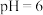 (忽略混合时溶液体积变化),则
(忽略混合时溶液体积变化),则
③曲线A所对应的温度下,
 的
的 溶液和
溶液和 的某
的某 溶液中,若水的电离程度分别用
溶液中,若水的电离程度分别用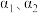 表示,则
表示,则
 。
。
更新时间:2023-10-11 21:41:37
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】根据化学平衡理论,请回答下列几个问题:
(1)某温度(t℃)时,水中c(H+)和c(OH-)的关系如图所示,a点水的离子积Kw=___________ 。该温度下,pH=12的NaOH溶液与pH=2的H2SO4溶液等体积混合,溶液显___________ (填“酸”或“碱”或“中”)性。

(2)向含有酚酞的0.1mol·L−1的氨水中加入少量NH4Cl固体,观察到的现象是___________ ,请结合离子方程式分析产生该现象的主要原因是:___________ 。
(3)将体积相等的NaOH稀溶液和CH3COOH溶液混合,若溶液呈中性,则溶液中c(Na+)______ c(CH3COO-)(填“>”“<”或“=”),则混合前c(NaOH)_______ c(CH3COOH)(填“>”“<”或“=”)。
(4)为配制SbCl3溶液,取少量SbCl3固体溶于2~3mL水中,观察到有白色沉淀生成,为避免出现该现象,配制SbCl3溶液的正确方法是___________ 。
(5)25℃时,已知Ksp[Cu(OH)2]=2×10−20,要使c(Cu2+)=0.2mol·L−1溶液中的Cu2+沉淀较完全[残留在溶液中的c(Cu2+)降低到2×10−4mol·L−1],则应加入NaOH溶液调节pH为___________ 。
(1)某温度(t℃)时,水中c(H+)和c(OH-)的关系如图所示,a点水的离子积Kw=

(2)向含有酚酞的0.1mol·L−1的氨水中加入少量NH4Cl固体,观察到的现象是
(3)将体积相等的NaOH稀溶液和CH3COOH溶液混合,若溶液呈中性,则溶液中c(Na+)
(4)为配制SbCl3溶液,取少量SbCl3固体溶于2~3mL水中,观察到有白色沉淀生成,为避免出现该现象,配制SbCl3溶液的正确方法是
(5)25℃时,已知Ksp[Cu(OH)2]=2×10−20,要使c(Cu2+)=0.2mol·L−1溶液中的Cu2+沉淀较完全[残留在溶液中的c(Cu2+)降低到2×10−4mol·L−1],则应加入NaOH溶液调节pH为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某温度(T℃)下的溶液中,c(H+)=10-x mol·L-1,c(OH-)= 10-y mol·L-1,x与y的关系如图所示,请回答下列问题:

(1)该温度T________ 25℃(填“>”、“<”或“=” ),
(2)若将此温度(T℃)下,pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(假设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两种溶液的体积比:
①若所得混合液为中性,则a∶b=____________ ;
②若所得混合液的pH=2,则a∶b=____________ 。

(1)该温度T
(2)若将此温度(T℃)下,pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(假设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两种溶液的体积比:
①若所得混合液为中性,则a∶b=
②若所得混合液的pH=2,则a∶b=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)①0.1 mol/L (NH4)2SO4溶液中各种离子的浓度由大到小顺序为__________ 。
②用离子方程式表示NaHCO3溶液显碱性的原因:______________ 。实验室中配制FeCl3溶液时常加入________ 溶液以抑制其水解。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=____________ mol/L,在pH=3的CH3COOH溶液中,水电离出的c(H+)=__________ mol/L。
(3)利用反应Cu + H2O2 + H2SO4 = CuSO4 + 2H2O设计一个原电池,回答下列问题:
①负极材料为____________ ;正极反应式为__________________________ 。
②反应过程中SO42-向_______ 极移动。
③当电路中转移0.1mol电子时,电解液质量(不含电极)增加了______ 克。
②用离子方程式表示NaHCO3溶液显碱性的原因:
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=
(3)利用反应Cu + H2O2 + H2SO4 = CuSO4 + 2H2O设计一个原电池,回答下列问题:
①负极材料为
②反应过程中SO42-向
③当电路中转移0.1mol电子时,电解液质量(不含电极)增加了
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】⑴常温下将0.2 mol/L HCl溶液与0.2 mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中由水电离出的c(H+)_______ 0.2 mol/L的HCl溶液中由水电离出的c(H+);(填“>”、“<”、或“=”)
②求出混合溶液中下列算式的精确计算结果(填具体数字):c(Cl-)-c(M+)=_____ mol/L;
c(H+)-c(MOH)=__________ mol/L
⑵常温下若将0.2 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下HA的电离程度______ NaA的水解程度。(填“>”、“<”、或“=”)
⑶已知:难溶电解质Cu(OH)2在常温下的Ksp = 2×10−20,则常温下:某CuSO4溶液中c(Cu2+) = 0.02 mol·L−1,如要生成Cu(OH)2沉淀,应调整溶液的pH最小为_________ 。
⑷已知:温度和浓度相等时,氨水的电离程度与醋酸相等。常温下,下列4种溶液:
①0.1mol/L CH3COONa ②0.1mol/L CH3COONH4 ③0.1mol/L CH3COOH
④0.1mol/LCH3COONa和0.1mol/LNaOH的混合溶液
按pH由大到小顺序排列___________ (填序号)
①混合溶液中由水电离出的c(H+)
②求出混合溶液中下列算式的精确计算结果(填具体数字):c(Cl-)-c(M+)=
c(H+)-c(MOH)=
⑵常温下若将0.2 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下HA的电离程度
⑶已知:难溶电解质Cu(OH)2在常温下的Ksp = 2×10−20,则常温下:某CuSO4溶液中c(Cu2+) = 0.02 mol·L−1,如要生成Cu(OH)2沉淀,应调整溶液的pH最小为
⑷已知:温度和浓度相等时,氨水的电离程度与醋酸相等。常温下,下列4种溶液:
①0.1mol/L CH3COONa ②0.1mol/L CH3COONH4 ③0.1mol/L CH3COOH
④0.1mol/LCH3COONa和0.1mol/LNaOH的混合溶液
按pH由大到小顺序排列
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】0.1mol/L的盐酸和0.06mol/L的Ba(OH)2溶液等体积混合,求混合溶液的pH___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】常温下,用0.1 mol·L-1的盐酸和25.00 mL 0.1 mol·L-1氨水混合。
(1)当加入10.00 mL稀盐酸时,溶液中的溶质是_______________________ (填化学式),溶液的pH________ (填“>”、“<”或“=”)7。
(2)当某一时刻溶液中c(NH4+)=c(Cl-),此时溶液的pH________ (填“>”、“<”或“=”)7。所加的盐酸体积V是不是等于25.00 mL?______ (填“是”或“不是”)。其原因是_______
(3)某一时刻溶液中会不会存在:c(Cl-)>c(NH4+),且c(OH-)>c(H+)的关系?________ (填“会”或“不会”)。其原因是_____________________________
(4)当盐酸过量时,下列离子浓度的大小关系是:c(Cl-)________ c(NH4+),c(OH-)___ c(H+)。(填“>”、“<”或“=”)
(1)当加入10.00 mL稀盐酸时,溶液中的溶质是
(2)当某一时刻溶液中c(NH4+)=c(Cl-),此时溶液的pH
(3)某一时刻溶液中会不会存在:c(Cl-)>c(NH4+),且c(OH-)>c(H+)的关系?
(4)当盐酸过量时,下列离子浓度的大小关系是:c(Cl-)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
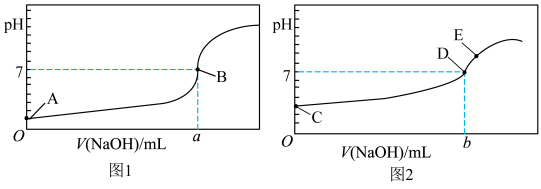
【推荐3】I. 常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:
(1)滴定盐酸的曲线是图__________ (填“1”或“2”)。
(2)滴定前CH3COOH的电离度为__________ (  )。
)。
(3)达到B、D状态时,反应消耗的NaOH溶液的体积a__________ b(填“>”“<”或“=”);若图中E点pH=8,则c(Na+)-c(CH3COO-)的精确值为__________ mol/L。
(4)若同pH同体积的下列溶液:①醋酸溶液;②盐酸溶液分别用氢氧化钠中和,所需氢氧化钠物质的量较大的是_______________ (填序号)。
Ⅱ.重金属离子会对河流和海洋造成严重污染。某化工厂废水(pH=2.0,ρ=1 g/mL)中含有
Ag+、Pb2+等重金属离子,其浓度约为0.01 mol/L,排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(1)你认为往废水中加入________ (填字母序号),沉淀效果最好。
A.NaOH B.Na2S C.KI D.Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8,处理后废水中c(Pb2+)=_____ 。
(3)如果用食盐处理只含Ag+的废水,测得处理后的废水(ρ=1 g/mL)中NaCl的质量分数为0.117%,若环境要求排放标准为c(Ag+)低于1×10−8mol/L,问该工厂处理后的废水中Ag+是否符合排放标准?_______ 已知Ksp(AgCl)=1.8×10−10。

(1)滴定盐酸的曲线是图
(2)滴定前CH3COOH的电离度为
 )。
)。(3)达到B、D状态时,反应消耗的NaOH溶液的体积a
(4)若同pH同体积的下列溶液:①醋酸溶液;②盐酸溶液分别用氢氧化钠中和,所需氢氧化钠物质的量较大的是
Ⅱ.重金属离子会对河流和海洋造成严重污染。某化工厂废水(pH=2.0,ρ=1 g/mL)中含有
Ag+、Pb2+等重金属离子,其浓度约为0.01 mol/L,排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S |
| Ksp | 8.3×10−12 | 5.6×10−8 | 6.3×10−50 |
| 难溶电解质 | PbI2 | Pb(OH)2 | PbS |
| Ksp | 7.1×10−9 | 1.2×10−15 | 3.4×10−28 |
(1)你认为往废水中加入
A.NaOH B.Na2S C.KI D.Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8,处理后废水中c(Pb2+)=
(3)如果用食盐处理只含Ag+的废水,测得处理后的废水(ρ=1 g/mL)中NaCl的质量分数为0.117%,若环境要求排放标准为c(Ag+)低于1×10−8mol/L,问该工厂处理后的废水中Ag+是否符合排放标准?
您最近一年使用:0次

 溶液的
溶液的 ,则溶液中由水电离出来的
,则溶液中由水电离出来的


