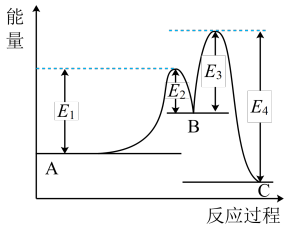
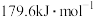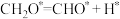某反应使用催化剂后,其反应过程中能量变化如图,下列说法正确的是
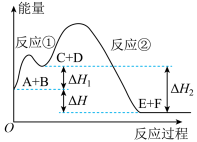

| A.使用催化剂可以加快反应速率的原因是提高了反应的活化能 |
| B.①是放热反应,反应②是吸热反应 |
| C.使用催化剂后,单位体积内的活化分子数目增加,活化分子百分数也增加 |
| D.△H=△H2-△H1 |
更新时间:2023-10-12 12:43:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某反应的ΔH=+100 kJ•mol-1,下列有关该反应的叙述正确的是( )
| A.正反应活化能小于100 kJ•mol-1 |
| B.逆反应活化能一定小于100 kJ•mol-1 |
| C.正反应活化能不小于100 kJ•mol-1 |
| D.正反应活化能比逆反应活化能小100 kJ•mol-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知化学反应A2(g)+B2(g)=2AB(s)的能量变化如图所示,下列叙述正确的是
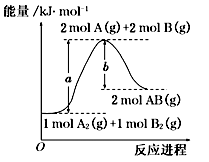

| A.该反应为放热反应 |
| B.A—B的键能为bkJ•mol-1 |
| C.加催化剂能降低该反应焓变 |
| D.该反应的反应热为△H=(a-b)kJ•mol-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一种以太阳能为热源分解水的历程,如图所示:
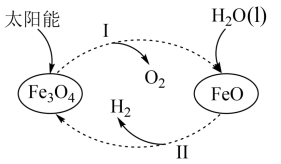
已知:2H2O(l)=2H2(g)+O2(g) △H=571.0 kJ·mol-1
过程I:2Fe3O4(s)=6FeO(s)+O2(g) △H=313.2 kJ·mol-1
下列说法错误的是

已知:2H2O(l)=2H2(g)+O2(g) △H=571.0 kJ·mol-1
过程I:2Fe3O4(s)=6FeO(s)+O2(g) △H=313.2 kJ·mol-1
下列说法错误的是
| A.过程I、II中能量转化的形式依次是:太阳能→化学能→热能 |
| B.转化过程中Fe3O4作催化剂 |
| C.破坏2 mol液态水中化学键所需能量高于形成2 mol氢气和1 mol氧气中化学键释放的能量 |
| D.过程II热化学方程式为3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) △H=128.9 kJ·mol-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各实验装置、目的或结论全都正确的是
| 实验装置 | 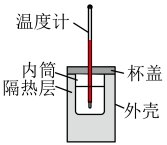 | 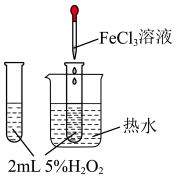 |  | 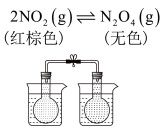 |
| 甲 | 乙 | 丙 | 丁 |
| A.甲用于测定中和反应的反应热 |
| B.乙可验证FeCl3对H2O2的分解反应有催化作用 |
| C.丙可验证镁片与稀盐酸反应放热 |
D.由丁可推断出:反应2NO2(g) N2O4(g)为吸热反应 N2O4(g)为吸热反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】NO2的储存和还原技术能有效降低柴油发动机在空气过量时排放的NO2,原理如图1所示。用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,如图2所示。
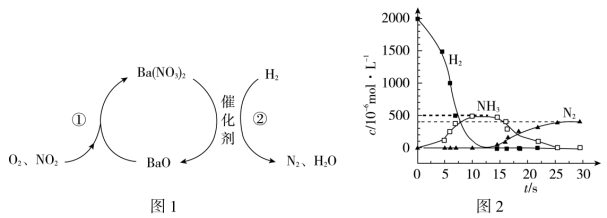
下列说法不正确的是

下列说法不正确的是
A.反应①为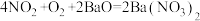 |
| B.储存和还原技术也能降低尾气排放的NO |
| C.0~12.5s内,氢气的消耗速率为v(H2)=1.6×10-4mol/(L·s) |
| D.反应②分两步进行,第二步Ba(NO3)2消耗的速率大于第一步的 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2SO2(g)+O2(g)⇌2SO3(g)反应过程中的能量变化如图。下列有关叙述不正确的是
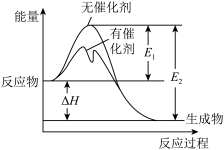

| A.该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数 |
| B.将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应放热akJ,其热化学方程式为2SO2(g)+O2(g)⇌2SO3(g) ΔH=-2a kJ·mol-l |
| C.该反应中,反应物的总键能小于生成物的总键能 |
| D.ΔH=-(E2-E1),使用催化剂改变活化能,但不改变反应热 |
您最近半年使用:0次

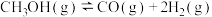 的五个路径与相对能量历程关系,如图所示,其中吸附在钯催化剂表面上的物种用*标注。
的五个路径与相对能量历程关系,如图所示,其中吸附在钯催化剂表面上的物种用*标注。