下列对有关实验现象的解释或所得结正确的是
| 实验操作 | 现象 | 解释或结论 | |
| A | 将少量铜粉加入稀硫酸中,无明显现象,再加入硝酸铁溶液 | 铜粉溶解 | Fe3+与铜粉反应 |
| B | 用蒸馏水溶解CuCl2固体,并继续加水稀释 | 溶液由绿色逐渐变为蓝色 | [CuCl4]2-+4H2O 4Cl-+[Cu(H2O)4]2+正向移动 4Cl-+[Cu(H2O)4]2+正向移动 |
| C | 将25℃0.1mol/L的Na2SO3溶液加热到40℃,用传感器监测溶液pH变化 | 溶液的pH逐渐减小 | 温度升高, 的水解程度增大 的水解程度增大 |
| D | 取2mL某卤代烃样品于试管中,加入5mL20%KOH溶液并加热,冷却到室温后滴加AgNO3溶液 | 产生白色沉淀 | 该卤代烃中含有氯元素 |
| A.A | B.B | C.C | D.D |
更新时间:2023-09-16 15:59:34
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】假设NA代表阿伏加德罗常数值。下列说法一定正确的是
| A.25℃,1 LpH=14的Ba(OH)2溶液含有OH-为NA个 |
| B.含1 mol AlCl3的溶液中离子总数目为4NA |
| C.32 g Cu与足量浓硝酸反应得到的气体分子总数为NA |
| D.标准状况下,每生成22.4 LO2转移电子数为4NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定体积的稀硝酸分成两等份,一份与足量的铜粉充分反应后收集到V1L(标准状况下,下同)气体;另一份先加入与其等体积的稀硫酸,再投入足量的铜粉收集到V2L气体。已知5V1=2V2,则稀硝酸与稀硫酸的物质的量浓度之比为
| A.2∶3 | B.3∶2 |
| C.3∶4 | D.4∶3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列各实验的方案设计、现象及结论都正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将少量Fe(NO3)2加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2不一定变质 |
| B | 镁、铝为电极,氢氧化钠为电解质的原电池装置 | 铝表面有气泡 | 金属活动性:Mg>Al |
| C | 向待测液中滴加浓氢氧化钠溶液并加热 | 产生使湿润蓝色石蕊试纸变红的气体 | 待测液中含有 |
| D | 将灼热的木炭加入到浓硝酸中 | 有红棕色气体产生 | 木炭在加热时能与浓硝酸发生反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列化学用语或图示不正确的是
A.邻羟基苯甲酫分子内氢键: |
B. 水解的离子方程式: 水解的离子方程式: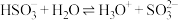 |
C. 分子中 分子中 键的形成: 键的形成: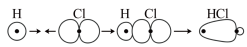 |
D. 的VSEPR模型: 的VSEPR模型: |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1L0.1mol·L-1NH4Cl溶液中, 的数量为0.1NA 的数量为0.1NA |
| B.2.0gH218O与D2O的混合物中所含中子数为NA |
| C.56gFe溶于过量硝酸,电子转移数为2NA |
| D.标准状况下,2.24LCCl4含有的共价键数为0.4NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】为了测定某卤代烃分子中所含有的卤原子种类,可按下列步骤进行实验: ①量取该卤代烃液体;②冷却后加入稀硝酸酸化;③加入AgNO3溶液至沉淀完全;④加入适量NaOH溶液,煮沸至液体不分层;正确操作顺序为
| A.④③②① | B.①④②③ | C.③①④② | D.①④③② |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关变化中发生反应的有机物均为1mol,下列说法正确的是( )
| A.一元醛与足量银氨溶液充分反应均可得到2mol Ag |
| B.一元卤代烃发生水解反应或消去反应时,均消耗1mol NaOH |
| C.不饱和烃CxH6与2molHBr完全加成后的产物最多可与8mol Cl2发生取代反应 |
| D.一元醇发生催化氧化时,可消耗1mol O2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】 下列物质的转化在给定条件下能实现的是
①Na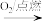 Na2O
Na2O NaOH
NaOH
②NH3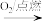 NO
NO NO2
NO2
③NaI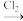 I2(aq)
I2(aq)  FeI3
FeI3
④Fe2O3 Fe2(SO4)3 (aq)
Fe2(SO4)3 (aq)  Fe2(SO4)3(s)
Fe2(SO4)3(s)
⑤AgNO3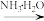 [Ag(NH3)2]OH
[Ag(NH3)2]OH 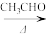 Ag(s)
Ag(s)
①Na
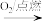 Na2O
Na2O NaOH
NaOH②NH3
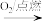 NO
NO NO2
NO2③NaI
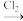 I2(aq)
I2(aq)  FeI3
FeI3④Fe2O3
 Fe2(SO4)3 (aq)
Fe2(SO4)3 (aq)  Fe2(SO4)3(s)
Fe2(SO4)3(s)⑤AgNO3
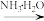 [Ag(NH3)2]OH
[Ag(NH3)2]OH 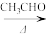 Ag(s)
Ag(s) | A.①③ | B.②⑤ | C.②④ | D.④⑤ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】配位化合物物广泛的应用于物质分离、定量测定.医药、催化等方面。利用氧化法可制备某些配位化合物。如2CoCl2+2NH4Cl+8NH3+H2O2=2[Co(NH3)5Cl]Cl2+2H2O
下列说法正确的是
下列说法正确的是
| A.该配位化合物的配位数为5 |
| B.提供孤电子对的成键原子是N和Cl |
| C.[Co(NH3)5Cl]2+中存在配位键、共价键和离子键 |
| D.氧化剂H2O2是非极性分子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】配位化学和超分子化学在生命科学领域有着广泛的应用,在生命体中扮演着举足轻重的角色。如下图甲表示血红蛋白中Fe(Ⅱ)结合氧气形成配合物的结构,图乙表示磷酸根与二脲基分子形成的超分子阴离子配合物。相关说法错误的是
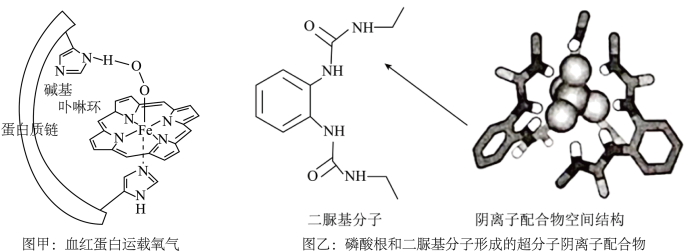
| A.图甲中,血红蛋白结合O2的作用力有两种,但强度不同,O2与Fe(Ⅱ)间作用力远强于与H间的作用力 |
| B.图乙中,磷酸根和二脲基分子间形成超分子的相互作用属于强度较弱的化学键 |
| C.亚硝酸钠是一种氧化剂,误服中毒会出现面色发青、口唇紫绀等典型缺氧症状,推测中毒机理是其将血红蛋白中Fe(Ⅱ)氧化,使其无法再与O2配位而丧失输氧能力 |
| D.CO中毒的原因:因电负性C<O,故C相比O更易给出电子对与血红蛋白中Fe(Ⅱ)成配位键,当CO存在时,血红蛋白优先与CO结合而丧失输氧能力 |
您最近半年使用:0次

 X
X Y
Y 乙二醇
乙二醇

