下图是FeCl3溶液与KSCN溶液反应的实验示意图,下列分析不正确的是


A.溶液中存在平衡: |
| B.加入KSCN溶液后,Q>K,平衡向正反应方向移动 |
C.溶液中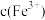 减小 减小 |
| D.若加入少量KOH溶液,则会产生红褐色沉淀 |
更新时间:2023-10-17 19:19:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】若反应:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法不正确的是
N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法不正确的是
 N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法不正确的是
N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法不正确的是| A.及时分离出 CO2,使 Q 减小,Q<K,因此平衡正向移动 |
| B.及时分离出 N2,使 Q 减小,Q<K,因此平衡正向移动 |
| C.降低温度,使 Q 减小,Q<K,因此平衡正向移动 |
| D.加入催化剂可增大反应速率,从而增大一段时间内的反应物转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】温度、压强分别超过临界温度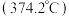 、临界压强
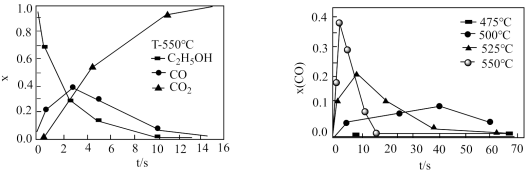
、临界压强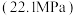 时的水称为超临界水。超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定条件下,乙醇的超临界水氧化结果如图所示,其中
时的水称为超临界水。超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定条件下,乙醇的超临界水氧化结果如图所示,其中 为以碳元素计的物质的量分数,t为反应时间。
为以碳元素计的物质的量分数,t为反应时间。
下列说法错误的是
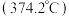 、临界压强
、临界压强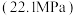 时的水称为超临界水。超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定条件下,乙醇的超临界水氧化结果如图所示,其中
时的水称为超临界水。超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定条件下,乙醇的超临界水氧化结果如图所示,其中 为以碳元素计的物质的量分数,t为反应时间。
为以碳元素计的物质的量分数,t为反应时间。
下列说法错误的是
| A.乙醇的超临界水氧化过程中,一氧化碳是中间产物,二氧化碳是最终产物 |
| B.在550℃条件,反应时间小于2s时,乙醇的氧化速率大于一氧化碳的氧化速率 |
| C.在550℃条件,反应时间大于11s时,乙醇的氧化已趋于完全 |
D.随温度升高,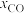 峰值出现时间提前,且峰值更高,说明乙醇的氧化是吸热反应 峰值出现时间提前,且峰值更高,说明乙醇的氧化是吸热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向2L容密闭容器中投入一定量的CO和 ,发生如下反应:
,发生如下反应:
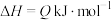 ,CO的平衡转化率与温度、投料比
,CO的平衡转化率与温度、投料比 [
[ ]的关系如下图所示。
]的关系如下图所示。
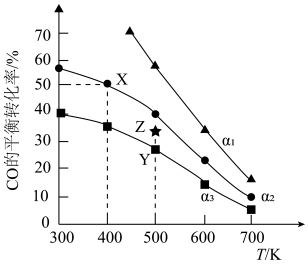
下列说法正确的是
 ,发生如下反应:
,发生如下反应:
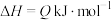 ,CO的平衡转化率与温度、投料比
,CO的平衡转化率与温度、投料比 [
[ ]的关系如下图所示。
]的关系如下图所示。
下列说法正确的是
A.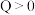 |
B.投料比: |
C.在400K、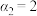 条件下,反应的平衡常数的值为0.25 条件下,反应的平衡常数的值为0.25 |
D.在500K、 条件下,增大压强,CO的平衡转化率能从Y点到Z点 条件下,增大压强,CO的平衡转化率能从Y点到Z点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知反应原理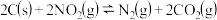 ,在密闭容器中1mol
,在密闭容器中1mol  和足量C发生反应,相同时间内测得
和足量C发生反应,相同时间内测得 的生成速率与
的生成速率与 的生成速率随温度变化的关系如图1;维持温度不变,反应相同时间内测得
的生成速率随温度变化的关系如图1;维持温度不变,反应相同时间内测得 的转化率随压强的变化如图2。
的转化率随压强的变化如图2。
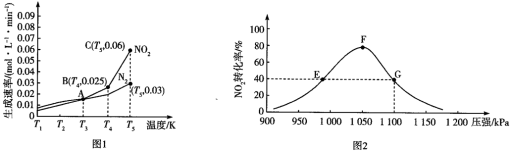
下列说法错误的是
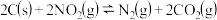 ,在密闭容器中1mol
,在密闭容器中1mol  和足量C发生反应,相同时间内测得
和足量C发生反应,相同时间内测得 的生成速率与
的生成速率与 的生成速率随温度变化的关系如图1;维持温度不变,反应相同时间内测得
的生成速率随温度变化的关系如图1;维持温度不变,反应相同时间内测得 的转化率随压强的变化如图2。
的转化率随压强的变化如图2。
下列说法错误的是
| A.图1中的A、B、C三个点中只有C点是平衡点 |
| B.图2中平衡常数K(F)=K(G) |
C.图2中E点的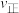 小于F点的 小于F点的 |
D.图2中 的浓度 的浓度 |
您最近一年使用:0次
【推荐3】一定温度下,在三个恒容体积均为2.0L的容器中发生反应:PCl5(g) PCl3(g)+Cl2(g),下列说法不正确的个数有
PCl3(g)+Cl2(g),下列说法不正确的个数有
①平衡常数K:容器Ⅱ>容器Ⅲ
②反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
③反应从开始到平衡时,容器I中的平均速率为v(PCl5)=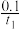 mol·L-1·s-1
mol·L-1·s-1
④起始时向容器Ⅲ中充入PCl50.30mol、PCl30.45mol和Cl20.10mol,则反应正向进行
 PCl3(g)+Cl2(g),下列说法不正确的个数有
PCl3(g)+Cl2(g),下列说法不正确的个数有| 编号 | 温度(℃) | 起始/mol | 平衡/mol | 达到平衡所需时间/s | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
| Ⅱ | 320 | 0.80 | t2 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
②反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
③反应从开始到平衡时,容器I中的平均速率为v(PCl5)=
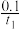 mol·L-1·s-1
mol·L-1·s-1④起始时向容器Ⅲ中充入PCl50.30mol、PCl30.45mol和Cl20.10mol,则反应正向进行
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次


 ,下列说法正确的是
,下列说法正确的是 的浓度将升高
的浓度将升高

