工厂烟气(主要污染物 SO2、NO)直接排放会造成空气污染,需处理后才能排放。
(1)O3 氧化:O3 氧化过程中部分反应的能量变化如图所示, Ea1 是反应的活化能,一定条件下,活化能越大反应速 率越慢,反应越困难。

①写出 NO 与 O3 反应的热化学方程式:___________ 。
②在相同条件下,O3 与 SO2 反应的速率___________ O3 与 NO 的反应速率。(填“>”“<”或“=”)
③其他条件不变时,工厂烟气处理主要发生 NO 与 O3 反应,即使增加 n(O3),O3 氧化 SO2 的反应几乎不受影响, 可能原因是___________ 。
(2)NaClO2 氧化:40 ℃时向一定量 NaClO2 溶液中按一定流速持续通入工厂烟气,溶液的 pH 与 ORP 值(氧化还原 电位)随时间变化如图所示。

①写出溶液中 NO 与 反应生成
反应生成 和 Cl-的离子方程式:
和 Cl-的离子方程式:___________ 。
②烟气中含有少量 SO2,NO 的脱除率比不含 SO2 的烟气高,可能原因是___________ 。
(1)O3 氧化:O3 氧化过程中部分反应的能量变化如图所示, Ea1 是反应的活化能,一定条件下,活化能越大反应速 率越慢,反应越困难。

①写出 NO 与 O3 反应的热化学方程式:
②在相同条件下,O3 与 SO2 反应的速率
③其他条件不变时,工厂烟气处理主要发生 NO 与 O3 反应,即使增加 n(O3),O3 氧化 SO2 的反应几乎不受影响, 可能原因是
(2)NaClO2 氧化:40 ℃时向一定量 NaClO2 溶液中按一定流速持续通入工厂烟气,溶液的 pH 与 ORP 值(氧化还原 电位)随时间变化如图所示。

①写出溶液中 NO 与
 反应生成
反应生成 和 Cl-的离子方程式:
和 Cl-的离子方程式:②烟气中含有少量 SO2,NO 的脱除率比不含 SO2 的烟气高,可能原因是
更新时间:2023-11-02 15:38:15
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】氧缺位体( )是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是(
)是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是( ,含
,含 、
、 等杂质)、为原料制备
等杂质)、为原料制备 的流程如下:
的流程如下: 、
、 、
、 和
和
②25℃时已知几种金属离子沉淀的pH如表所示:
请回答下列问题:
(1)加Cu“还原”的目是___________ 。
 )是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是(
)是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是( ,含
,含 、
、 等杂质)、为原料制备
等杂质)、为原料制备 的流程如下:
的流程如下: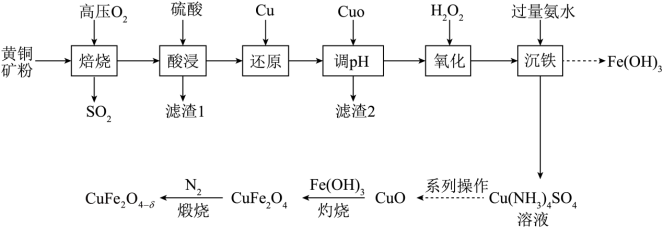
 、
、 、
、 和
和
②25℃时已知几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |
| 开始沉淀的pH | 1.9 | 3.4 | 6.4 | 7.0 |
| 完全沉淀的pH | 3.2 | 4.7 | 7.6 | 9.0 |
(1)加Cu“还原”的目是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】(1)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
NaBiO3 + MnSO4 + H2SO4===Na2SO4 + Bi2(SO4)3 + NaMnO4 + H2O
①上述反应中还原产物是____________ ,若有2mol氧化剂在该反应中被还原,则生成的MnO4-被还原为Mn2+时,能将____________ molHCl氧化成Cl2;
②写出NaBiO3固体溶于浓盐酸产生黄绿色气体的化学反应方程式______________ 。
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(S)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=64.39kJ·mol-1
2H2O2(L)===2H2O(L)+O2(g) ΔH=-196.46kJ·mol-1
H2(g)+ O2(g)===H2O(L) ΔH=-285.84kJ·mol-1
O2(g)===H2O(L) ΔH=-285.84kJ·mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为______________ 。
NaBiO3 + MnSO4 + H2SO4===Na2SO4 + Bi2(SO4)3 + NaMnO4 + H2O
①上述反应中还原产物是
②写出NaBiO3固体溶于浓盐酸产生黄绿色气体的化学反应方程式
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(S)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=64.39kJ·mol-1
2H2O2(L)===2H2O(L)+O2(g) ΔH=-196.46kJ·mol-1
H2(g)+
 O2(g)===H2O(L) ΔH=-285.84kJ·mol-1
O2(g)===H2O(L) ΔH=-285.84kJ·mol-1在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而引发中毒的事故。
(1)两种日化产品的主要成分中都含有氯元素,该元素在元素周期表中的位置是_______________ 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:________________________ 。
(3)洁厕液的主要成分是盐酸.下列关于卤化氢性质的比较中,错误的是________ 。
A.酸性:
B.稳定性:
C.熔点:
D.还原性:
(4)常温下,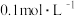 的NaClO溶液的
的NaClO溶液的 ,原因是
,原因是________________________________ (用方程式解释).常温下HClO的电离平衡常数为________ 。洁厕液与84消毒液混合后会生成有毒的氯气,写出该反应的离子方程式:____________________________ 。
(5)高铁酸钾(K2FeO4)是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产:
①在碱性条件下,利用NaClO氧化硝酸铁,制得K2FeO4,该反应的离子方程式为___________ 。
②K2FeO4与KOH反应生成 。K2FeO4在水溶液中易水解:
。K2FeO4在水溶液中易水解: ,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用________ 溶液(填序号)。
A.水
B.NH4Cl、2-甲基-2-丙醇
C.Fe(NO3)3、2-甲基-2-丙醇
D.CH3COONa、2-甲基-2-丙醇
(6)消毒效率是单位质量物质得到的电子数,则 与NaClO两种消毒剂的消毒效率之比为
与NaClO两种消毒剂的消毒效率之比为________ 。
(1)两种日化产品的主要成分中都含有氯元素,该元素在元素周期表中的位置是
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:
(3)洁厕液的主要成分是盐酸.下列关于卤化氢性质的比较中,错误的是
A.酸性:

B.稳定性:

C.熔点:

D.还原性:

(4)常温下,
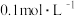 的NaClO溶液的
的NaClO溶液的 ,原因是
,原因是(5)高铁酸钾(K2FeO4)是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产:
①在碱性条件下,利用NaClO氧化硝酸铁,制得K2FeO4,该反应的离子方程式为
②K2FeO4与KOH反应生成
 。K2FeO4在水溶液中易水解:
。K2FeO4在水溶液中易水解: ,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用A.水
B.NH4Cl、2-甲基-2-丙醇
C.Fe(NO3)3、2-甲基-2-丙醇
D.CH3COONa、2-甲基-2-丙醇
(6)消毒效率是单位质量物质得到的电子数,则
 与NaClO两种消毒剂的消毒效率之比为
与NaClO两种消毒剂的消毒效率之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】(1)①一定温度下,在密闭容器中充入 1molN2和 3molH2 发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0 。若容器容积恒定,达到平衡状态时,气体的 总物质的量是原来的 7/10,则 N2的转化率 a1=
2NH3(g) ΔH<0 。若容器容积恒定,达到平衡状态时,气体的 总物质的量是原来的 7/10,则 N2的转化率 a1=_____ ;
②若向该容器中再加入 1molN2和 3molH2,达到平衡状态时,N2的转化率为 a2,则a2_____ a1(填“>”、“<”或“=”)。
(2)对于反应 2NO(g)+O2(g) 2NO2(g)。在其他条件相同时,分别测得 NO 的平衡转化 率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得 NO 的平衡转化 率在不同压强(P1、P2)下温度变化的曲线(如图)。
_____ P2(填“>”、“<”或“=”)。
②该反应的平衡常数 K 的表达式为_____ ,随温度升高,该反应平衡常 数变化的趋势是_____ 。(填“增大”、“减小”或“不变”)。
③下列措施中能够同时满足增大反应速率和提高 NO 转化率的是_____ 。(填写相应字母)
A.使用高效催化剂 B.保持容器体积不变加入惰性气体 C.保持容器体积不变加入 O2 D.降低温度E. 压缩容器体积
(3)硝酸厂常用催化还原法处理尾气:催化剂存在时用 H 2 将 NO2还原为 N2。
已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483kJ/mol
N2(g)+2O2(g)=2NO2(g) ΔH=+67kJ/mol
则 H2还原 NO2生成 N2的热化学方程式是_____
 2NH3(g) ΔH<0 。若容器容积恒定,达到平衡状态时,气体的 总物质的量是原来的 7/10,则 N2的转化率 a1=
2NH3(g) ΔH<0 。若容器容积恒定,达到平衡状态时,气体的 总物质的量是原来的 7/10,则 N2的转化率 a1=②若向该容器中再加入 1molN2和 3molH2,达到平衡状态时,N2的转化率为 a2,则a2
(2)对于反应 2NO(g)+O2(g)
 2NO2(g)。在其他条件相同时,分别测得 NO 的平衡转化 率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得 NO 的平衡转化 率在不同压强(P1、P2)下温度变化的曲线(如图)。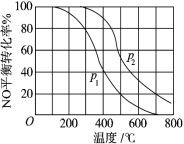
②该反应的平衡常数 K 的表达式为
③下列措施中能够同时满足增大反应速率和提高 NO 转化率的是
A.使用高效催化剂 B.保持容器体积不变加入惰性气体 C.保持容器体积不变加入 O2 D.降低温度E. 压缩容器体积
(3)硝酸厂常用催化还原法处理尾气:催化剂存在时用 H 2 将 NO2还原为 N2。
已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483kJ/mol
N2(g)+2O2(g)=2NO2(g) ΔH=+67kJ/mol
则 H2还原 NO2生成 N2的热化学方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】碳和氧元素及其化合物与人类的生产、生活密切相关。
I.氯的化合物合成、转化一直是科学研究的热点。
(1)一定条件下,氯气与氨气反应可以制备气态氯胺(NH2Cl),已知部分化学键的键能:
则上述反应的热化学方程式为:__________________ 。
(2)氯胺是一种长效缓释含氯消毒剂,有缓慢而持久的杀菌作用,可以杀死H7N9禽流感病毒,其消毒原理为与水缓慢反应生成强氧化性的物质,该反应的化学方程式为_____________ 。
II.碳的化合物的转换在生产、生活中具有重要的应用。特别是CO2的低碳转型对抵御气候变化具有重要意义。
(3)在三个容积均为1L的密闭容器中以不同的氢碳比 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。
C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。
请回答下列问题:
①反应的△H______ 0,氢碳比α____ β,Q点v(正)_____ v(逆)(填“>”或“<”、“=”)
②若起始时,CO2的浓度分别为0.5mol/L,则P点对应温度度的平衡常数的值为________ 。
(4)已知:碳酸 H2CO3: K1=4.3×10-7、K2=5.6×10-11;
草酸 H2C2O4: K1=6.0×10-2、K2=6.0×10-5
①下列微粒可以大量共存的是_______ (填字母)。
a.CO32-、HC2O4-b.H2CO3、C2O42-c. C2O42-、HCO3-d.H2C2O4、HCO3-
②若将等物质的量浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子(除OH-外)浓度由大到小的顺序是_________ 。
I.氯的化合物合成、转化一直是科学研究的热点。
(1)一定条件下,氯气与氨气反应可以制备气态氯胺(NH2Cl),已知部分化学键的键能:
| 化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
| 键能/KJ•mol-1 | 391.3 | 243.0 | 191.2 | 431.8 |
则上述反应的热化学方程式为:
(2)氯胺是一种长效缓释含氯消毒剂,有缓慢而持久的杀菌作用,可以杀死H7N9禽流感病毒,其消毒原理为与水缓慢反应生成强氧化性的物质,该反应的化学方程式为
II.碳的化合物的转换在生产、生活中具有重要的应用。特别是CO2的低碳转型对抵御气候变化具有重要意义。
(3)在三个容积均为1L的密闭容器中以不同的氢碳比
 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。
C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示。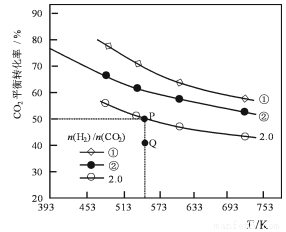
请回答下列问题:
①反应的△H
②若起始时,CO2的浓度分别为0.5mol/L,则P点对应温度度的平衡常数的值为
(4)已知:碳酸 H2CO3: K1=4.3×10-7、K2=5.6×10-11;
草酸 H2C2O4: K1=6.0×10-2、K2=6.0×10-5
①下列微粒可以大量共存的是
a.CO32-、HC2O4-b.H2CO3、C2O42-c. C2O42-、HCO3-d.H2C2O4、HCO3-
②若将等物质的量浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子(除OH-外)浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】肼(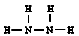 )可作为火箭发动机的燃料,NH3与NaClO反应可得到肼。
)可作为火箭发动机的燃料,NH3与NaClO反应可得到肼。
(1)实验室用氯化铵和氢氧化钙制备氨气的化学方程式:__________________
(2)已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-195kJ·mol-1
②N2H4(l) +O2(g)= N2(g) +2H2O(g) ΔH2=-534kJ·mol-1
写出液态肼和N2O4(l)反应生成N2和水蒸气的热化学方程式:______________________
(3)已知断裂1 mol化学键所需的能量(kJ)如下:N≡N为942、O=O为498、N-N为154、H-O 为464、请根据N2H4(l) +O2(g)= N2(g) +2H2O(g) ΔH2=-534kJ·mol-1中数据计算断裂1 molN-H键所需的能量(kJ)是:__________________
(4)写出NH3与NaClO反应得到肼的化学方程式:___________________________
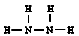 )可作为火箭发动机的燃料,NH3与NaClO反应可得到肼。
)可作为火箭发动机的燃料,NH3与NaClO反应可得到肼。(1)实验室用氯化铵和氢氧化钙制备氨气的化学方程式:
(2)已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-195kJ·mol-1
②N2H4(l) +O2(g)= N2(g) +2H2O(g) ΔH2=-534kJ·mol-1
写出液态肼和N2O4(l)反应生成N2和水蒸气的热化学方程式:
(3)已知断裂1 mol化学键所需的能量(kJ)如下:N≡N为942、O=O为498、N-N为154、H-O 为464、请根据N2H4(l) +O2(g)= N2(g) +2H2O(g) ΔH2=-534kJ·mol-1中数据计算断裂1 molN-H键所需的能量(kJ)是:
(4)写出NH3与NaClO反应得到肼的化学方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】Ⅰ.对于可逆反应:2SO2(g)+O2(g) ⇌2SO3(g),在容积固定的密闭容器中充入等物质的量的SO2、O2,①单位时间内消耗2n mol SO2的同时生成2n mol SO3;②单位时间内消耗2n mol SO2的同时生成2n mol SO2;③用SO2、O2、SO3表示的反应速率之比为2:1:2的状态;④SO2的质量分数不再改变;⑤c(SO2): c(O2): c(SO3)=2:1:2;⑥c(SO2) : c(SO3)的比值不再改变;⑦c(SO2): c(O2)的比值不再改变;⑧混合气体的压强不再改变;⑨混合气体的密度不再改变;⑩混合气体的平均相对分子质量不再改变
(1)以上达到平衡状态的标志是___________________________
(2)若在恒温恒压条件下,以上可判断达到化学平衡状态的是______________________
II.在一密闭容器中发生反应:H2(g)+I2(g) ⇌2HI(g) △H<0,已达平衡:
①保持容器容积不变,充入1mlH2;②保持容器容积不变,充入1mlHe;③保持容器内气体压强不变,充入1mlHe;④升高温度;⑤加入正催化剂
(1)改变条件,反应速率加快的是__________ ,其中活化分子百分数增大的是________ 。
(2)改变条件,平衡正向移动的是______________ 。
(1)以上达到平衡状态的标志是
(2)若在恒温恒压条件下,以上可判断达到化学平衡状态的是
II.在一密闭容器中发生反应:H2(g)+I2(g) ⇌2HI(g) △H<0,已达平衡:
①保持容器容积不变,充入1mlH2;②保持容器容积不变,充入1mlHe;③保持容器内气体压强不变,充入1mlHe;④升高温度;⑤加入正催化剂
(1)改变条件,反应速率加快的是
(2)改变条件,平衡正向移动的是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】国家主席习近平在9月22日召开的联合国大会上表示:“中国将争取在2060年前实现碳中和”。所谓“碳中和”,通俗地说,日常活动可能制造的二氧化碳排放量,通过植树、节能减排等方法来中和抵消。
(1)CO2甲烷化反应是由法国化学家PaulSabatier提出的,因此,该反应又叫Sabatier反应。CO2催化氢化制甲烷的研究过程如图1:

①上述过程中,加入铁粉的作用是_______________ 。
②HCOOH是CO2转化为CH4的中间体:
CO2 HCOOH
HCOOH CH4。
CH4。
当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是_________________ 。
(2)一定条件下,Pd-Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为_________ ,反应过程中碳元素的化合价为-2价的中间体是_______ 。

(3)我国科学家研究Li—CO2电池,取得了重大科研成果。回答下列问题:
①在Li—CO2电池中,Li为单质锂片,则该电池中的CO2在_________ (填“正”或“负”)极发生电化学反应。
②研究表明,在电解质水溶液中,CO2气体可被电化学还原。
Ⅰ.CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为_________ 。
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上CO2电还原为CO的反应进程中(H+被还原为H2的反应可同时发生),相对能量变化如下图所示。由此判断,CO2电还原为CO从易到难的顺序为:________ (用 a、b、c字母排序)。

(1)CO2甲烷化反应是由法国化学家PaulSabatier提出的,因此,该反应又叫Sabatier反应。CO2催化氢化制甲烷的研究过程如图1:

①上述过程中,加入铁粉的作用是
②HCOOH是CO2转化为CH4的中间体:
CO2
 HCOOH
HCOOH CH4。
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是
(2)一定条件下,Pd-Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为

(3)我国科学家研究Li—CO2电池,取得了重大科研成果。回答下列问题:
①在Li—CO2电池中,Li为单质锂片,则该电池中的CO2在
②研究表明,在电解质水溶液中,CO2气体可被电化学还原。
Ⅰ.CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上CO2电还原为CO的反应进程中(H+被还原为H2的反应可同时发生),相对能量变化如下图所示。由此判断,CO2电还原为CO从易到难的顺序为:

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】浙江大学某国家实验室用水热法还原CO2转化为HCOOH,探究了不同条件下CO2的转化率,数据如下图所示:
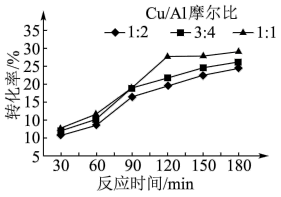
(1)依据以上数据,最佳的 摩尔比和反应时间是
摩尔比和反应时间是_____ 、_____ 。
中国科学院大学以Bi为电极材料,利用电化学催化还原法制备HCOOH。用计算机模拟CO2在电极材料表面发生还原反应的历程如下(*表示微粒与Bi的接触位点):
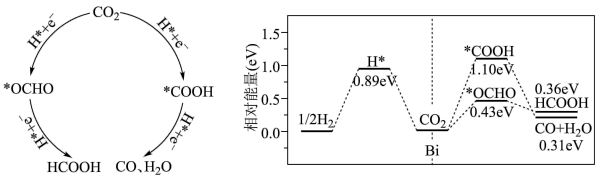
(2)HCOOH是_____(填字母)产物。
(3)依据反应历程图中数据,你认为电催化还原CO2生成HCOOH的选择性_____ (填“高于”或“低于”)生成CO的选择性,原因是_____ 。

(1)依据以上数据,最佳的
 摩尔比和反应时间是
摩尔比和反应时间是中国科学院大学以Bi为电极材料,利用电化学催化还原法制备HCOOH。用计算机模拟CO2在电极材料表面发生还原反应的历程如下(*表示微粒与Bi的接触位点):

(2)HCOOH是_____(填字母)产物。
| A.阴极 | B.阳极 | C.负极 | D.正极 |
(3)依据反应历程图中数据,你认为电催化还原CO2生成HCOOH的选择性
您最近一年使用:0次



