18. 碳及其化合物的价值型转化在工业生产方面具有重要的研究价值。利用太阳能等可再生能源,通过光 催化、光电催化或电解水制氢来进行二氧化碳加氢制甲醇,发生的主要反应是:CO2(g)+3H2(g)  CH3OH(g) + H2O(g)请回答下列有关问题:
CH3OH(g) + H2O(g)请回答下列有关问题:
(1)若二氧化碳加氢制甲醇反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明 该反应进行到t
1时刻达到平衡状态的是
___________(填标号)。
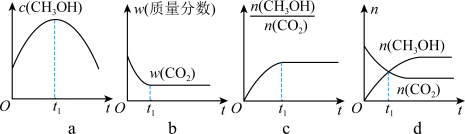
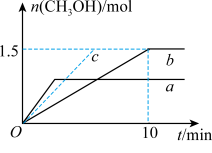
(2)在2L恒容密闭容器 a和b中分别投入2molCO
2 和6molH
2,在不同温度下进行二氧化碳加氢制甲醇的反应,各容器 中甲醇的物质的量与时间的关系如图 所示。若容器a、容器b中的反应温度分别为T
1、T
2,则判断T
1___________T
2(填“>”“<”或“=”)。若容器b中改变条件时,反应情况会由曲线b变为曲线c,则改变的条件是
___________。
(3)工业上也可利用 CO 来生产燃料甲醇。已知用 CO 和 CO
2制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度/℃ |
500 | 800 |
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.15 |
②H2(g)+ CO2(g)  H2O(g)+CO(g) H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g)  CH3OH(g)+H2O(g) CH3OH(g)+H2O(g) | K3 | | |
①据反应①与②可推导出K1、K2与K3之间的关系,则K3=___________(用K1、K2表示)。
②500℃时测得反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为 0.8、0.1、0.3、0.15,则 此时v正___________v逆(填“>”“<”或“=”)。
(4)已知 CO 分子中化学键为 C≡O。相关的化学键键能数据如下:
化学键 | H—O | C≡O | C=O | H—H |
E/(kJ·mol−1) | 463 | 1075 | 803 | 436 |
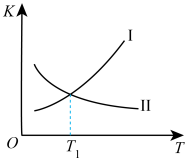
①CO2(g)+H2(g)  CO(g)+H2O(g) ΔH =___________。该反应正反应的平衡常数 K 正和逆反应的平衡常数 K 逆随温度变化曲线如图。表示 K 正曲线的是___________(填“Ⅰ”或“Ⅱ”)。
CO(g)+H2O(g) ΔH =___________。该反应正反应的平衡常数 K 正和逆反应的平衡常数 K 逆随温度变化曲线如图。表示 K 正曲线的是___________(填“Ⅰ”或“Ⅱ”)。
②T1时,向体积为 10 L 的固定容积的容器中充入 2 mol CO2、2 mol H2,CO2的 平衡转化率为___________。