I.测定50mL0.50mol/L稀盐酸和50mL0.55mol/LNaOH溶液反应的反应热的实验装置如图所示:
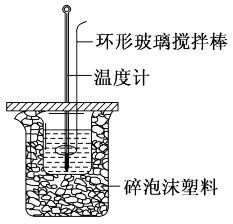
(1)烧杯间填满碎泡沫塑料的作用是___________ 。
(2)NaOH溶液稍过量的原因___________ 。
Ⅱ.某探究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究外界条件对化学反应速率的影响,实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢,该小组设计了如下方案:
(3)通过实验A、B可探究___________ (填外界条件)的改变对反应速率的影响,其中V1=___________ ;T1=___________ 。
(4)若t1<8,则由此实验可以得出的结论是___________ 。

(1)烧杯间填满碎泡沫塑料的作用是
(2)NaOH溶液稍过量的原因
Ⅱ.某探究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究外界条件对化学反应速率的影响,实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢,该小组设计了如下方案:
| 实验序号 | 实验温度/K | KMnO4溶液 | H2C2O4溶液 | H2O | 溶液颜色褪至无色时所需时间/s | ||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 5 | 0.1 | 5 | t1 |
| B | T1 | 2 | 0.02 | 4 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 6 | t2 |
(4)若t1<8,则由此实验可以得出的结论是
更新时间:2023-09-23 21:09:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】分别取40 mL的0.50 mol·L-1盐酸与40 mL的0.55 mol·L-1NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题:
(1)理论上稀强酸、稀强碱反应生成1 mol 水时放出57.3 kJ的热量,写出表示稀硫酸和稀NaOH溶液反应的中和热的热化学方程式_______________________________ 。
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是______________ 。

(3)假设盐酸和NaOH溶液的密度都是1 g·cm-3,又知中和后生成溶液的比热容c=4.18 J·g-1·℃-1,为了计算中和热,实验时还需测量的数据有(填字母)______________
A.反应前盐酸溶液的温度 B.反应前盐酸溶液的质量
C.反应前NaOH溶液的温度 D.反应前NaOH溶液的质量
E.反应后混合溶液的最高温度 F.反应后混合溶液的质量
(1)理论上稀强酸、稀强碱反应生成1 mol 水时放出57.3 kJ的热量,写出表示稀硫酸和稀NaOH溶液反应的中和热的热化学方程式
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是

(3)假设盐酸和NaOH溶液的密度都是1 g·cm-3,又知中和后生成溶液的比热容c=4.18 J·g-1·℃-1,为了计算中和热,实验时还需测量的数据有(填字母)
A.反应前盐酸溶液的温度 B.反应前盐酸溶液的质量
C.反应前NaOH溶液的温度 D.反应前NaOH溶液的质量
E.反应后混合溶液的最高温度 F.反应后混合溶液的质量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是________ 。
(2)烧杯间填满碎纸条的作用是________ 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值____________ (填“偏大”、“偏小”或“无影响”)。
(4)该实验常用0.50 mol·L-1 HCl和0.55 mol·L-1 NaOH溶液各50 mL进行实验,其中NaOH溶液浓度大于盐酸浓度的作用是______ ,当室温低于10 ℃时进行实验,对实验结果会造成较大的误差,其原因是_____________ 。
(5)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求得的中和热________ (填“相等”或“不相等”),简述理由: ______________ 。
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热ΔH将________ (填“偏大”、“偏小”或“无影响”)。

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)烧杯间填满碎纸条的作用是
(3)大烧杯上如不盖硬纸板,求得的中和热数值
(4)该实验常用0.50 mol·L-1 HCl和0.55 mol·L-1 NaOH溶液各50 mL进行实验,其中NaOH溶液浓度大于盐酸浓度的作用是
(5)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求得的中和热
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热ΔH将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组利用如图装置进行中和反应反应热的测定实验。
①量取50 mL 0.25 mol/L H2SO4溶液,倒入小烧杯中,测量温度;
②量取50 mL 0.55 mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,测量混合液的最高温度。
Ⅱ.实验数据如下:
请回答下列问题:
(1)仪器甲的名称为___________ ,进行该实验还缺少的仪器为___________ (填仪器名称)。
(2)设实验所用的酸、碱溶液的密度均为1 g/cm ,且酸、碱中和后的溶液的比热容
,且酸、碱中和后的溶液的比热容 J⋅g
J⋅g ⋅C
⋅C 。计算该实验中生成1 mol水时的反应热△H=
。计算该实验中生成1 mol水时的反应热△H=___________ (保留一位小数)
(3)若改用60 mL 0.50 mol/L盐酸与60 mL 0.55 mol/LNaOH溶液进行反应,与(1)中实验相比,所放出的热量___________ (填写“相等”或“不相等”);若用50 mL 0.50 mol/LCH3COOH溶液代替盐酸进行(1)中实验,测得反应生成1 mol水时的反应热
___________ (填写“偏大”、“偏小”或“不变”)。

①量取50 mL 0.25 mol/L H2SO4溶液,倒入小烧杯中,测量温度;
②量取50 mL 0.55 mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,测量混合液的最高温度。
Ⅱ.实验数据如下:
| 实验序号 | 起始温度T1/℃ | 终止温度T2/℃ | ||
| H2SO4溶液 | NaOH溶液 | 平均值 | ||
| 1 | 25.0 | 25.2 | 28.5 | |
| 2 | 24.9 | 25.1 | 28.2 | |
| 3 | 25.5 | 26.5 | 31.8 | |
(1)仪器甲的名称为
(2)设实验所用的酸、碱溶液的密度均为1 g/cm
 ,且酸、碱中和后的溶液的比热容
,且酸、碱中和后的溶液的比热容 J⋅g
J⋅g ⋅C
⋅C 。计算该实验中生成1 mol水时的反应热△H=
。计算该实验中生成1 mol水时的反应热△H=(3)若改用60 mL 0.50 mol/L盐酸与60 mL 0.55 mol/LNaOH溶液进行反应,与(1)中实验相比,所放出的热量

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】某研究型学习小组的同学根据化学反应中的能量和速率变化对生产生活有着重要意义,进行下面的探究活动。
(1)甲同学为探究反应Fe+H2SO4(稀)=FeSO4+H2↑中的能量变化,向装有铁片的试管中滴加lmol/L的H2SO4,试管内产生气泡,触摸试管外壁,温度升高。
①该反应为______ (填“放热” 或“吸热” ) 反应。
②下列措施中,能加快氢气生成速率的是______ (填字母)。
a.将铁片改成铁粉 b. 将稀H2SO4改成浓硫酸 c.加硫酸钠溶液
(2)乙学生依据原电池原理也可加快反应速率,设计了Fe与稀硫酸反应的装置图,观察到的现象是_____ ;铜片上发生反应的电极反应式为_____ 。

(3)丙同学根据4NH3+6NO 5N2+6H2O反应的发生条件,在老师的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。
5N2+6H2O反应的发生条件,在老师的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。

①写出实验室用固体混合物加热的方法制备 NH3的化学方程式________ 。
②为了比较不同催化剂的催化性能,需要测量并记录的数据是__________ 。
③在不同催化剂时测得混合气体中NH3的物质的量与时间的关系如下图,则曲线_______ (填“①”或“②” 或“③”)使用的催化剂催化性能最好,理由是________ 。

(1)甲同学为探究反应Fe+H2SO4(稀)=FeSO4+H2↑中的能量变化,向装有铁片的试管中滴加lmol/L的H2SO4,试管内产生气泡,触摸试管外壁,温度升高。
①该反应为
②下列措施中,能加快氢气生成速率的是
a.将铁片改成铁粉 b. 将稀H2SO4改成浓硫酸 c.加硫酸钠溶液
(2)乙学生依据原电池原理也可加快反应速率,设计了Fe与稀硫酸反应的装置图,观察到的现象是

(3)丙同学根据4NH3+6NO
 5N2+6H2O反应的发生条件,在老师的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。
5N2+6H2O反应的发生条件,在老师的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。
①写出实验室用固体混合物加热的方法制备 NH3的化学方程式
②为了比较不同催化剂的催化性能,需要测量并记录的数据是
③在不同催化剂时测得混合气体中NH3的物质的量与时间的关系如下图,则曲线

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)直接排放煤燃烧产生的烟气会引起严重的环境问题。如果采用NaClO、Ca(ClO)2作吸收剂,能得到较好的烟气脱硫效果。已知下列反应:
SO2(g)+2OH-(aq)=SO32-(aq)+H2O(l) ΔH1
ClO-(aq)+SO32-(aq)=SO42-(aq)+Cl-(aq) ΔH2
CaSO4(s)=Ca2+(aq)+SO42-(aq) ΔH3
则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=_____ 。
(2)将0.1 mol MnO2粉末加入到50 mL过氧化氢溶液(H2O2,ρ=1.1 g/mL)中,在标准状况下放出气体的体积和时间的关系如图所示。

①实验时放出气体的总体积是________ 。
②放出一半气体所需的时间为______ 。
③反应放出 体积气体所需的时间约为
体积气体所需的时间约为_______ 。
④A,B,C,D各点反应速率的快慢顺序为______ 。
⑤解释反应速率变化的原因:_______ 。
⑥H2O2初始状态的浓度为________ 。
SO2(g)+2OH-(aq)=SO32-(aq)+H2O(l) ΔH1
ClO-(aq)+SO32-(aq)=SO42-(aq)+Cl-(aq) ΔH2
CaSO4(s)=Ca2+(aq)+SO42-(aq) ΔH3
则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)=CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=
(2)将0.1 mol MnO2粉末加入到50 mL过氧化氢溶液(H2O2,ρ=1.1 g/mL)中,在标准状况下放出气体的体积和时间的关系如图所示。

①实验时放出气体的总体积是
②放出一半气体所需的时间为
③反应放出
 体积气体所需的时间约为
体积气体所需的时间约为④A,B,C,D各点反应速率的快慢顺序为
⑤解释反应速率变化的原因:
⑥H2O2初始状态的浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
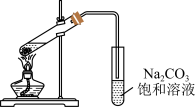
【推荐3】制备乙酸乙酯是中学有机化学中的一个重要实验。某化学学习小组的同学查阅资料发现,某些无机盐类也可以催化乙酸乙酯的合成,为了探究不同盐的催化效果,设计了如下实验:
实验步骤:向大试管中加入一定量的无机盐催化剂,再加入3mL无水乙醇和2mL冰醋酸,按图连接装置。用酒精灯小心均匀地加热试管5min,产生的蒸气经导管通到饱和碳酸钠溶液上方。
实验记录:使用不同的催化剂,实验得到的酯层高度如下表。
(1)实验时,需要加入几粒沸石,目的是_______ 。
(2)催化剂用量为3mmol(以阳离子计),选用的催化剂A可能是_______ (填标号)。
a.氯化铜晶体b.硫酸钙晶体c.碳酸钠晶体d.硝酸钾晶体
实验所用四种催化剂中,制备乙酸乙酯最好选用_______ 。
(3)若用18O标记乙醇中的O,用氯化铝作催化剂时,产生乙酸乙酯的化学方程式为_______ ,反应类型_______ 。
(4)实验中用饱和碳酸钠溶液的作用是_______ 。得到的混合液经_______ ,蒸馏,最终得到较纯净的乙酸乙酯。
实验步骤:向大试管中加入一定量的无机盐催化剂,再加入3mL无水乙醇和2mL冰醋酸,按图连接装置。用酒精灯小心均匀地加热试管5min,产生的蒸气经导管通到饱和碳酸钠溶液上方。
实验记录:使用不同的催化剂,实验得到的酯层高度如下表。

| 催化剂 | 酯层高度/cm | 催化剂 | 酯层高度/cm |
| 氯化铁晶体 | 2.7 | 氯化铝 | 3.2 |
| A | 2.2 | 氯化钠 | 0.0 |
(2)催化剂用量为3mmol(以阳离子计),选用的催化剂A可能是
a.氯化铜晶体b.硫酸钙晶体c.碳酸钠晶体d.硝酸钾晶体
实验所用四种催化剂中,制备乙酸乙酯最好选用
(3)若用18O标记乙醇中的O,用氯化铝作催化剂时,产生乙酸乙酯的化学方程式为
(4)实验中用饱和碳酸钠溶液的作用是
您最近一年使用:0次
【推荐1】Ⅰ、食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应用与其电离平衡密切相关。某小组研究25℃下HAc电离平衡的影响因素。
提出假设:稀释HAc溶液或改变 浓度,HAc电离平衡会发生移动。
浓度,HAc电离平衡会发生移动。
设计方案并完成实验,用浓度均为0.1mol⋅L 的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
(1)根据表中信息,补充数据:
___________ ,
___________ 。
(2)由表中实验Ⅰ和Ⅱ数据,可以得出HAc是弱电解质的结论,给出判断理由:___________ 。
(3)由实验Ⅱ~Ⅷ可知,增大 浓度,HAc电离平衡
浓度,HAc电离平衡___________ 移动(填“正向”或“逆向”)。
Ⅱ、研究金属腐蚀和防腐的原理很有现实意义。
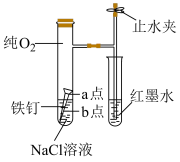
(4)探究钢铁吸氧腐蚀的装置如图所示。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰地观察到液柱上升现象的有___________(填字母)。

(5)为探究下图中铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,请完成表格空白:
提出假设:稀释HAc溶液或改变
 浓度,HAc电离平衡会发生移动。
浓度,HAc电离平衡会发生移动。设计方案并完成实验,用浓度均为0.1mol⋅L
 的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。| 序号 | V(HAc)/mL | V(NaAc)/mL |  /mL /mL |  | pH |
| Ⅰ | 40.00 | / | / | 0 | 2.86 |
| Ⅱ | 4.00 | / | 36.00 | 0 | 3.36 |
| … | |||||
| Ⅶ | 4.00 | a | 33.00 |  | 4.53 |
| Ⅷ | 4.00 | 4.00 | b |  | 4.65 |


(2)由表中实验Ⅰ和Ⅱ数据,可以得出HAc是弱电解质的结论,给出判断理由:
(3)由实验Ⅱ~Ⅷ可知,增大
 浓度,HAc电离平衡
浓度,HAc电离平衡Ⅱ、研究金属腐蚀和防腐的原理很有现实意义。
(4)探究钢铁吸氧腐蚀的装置如图所示。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰地观察到液柱上升现象的有___________(填字母)。

| A.用纯氧气代替试管内空气 | B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 | D.换成更大的试管,水中滴加红墨水 |

| 实验操作 | 实验现象 | 实验结论 |
| 向NaCl溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现 | a点电极反应为 |
| 然后再滴加2~3滴 | b点周围出现蓝色沉淀 | b点电极反应为 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学实验小组的同学为探究和比较SO2 和氯水的漂白性,设计了如下的实验装置。
(1)实验室用装置A制备SO2,某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,该同学怎样操作可以使分液漏斗液体顺利滴下___________________________ ;
(2)实验室用装置E制备Cl2,其反应的化学方程式为____________________ ,若实验室用酸性KMnO4 和浓盐酸反应制Cl2,反应的离子方程式为________________________ 。
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液都褪色,停止通气后,再给B、D 两个试管分别加热;两个试管中的现象分别为:B:___________ ,D:___________ 。
(4)若将B中品红换成Na2S溶液,通SO2一段时间后B中现象为_____________________ 。
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_________________________ 。

(1)实验室用装置A制备SO2,某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,该同学怎样操作可以使分液漏斗液体顺利滴下
(2)实验室用装置E制备Cl2,其反应的化学方程式为
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液都褪色,停止通气后,再给B、D 两个试管分别加热;两个试管中的现象分别为:B:
(4)若将B中品红换成Na2S溶液,通SO2一段时间后B中现象为
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】目前,常利用催化技术将汽车尾气中的NO和CO进行下列转化: 。为研究如何增大该化学反应的速率,某课题组进行了以下实验探究。
。为研究如何增大该化学反应的速率,某课题组进行了以下实验探究。
【查阅资料】使用等质量的同种催化剂,催化剂比表面积对催化效率有影响。
【实验设计】实验数据如表所示。
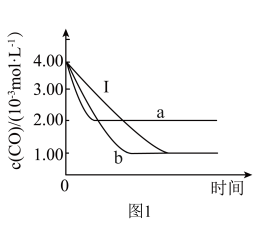
【图像分析】三组实验中CO的浓度随时间的变化如图1所示(曲线Ⅰ表示实验Ⅰ)。
(1)实验数据表格中,t=___________ ;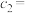
___________ 。
(2)第Ⅰ组实验中,从反应开始到达到平衡用时3min,用 表示该反应在此段时间内的反应速率为
表示该反应在此段时间内的反应速率为___________ 。
(3)要得出催化剂的比表面积对催化效率的影响,应比较曲线___________ 和曲线___________ (填“Ⅰ”、“a”或“b”)。
(4)从影响反应速率的角度分析,由曲线Ⅰ和a可得出的结论是___________ 。从化学平衡角度分析,该反应正方向为___________ (填“放热”或“吸热”)反应。
【拓展探究】该课题组进一步探究催化剂对CO、NO转化的影响。
将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图2所示。

(5)由此可知可使用的最佳催化剂和相应的最佳温度分别为___________ 、___________ 。
 。为研究如何增大该化学反应的速率,某课题组进行了以下实验探究。
。为研究如何增大该化学反应的速率,某课题组进行了以下实验探究。【查阅资料】使用等质量的同种催化剂,催化剂比表面积对催化效率有影响。
【实验设计】实验数据如表所示。
| 编号 | t/℃ |  | 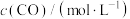 | 催化剂的比表面积/(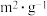 ) ) |
| Ⅰ | 280 | 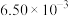 | 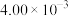 | 80 |
| Ⅱ |  | 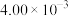 | 120.0 | |
| Ⅲ | 360 |  | 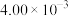 | 80.0 |

(1)实验数据表格中,t=
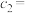
(2)第Ⅰ组实验中,从反应开始到达到平衡用时3min,用
 表示该反应在此段时间内的反应速率为
表示该反应在此段时间内的反应速率为(3)要得出催化剂的比表面积对催化效率的影响,应比较曲线
(4)从影响反应速率的角度分析,由曲线Ⅰ和a可得出的结论是
【拓展探究】该课题组进一步探究催化剂对CO、NO转化的影响。
将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图2所示。

(5)由此可知可使用的最佳催化剂和相应的最佳温度分别为
您最近一年使用:0次



