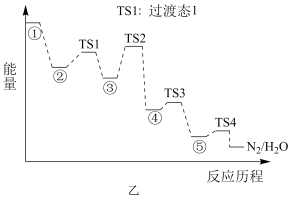
某种含二价铜微粒[CuⅡ(NH3)2]2+的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是
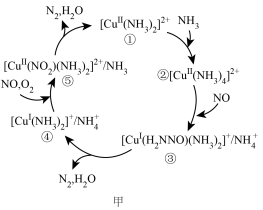


| A.催化机理中催化剂中Cu元素的化合价始终没有改变 |
| B.状态③到状态④的变化过程为图示反应的决速步骤 |
| C.[CuⅡ(NH3)2]2+可加快脱硝速率,提高脱销的平衡转化率 |
| D.升高温度,脱硝反应的正反应速率的增大程度大于逆反应速率的增大程度 |
22-23高二上·山东淄博·期末 查看更多[2]
更新时间:2023-10-04 12:28:29
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在一定温度下,在2L恒容密闭容器中发生反应N2+3H2⇌2NH3,反应过程中的部分数据如下表所示:
下列说法错误的是
| t/min | n(N2)/mol | n(H2)/mol | n(NH3)/mol |
| 0 | 2.0 | 2.4 | 0 |
| 5 | 1.7 | 1.5 | 0.6 |
| 10 | 1.6 | x | y |
| 15 | z | 1.2 | w |
| A.升高温度、增大N2的浓度均可加快反应速率 |
| B.0-5min内用NH3表示的平均反应速率为0.12mol·L-1·min-1 |
| C.10min时,反应已达到平衡状态,y为0.8mol |
| D.反应进行到2.5分钟时,剩余的N2的物质的量应小于1.85mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】液氨是一种很好的溶剂,液氨可以微弱的电离产生 和
和 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g)
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g) N2O4(g),下列说法正确的是
N2O4(g),下列说法正确的是
 和
和 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g)
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g) N2O4(g),下列说法正确的是
N2O4(g),下列说法正确的是A.该反应的 H>0 H>0  S<0 S<0 |
B.该反应的平衡常数表达式为  |
C.升高温度, 该反应的  (正)增大, (正)增大,  (逆)减小 (逆)减小 |
| D.将容器体积压缩为原来一半,气体颜色比压缩前深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】苯乙炔在某光催化材料上转化为苯乙烯的反应历程如图,Ph为苯基,下列说法错误的是
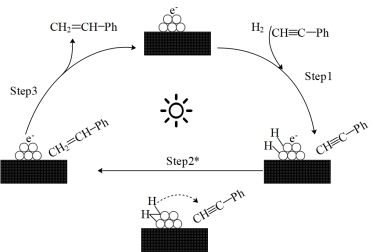

A.该反应的总方程式为 |
| B.该反应将太阳能转化为化学能 |
| C.苯乙炔经催化反应后转化率得到了提高 |
| D.催化剂表面无极性键的断裂,但有极性键的形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以TiO2为催化剂的光热化学循环分解CO2反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示,下列说法正确的是
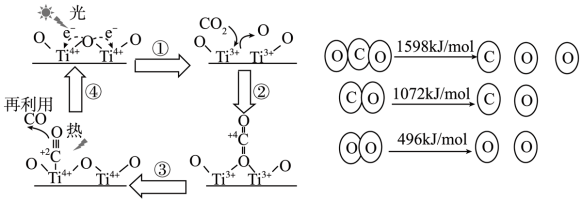

| A.过程①钛氧键发生了断裂释放了能量 |
| B.反应过程中,同时有极性键、非极性键的断裂和形成 |
| C.该反应中,光能和热能转化为化学能,且TiO2可以加快化学反应速率 |
| D.2mol二氧化碳完全分解成2mol一氧化碳和1mol氧气需要吸热30kJ |
您最近一年使用:0次

 S(l)+2CO2(g) ∆H= -37.0kJ·mol-1,SO2的平衡转化率[
S(l)+2CO2(g) ∆H= -37.0kJ·mol-1,SO2的平衡转化率[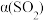 ]与投料比的比值
]与投料比的比值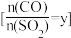 、温度(T)的关系如图所示。下列说法正确的是
、温度(T)的关系如图所示。下列说法正确的是

 是该反应的催化剂
是该反应的催化剂

