镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯[主要成分为 、
、 及少量铁、铝的氧化物等]生产硫酸镍﹑碳酸钴,其工艺流程如图所示。
及少量铁、铝的氧化物等]生产硫酸镍﹑碳酸钴,其工艺流程如图所示。

已知:
① 和
和 都能与盐酸发生氧化还原反应。
都能与盐酸发生氧化还原反应。
②常温下,部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
提示:当离子浓度小于 时,认为该种离子沉淀完全。
时,认为该种离子沉淀完全。
回答下列问题:
(1)“步骤①”用稀硫酸浸取金属电极芯前,需先粉碎金属电极芯,粉碎的目的是_______________ 。常温下,0.05 的稀硫酸的pH=
的稀硫酸的pH=__________ ,若将该稀硫酸的温度升高到40℃,pH将__________ (填“增大”、“减小”或“不变”)。
(2)“步骤②”调pH的范围为__________ 。
(3)常温下, ,则m=
,则m=__________ 。
(4)“步骤④”中从环保角度分析不采用盐酸的原因是_______________________ 。
(5)“步骤⑤”制 的离子方程式为
的离子方程式为___________________________________ 。
(6) 在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料[
在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料[ ]。该反应的离子方程式为
]。该反应的离子方程式为______________________________________ 。
 、
、 及少量铁、铝的氧化物等]生产硫酸镍﹑碳酸钴,其工艺流程如图所示。
及少量铁、铝的氧化物等]生产硫酸镍﹑碳酸钴,其工艺流程如图所示。
已知:
①
 和
和 都能与盐酸发生氧化还原反应。
都能与盐酸发生氧化还原反应。②常温下,部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
金属阳离子 |
|
|
|
|
|
|
开始沉淀时pH | 6.3 | 1.5 | 3.4 | 7.2 | — | 7.0 |
完全沉淀时pH | 8.3 | 2.8 | 4.7 | 9.1 | 1.1 | 9.0 |
 时,认为该种离子沉淀完全。
时,认为该种离子沉淀完全。回答下列问题:
(1)“步骤①”用稀硫酸浸取金属电极芯前,需先粉碎金属电极芯,粉碎的目的是
 的稀硫酸的pH=
的稀硫酸的pH=(2)“步骤②”调pH的范围为
(3)常温下,
 ,则m=
,则m=(4)“步骤④”中从环保角度分析不采用盐酸的原因是
(5)“步骤⑤”制
 的离子方程式为
的离子方程式为(6)
 在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料[
在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料[ ]。该反应的离子方程式为
]。该反应的离子方程式为
23-24高二上·贵州·期中 查看更多[4]
贵州省部分学校2023-2024学年高二上学期11月期中考试化学试题(已下线)期末押题卷02-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)广东省清远市阳山县南阳中学2023-2024学年高二上学期第二次月考(期中)化学试题安徽省安庆市怀宁县高河中学2023-2024学年高二上学期第三次月考化学试题
更新时间:2023-12-05 08:34:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】用于灭活新冠病毒的二氧化氯稳定性较差(纯 易分解爆炸),故用
易分解爆炸),故用 和
和 混合溶液将其吸收转化为
混合溶液将其吸收转化为 保存。现利用如下装置(夹持装置略去)及试剂制备
保存。现利用如下装置(夹持装置略去)及试剂制备 。
。

已知:① 熔点
熔点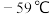 、沸点11℃,在碱性环境中发生反应:
、沸点11℃,在碱性环境中发生反应: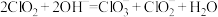 ;
;
②温度高于60℃时, 分解成
分解成 和
和 。
。
回答下列问题:
(1)装置A为 的发生装置,生成
的发生装置,生成 的离子方程式为
的离子方程式为_______ 。
(2)实验过程中持续通入 的作用是
的作用是
_______ 。
(3)装置B中 和
和 需按照一定比例混合配成溶液与
需按照一定比例混合配成溶液与 反应制取
反应制取 ,
, 作
作_______ (填“氧化剂”或“还原剂”);此装置需要采用冰水浴,可能的原因为_______ (任写一点)。
(4)装置C烧杯中的试剂是_______ 。
(5)某同学认为实验过程中会产生 ,推测产品中可能含
,推测产品中可能含 杂质,请设计简单实验证明:
杂质,请设计简单实验证明:_______ 。
 易分解爆炸),故用
易分解爆炸),故用 和
和 混合溶液将其吸收转化为
混合溶液将其吸收转化为 保存。现利用如下装置(夹持装置略去)及试剂制备
保存。现利用如下装置(夹持装置略去)及试剂制备 。
。
已知:①
 熔点
熔点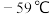 、沸点11℃,在碱性环境中发生反应:
、沸点11℃,在碱性环境中发生反应: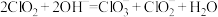 ;
;②温度高于60℃时,
 分解成
分解成 和
和 。
。回答下列问题:
(1)装置A为
 的发生装置,生成
的发生装置,生成 的离子方程式为
的离子方程式为(2)实验过程中持续通入
 的作用是
的作用是
(3)装置B中
 和
和 需按照一定比例混合配成溶液与
需按照一定比例混合配成溶液与 反应制取
反应制取 ,
, 作
作(4)装置C烧杯中的试剂是
(5)某同学认为实验过程中会产生
 ,推测产品中可能含
,推测产品中可能含 杂质,请设计简单实验证明:
杂质,请设计简单实验证明:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁( ),流程如图,回答下列问题。
),流程如图,回答下列问题。

(1)为提高浸取得速率,可采用的措施有___________ (任写一种)。
(2)过滤Ⅰ后,滤液中的含有金属阳离子___________ ,滤渣Ⅱ的主要成分是___________ (填化学式)。
(3)从过滤Ⅱ后的滤液中得到产品,应进行的操作是___________ 、___________ 、过滤、洗涤、干燥。
(4)还原时,试剂X的选用尽量不引入新的杂质,则该过程涉及的离子方程式有___________ 。如何检验还原是否彻底?___________ 。
 ),流程如图,回答下列问题。
),流程如图,回答下列问题。
(1)为提高浸取得速率,可采用的措施有
(2)过滤Ⅰ后,滤液中的含有金属阳离子
(3)从过滤Ⅱ后的滤液中得到产品,应进行的操作是
(4)还原时,试剂X的选用尽量不引入新的杂质,则该过程涉及的离子方程式有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】沼气中除 外,还含有
外,还含有 等气体,脱除沼气中的
等气体,脱除沼气中的 并使之转化为可再利用的资源有重要意义。
并使之转化为可再利用的资源有重要意义。
资料:i. (黄色溶液),
(黄色溶液), 与酸反应生成S、
与酸反应生成S、 (或
(或 )
)
ii. 均易溶于水
均易溶于水
(1)乙醇胺 可脱除沼气中的
可脱除沼气中的 ,这与其结构中的
,这与其结构中的_______ (填官能团名称)有关。加热所得产物,得到 ,同时乙醇胺得以再生。
,同时乙醇胺得以再生。
(2)采用加热法可将 转化为
转化为 和
和 。反应为:
。反应为: 。一定温度下,将
。一定温度下,将 置于
置于 密闭容器中加热分解,平衡时混合气中
密闭容器中加热分解,平衡时混合气中 与
与 的物质的量相等,该温度下反应的平衡常数
的物质的量相等,该温度下反应的平衡常数
_______ (用含a、v的代数式表示)。
(3)采用电解法也可将 转化为S和
转化为S和 。先用
。先用 溶液吸收
溶液吸收 气体,再电解所得溶液。电解时阴极产生无色气体,阳极附近溶液变为黄色。
气体,再电解所得溶液。电解时阴极产生无色气体,阳极附近溶液变为黄色。
①写出足量 溶液吸收
溶液吸收 气体的离子方程式:
气体的离子方程式:_______ 。
②用方程式解释阳极附近溶液变为黄色的原因_______ 。
③实验测得 的转化率大于S的收率,推测电解时阳极可能生成
的转化率大于S的收率,推测电解时阳极可能生成 、
、 等物质。实验证实了上述推测成立,写出检验
等物质。实验证实了上述推测成立,写出检验 的实验操作及现象:
的实验操作及现象:_______ 。
资料: 的转化率
的转化率 ;S的收率
;S的收率
④停止通电,向黄色溶液中通入_______ (填化学式)气体,析出S,过滤,滤液可继续电解。
 外,还含有
外,还含有 等气体,脱除沼气中的
等气体,脱除沼气中的 并使之转化为可再利用的资源有重要意义。
并使之转化为可再利用的资源有重要意义。资料:i.
 (黄色溶液),
(黄色溶液), 与酸反应生成S、
与酸反应生成S、 (或
(或 )
)ii.
 均易溶于水
均易溶于水(1)乙醇胺
 可脱除沼气中的
可脱除沼气中的 ,这与其结构中的
,这与其结构中的 ,同时乙醇胺得以再生。
,同时乙醇胺得以再生。(2)采用加热法可将
 转化为
转化为 和
和 。反应为:
。反应为: 。一定温度下,将
。一定温度下,将 置于
置于 密闭容器中加热分解,平衡时混合气中
密闭容器中加热分解,平衡时混合气中 与
与 的物质的量相等,该温度下反应的平衡常数
的物质的量相等,该温度下反应的平衡常数
(3)采用电解法也可将
 转化为S和
转化为S和 。先用
。先用 溶液吸收
溶液吸收 气体,再电解所得溶液。电解时阴极产生无色气体,阳极附近溶液变为黄色。
气体,再电解所得溶液。电解时阴极产生无色气体,阳极附近溶液变为黄色。①写出足量
 溶液吸收
溶液吸收 气体的离子方程式:
气体的离子方程式:②用方程式解释阳极附近溶液变为黄色的原因
③实验测得
 的转化率大于S的收率,推测电解时阳极可能生成
的转化率大于S的收率,推测电解时阳极可能生成 、
、 等物质。实验证实了上述推测成立,写出检验
等物质。实验证实了上述推测成立,写出检验 的实验操作及现象:
的实验操作及现象:资料:
 的转化率
的转化率 ;S的收率
;S的收率
④停止通电,向黄色溶液中通入
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料制备铵铁蓝Fe(NH4)Fe(CN)6颜料。工艺流程如下:

回答下列问题:
(1)红渣的主要成分为___________ (填化学式),滤渣①的主要成分为___________ (填化学式)。
(2)黄铁矿研细的目的是___________ 。
(3)工序①的名称为___________ ,所得母液循环使用。

回答下列问题:
(1)红渣的主要成分为
(2)黄铁矿研细的目的是
(3)工序①的名称为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】重铬酸钾(K2Cr2O7)是高中化学常见的的氧化剂,工业上以铬铁矿为原料用碱熔氧化法制备。铬铁矿中通常含有Cr2O3、FeO、Al2O3、SiO2等。

已知:
①NaFeO2常温遇大量水会强烈水解,高温时不与水反应
②2CrO (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O (橙色)+H2O
(橙色)+H2O
③+6价的铬元素在强酸性条件下具有强氧化性,还原产物为Cr3+,强碱性条件下几乎没有氧化性;请回答下列问题:
(1)将矿石粉碎的目的是___________________________ 。
(2)高温灼烧时生成NaFeO2的化学方程式____________________________________ 。
(3)①滤渣1中有红褐色物质,滤渣1的成分为__________________ (写化学式,下同),写出生成该物质反应的离子方程式___________________________ 。
②滤渣2的主要成分是__________________ 。
(4)若向Na2CrO4溶液中加入浓盐酸进行酸化,出现的现象为__________________
(5)生产后的废水中主要含有一定量的Cr2O72-,通常加一定量的绿矾进行净化并调节pH约为6,可生成两种难溶于水的沉淀,请写出该反应的离子方程式___________________________ 。

已知:
①NaFeO2常温遇大量水会强烈水解,高温时不与水反应
②2CrO
 (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O (橙色)+H2O
(橙色)+H2O③+6价的铬元素在强酸性条件下具有强氧化性,还原产物为Cr3+,强碱性条件下几乎没有氧化性;请回答下列问题:
(1)将矿石粉碎的目的是
(2)高温灼烧时生成NaFeO2的化学方程式
(3)①滤渣1中有红褐色物质,滤渣1的成分为
②滤渣2的主要成分是
(4)若向Na2CrO4溶液中加入浓盐酸进行酸化,出现的现象为
(5)生产后的废水中主要含有一定量的Cr2O72-,通常加一定量的绿矾进行净化并调节pH约为6,可生成两种难溶于水的沉淀,请写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】从铬锰矿渣(主要成分为 、MnO,杂质为
、MnO,杂质为 、
、 、
、 )中分离铬、锰的一种工艺流程如图所示:
)中分离铬、锰的一种工艺流程如图所示:
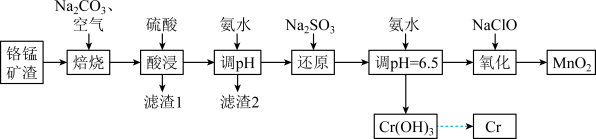
该工艺中,部分氢氧化物开始沉淀时和完全沉淀时的pH见下表:
回答下列问题:
(1)“焙烧”时空气是从焙烧炉下部进入,而矿渣粉是从上部投入的,这样做的优点是___________ 。
(2)“焙烧”中氧化产物只有 ,则相应反应中消耗的氧化剂与还原剂的物质的量之比为
,则相应反应中消耗的氧化剂与还原剂的物质的量之比为___________ ,“焙烧”中有___________ (填化学式)气体生成。
(3)第一次“调pH”时,理论上pH的最佳值是___________ 。“氧化”反应的离子方程式为___________ 。
(4)由 制备Cr的主要过程是灼烧
制备Cr的主要过程是灼烧 得到
得到 ,然后用铝热法还原
,然后用铝热法还原 得到Cr,则铝热法制备Cr的化学方程式为
得到Cr,则铝热法制备Cr的化学方程式为___________ 。
 、MnO,杂质为
、MnO,杂质为 、
、 、
、 )中分离铬、锰的一种工艺流程如图所示:
)中分离铬、锰的一种工艺流程如图所示:
该工艺中,部分氢氧化物开始沉淀时和完全沉淀时的pH见下表:
| 沉淀物 |  |  |  |  |
| 开始沉淀时的pH | 2.7 | 4.2 | 4.5 | 8.1 |
| 完全沉淀时的pH | 3.5 | 5.2 | 6.2 | 10.1 |
(1)“焙烧”时空气是从焙烧炉下部进入,而矿渣粉是从上部投入的,这样做的优点是
(2)“焙烧”中氧化产物只有
 ,则相应反应中消耗的氧化剂与还原剂的物质的量之比为
,则相应反应中消耗的氧化剂与还原剂的物质的量之比为(3)第一次“调pH”时,理论上pH的最佳值是
(4)由
 制备Cr的主要过程是灼烧
制备Cr的主要过程是灼烧 得到
得到 ,然后用铝热法还原
,然后用铝热法还原 得到Cr,则铝热法制备Cr的化学方程式为
得到Cr,则铝热法制备Cr的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】 (钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1%
(钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1% 、19.5%Fe和3.4%
、19.5%Fe和3.4% )为原料制备钒酸铋,并回收
)为原料制备钒酸铋,并回收 制备食品抗氧化剂
制备食品抗氧化剂 的流程如下:
的流程如下: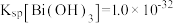 ,
,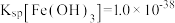 ;当金属离子浓度
;当金属离子浓度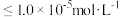 时,认为该离子已沉淀完全。请回答下列问题:
时,认为该离子已沉淀完全。请回答下列问题:
(1)“焙烧”中采用高压空气的目的是_______ , 转化成
转化成 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(2)浸渣的主要成分是_______ (填化学式)。
(3)“酸浸”得到的浸液中 ,则“除铁”调节pH的范围为
,则“除铁”调节pH的范围为_______ 。
(4)“合成”过程中将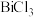 溶液和
溶液和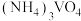 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为_______ (答一条)。
(5)向饱和碳酸钠溶液中通入过量 可制得
可制得 ,发生反应的化学方程式为
,发生反应的化学方程式为_______ 。 易变质生成
易变质生成 ,设计简单实验证明产品是否变质:
,设计简单实验证明产品是否变质:_______ 。(已知: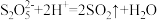 )
)
(6)某工厂用20吨该辉铋矿,最终得到18.468吨 ,则该过程中Bi的损耗率为
,则该过程中Bi的损耗率为______ %。
 (钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1%
(钒酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1% 、19.5%Fe和3.4%
、19.5%Fe和3.4% )为原料制备钒酸铋,并回收
)为原料制备钒酸铋,并回收 制备食品抗氧化剂
制备食品抗氧化剂 的流程如下:
的流程如下:
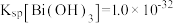 ,
,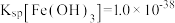 ;当金属离子浓度
;当金属离子浓度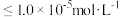 时,认为该离子已沉淀完全。请回答下列问题:
时,认为该离子已沉淀完全。请回答下列问题:(1)“焙烧”中采用高压空气的目的是
 转化成
转化成 发生反应的化学方程式为
发生反应的化学方程式为(2)浸渣的主要成分是
(3)“酸浸”得到的浸液中
 ,则“除铁”调节pH的范围为
,则“除铁”调节pH的范围为(4)“合成”过程中将
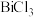 溶液和
溶液和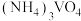 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为(5)向饱和碳酸钠溶液中通入过量
 可制得
可制得 ,发生反应的化学方程式为
,发生反应的化学方程式为 易变质生成
易变质生成 ,设计简单实验证明产品是否变质:
,设计简单实验证明产品是否变质: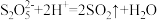 )
)(6)某工厂用20吨该辉铋矿,最终得到18.468吨
 ,则该过程中Bi的损耗率为
,则该过程中Bi的损耗率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】一种从阳极泥(主要成分为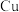 、
、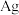 、
、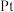 、
、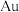 、
、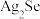 和
和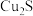 等)中回收
等)中回收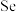 和贵重金属的工艺流程如下图所示.
和贵重金属的工艺流程如下图所示.
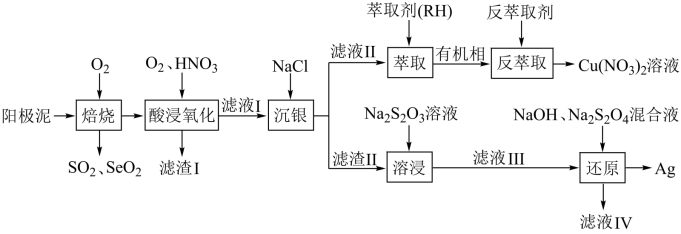
已知:①该工艺中萃取与反萃取原理为: ;
;
② 在碱性条件下很稳定,有很强的络合能力,易与
在碱性条件下很稳定,有很强的络合能力,易与 形成配离子:
形成配离子: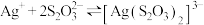 ,常温下该反应的平衡常数
,常温下该反应的平衡常数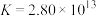 .
.
回答下列问题:
(1)“滤渣Ⅰ”的主要成分是____________ ;“酸浸氧化”中通入氧气的目的是___________________ .
(2)“反萃取剂”最好选用____________ (填化学式)溶液.
(3)“溶浸”中发生的反应为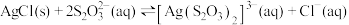 ,该反应的平衡常数
,该反应的平衡常数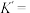
__________ [已知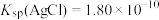 ].
].
(4)“滤液Ⅳ”中含有 ,则“还原”中发生反应的离子方程式为
,则“还原”中发生反应的离子方程式为____________________ ;“滤液Ⅳ”可返回“溶浸”工序循环使用,但循环多次后,银的浸出率会降低,原因是________________ (试用平衡原理解释).
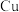 、
、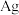 、
、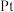 、
、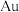 、
、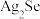 和
和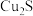 等)中回收
等)中回收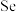 和贵重金属的工艺流程如下图所示.
和贵重金属的工艺流程如下图所示.
已知:①该工艺中萃取与反萃取原理为:
 ;
;②
 在碱性条件下很稳定,有很强的络合能力,易与
在碱性条件下很稳定,有很强的络合能力,易与 形成配离子:
形成配离子: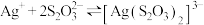 ,常温下该反应的平衡常数
,常温下该反应的平衡常数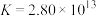 .
.回答下列问题:
(1)“滤渣Ⅰ”的主要成分是
(2)“反萃取剂”最好选用
(3)“溶浸”中发生的反应为
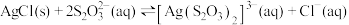 ,该反应的平衡常数
,该反应的平衡常数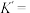
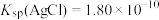 ].
].(4)“滤液Ⅳ”中含有
 ,则“还原”中发生反应的离子方程式为
,则“还原”中发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
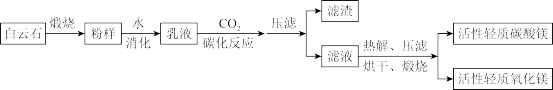
【推荐3】自然界中镁元素在地壳中存在的形式有菱镁矿[主要成分是碳酸镁,MgCO3]、 白云石[主要成分是碳酸钙镁,CaMg(CO3)2]、光卤石[主要成分是氯化铁钾,KCl·MgCl2·H2O]。图是利用白云石为原料获得活性轻质氧化镁和活性轻质碳酸镁[xMgCO3·yMg(OH)2·zH2O]的传统工艺流程:
已知:①Ksp(MgCO3)= 3.5 ×10-8, Ksp(CaCO3)= 2.8 ×10-9,Ksp[Mg(OH)2]= 1.8×10-11, Ksp[Ca(OH)2] = 5.5×10-6;
②MgO及MgCO3悬浊液在CO2作用下会逐渐溶解生成可溶性盐。
(1)“粉样”的主要成分是_____________________ ;“滤渣”的主要成分是___________________ 。
(2)“滤液” 热解首先发生的化学反应方程式是_________ 。
(3)以下是对传统工艺流程的改进方案流程:

①“滤液1”的主要溶质成分是_________ 。
②试用化学平衡移动原理解释过程“ 乳液 ”:
”: _________ 。
③下列关于传统方案与改进方案的说法错误的是_________ (填正确答案标号)
A. 传统方案所得滤渣中总是含有部分镁的化合物
B. 两种方案中滤渣的成分相同
C. 改进方案中CO2的消耗更低
D. “消化”过程中没有新物质生成
(4)向10 mL 0.01 mol·L-1 MgCl2溶液中加入Na2CO3固体到Mg2+沉淀完全(一般认为,当溶液中离子浓度小于1×10-5 mol·L-1时,该离子沉淀完全:忽略CO 的水解),忽略溶液体积变化,则所得溶液中c(Na+)至少为
的水解),忽略溶液体积变化,则所得溶液中c(Na+)至少为__________ mol·L-1。

已知:①Ksp(MgCO3)= 3.5 ×10-8, Ksp(CaCO3)= 2.8 ×10-9,Ksp[Mg(OH)2]= 1.8×10-11, Ksp[Ca(OH)2] = 5.5×10-6;
②MgO及MgCO3悬浊液在CO2作用下会逐渐溶解生成可溶性盐。
(1)“粉样”的主要成分是
(2)“滤液” 热解首先发生的化学反应方程式是
(3)以下是对传统工艺流程的改进方案流程:

①“滤液1”的主要溶质成分是
②试用化学平衡移动原理解释过程“ 乳液
 ”:
”: ③下列关于传统方案与改进方案的说法错误的是
A. 传统方案所得滤渣中总是含有部分镁的化合物
B. 两种方案中滤渣的成分相同
C. 改进方案中CO2的消耗更低
D. “消化”过程中没有新物质生成
(4)向10 mL 0.01 mol·L-1 MgCl2溶液中加入Na2CO3固体到Mg2+沉淀完全(一般认为,当溶液中离子浓度小于1×10-5 mol·L-1时,该离子沉淀完全:忽略CO
 的水解),忽略溶液体积变化,则所得溶液中c(Na+)至少为
的水解),忽略溶液体积变化,则所得溶液中c(Na+)至少为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】高铁酸钾(K2FeO4)是一种高效净水剂。已知:K2FeO4易溶于水,其溶液呈紫色、微溶于浓KOH溶液,在0℃~5℃的强碱性溶液中较稳定。某小组同学用下图装置制备并探究K2FeO4的性质。制备原理:3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,装置如图所示(夹持装置略)。

(1)盛放二氧化锰的仪器名称___________________ ,装置C的作用是____________________ 。
(2)装置A 中反应的化学方程式是________________________________________ 。
(3)实验时采用冰水浴的原因是________________ ,此装置存在一处明显缺陷,请指出___________ 。
(4)K2FeO4粗产品含有Fe(OH)3、KCl等杂质,一般用75%乙醇进行洗涤,其目的是_________ 。
(5)查阅资料知,K2FeO4能将 Mn2+氧化成 MnO4-。该小组设计如下实验进行验证:

关闭K,左烧杯溶液变黄色,右烧杯溶液变紫色。检验左侧烧杯溶液呈黄色的原因,需要的试剂是_______ ;写出上图中负极的电极反应式: _________ 。

(1)盛放二氧化锰的仪器名称
(2)装置A 中反应的化学方程式是
(3)实验时采用冰水浴的原因是
(4)K2FeO4粗产品含有Fe(OH)3、KCl等杂质,一般用75%乙醇进行洗涤,其目的是
(5)查阅资料知,K2FeO4能将 Mn2+氧化成 MnO4-。该小组设计如下实验进行验证:

关闭K,左烧杯溶液变黄色,右烧杯溶液变紫色。检验左侧烧杯溶液呈黄色的原因,需要的试剂是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】能量、速率与限度是认识和研究化学反应的重要视角。
Ⅰ.为了探究原电池的工作原理,设计如下装置。________ 。
(2)当乙装置中的负极质量减少1.8g时,正极产生气体________ L(标准状况下); 向
向________ (填“Mg”或“Al”)电极移动。
Ⅱ. 、
、 都是重要的能源物质,也是重要的化工原料。利用
都是重要的能源物质,也是重要的化工原料。利用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。
(3)反应过程中的能量变化如图所示:________ (填“放热”或“吸热”)反应。
(4)300℃时,向容积为2L的恒容密闭容器中,充入 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: 的浓度随时间变化曲线为
的浓度随时间变化曲线为________ (填“a”、“b”或“c”);在M点,
________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
②2min时,反应速率改变的原因可能是________ 。
A.升高温度 B.降低温度 C.充入一定量的 D.加入催化剂
D.加入催化剂
③下列叙述不能说明该反应达到平衡状态的是________ 。
A.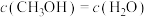
B.混合气体的密度不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内生成 ,同时消耗
,同时消耗
Ⅰ.为了探究原电池的工作原理,设计如下装置。
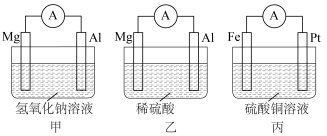
(2)当乙装置中的负极质量减少1.8g时,正极产生气体
 向
向Ⅱ.
 、
、 都是重要的能源物质,也是重要的化工原料。利用
都是重要的能源物质,也是重要的化工原料。利用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。(3)反应过程中的能量变化如图所示:

(4)300℃时,向容积为2L的恒容密闭容器中,充入
 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: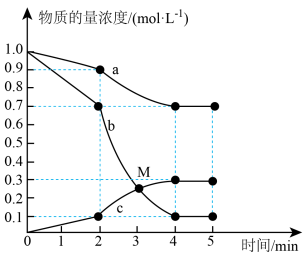
 的浓度随时间变化曲线为
的浓度随时间变化曲线为
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②2min时,反应速率改变的原因可能是
A.升高温度 B.降低温度 C.充入一定量的
 D.加入催化剂
D.加入催化剂③下列叙述不能说明该反应达到平衡状态的是
A.
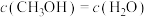
B.混合气体的密度不再变化
C.混合气体的平均摩尔质量不再变化
D.单位时间内生成
 ,同时消耗
,同时消耗
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】下图是某氢氧燃料电池的结构示意图,电解质为硫酸溶液。电池总反应为2H2+O2=2H2O,完成下列问题:

(1)通H2的极为电池的_______ 极(填“正”或“负”)。
(2)b极上的电极反应式为:_______ 。
(3)每转移0.1 mol电子,消耗H2的体积为_______ L(标准状况下)。
(4)若将氢气换成二乙醚(C4H10O),将电解质溶液硫酸换成氢氧化钠溶液,去掉质子交换膜。
①则b极的电极反应式为_______ 。
②电池工作一段时间后电解质溶液的pH_______ (填“增大”“减小”或“不变”)。
(5)氢氧燃料电池为环境友好电池。而传统电池生产企业排放的工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,常用FeS等难溶物质作为沉淀剂除去这些离子。室温下Ksp(FeS)=6.3×10-18 mol2·L-2,Ksp(CuS)=1.3×10-36 mol2·L-2。请用离子方程式说明上述除杂的原理_______ 。

(1)通H2的极为电池的
(2)b极上的电极反应式为:
(3)每转移0.1 mol电子,消耗H2的体积为
(4)若将氢气换成二乙醚(C4H10O),将电解质溶液硫酸换成氢氧化钠溶液,去掉质子交换膜。
①则b极的电极反应式为
②电池工作一段时间后电解质溶液的pH
(5)氢氧燃料电池为环境友好电池。而传统电池生产企业排放的工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,常用FeS等难溶物质作为沉淀剂除去这些离子。室温下Ksp(FeS)=6.3×10-18 mol2·L-2,Ksp(CuS)=1.3×10-36 mol2·L-2。请用离子方程式说明上述除杂的原理
您最近一年使用:0次









