已知N2O和CO反应进程的相对能量变化如图所示。已知CO(g)的燃烧热ΔH=-283kJ·mol-1。下列说法错误的是
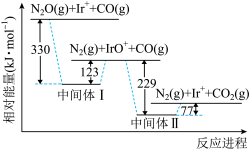

| A.中间体Ⅱ比中间体I稳定 |
| B.Ir+是上述反应的催化剂 |
| C.该反应过程中Ir元素的化合价发生了变化 |
D.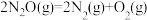 的反应热ΔH为-76kJ·mol-1 的反应热ΔH为-76kJ·mol-1 |
更新时间:2023-12-06 10:15:19
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知反应 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
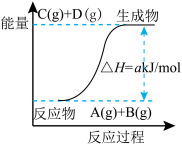
 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
| A.该体系的压强不变时标志此反应处于平衡状态 |
| B.若该反应中有电子得失,则可设计成原电池 |
| C.反应物的总键能高于生成物的总键能 |
| D.该反应中的反应物A和B的转化率一定相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知如下化学键的键能:
则下列热化学方程式不 正确的是
| 化学键 | H—H | Cl—Cl | H—Cl |
| 生成1 mol化学键时放出的能量 | 436kJ/mol | 243kJ/mol | 431kJ/mol |
A. H2(g)+ H2(g)+ Cl2(g)=HCl(g) ΔH=-91.5kJ/mol Cl2(g)=HCl(g) ΔH=-91.5kJ/mol |
| B.H2(g)+Cl2(g)=2HCl(g) ΔH=-183kJ/mol |
| C.2HCl(g)=H2(g)+Cl2(g) ΔH=+183kJ/mol |
D. H2(g)+ H2(g)+ Cl2(g)=HCl(g) ΔH=+91.5kJ/mol Cl2(g)=HCl(g) ΔH=+91.5kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知:2H2(g) +O2(g) =2H2O(l), △H =-571.6 kJ/mol;H2O(1) =H2O(g),△H = +44 kJ/mol下列说法中正确的是
| A.液态水的能量高于气态水 |
| B.2H2(g)+O2(g) =2H2O(g) △H =- 483.6 kJ/mol |
| C.1 mol H2完全燃烧生成气态水放出的热量大于285.8 kJ |
| D.形成1 mol H2O中化学键释放的总能量小于断裂1molH2和0.5molO2中化学键所吸收的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知:S(s)+O2(g)=SO2(g)△H=﹣297.2kJ•mol﹣1。下列说法中正确的是( )
| A.S(s)具有的能量大于SO2(g)具有的能量 |
| B.S(g)+O2(g)=SO2(g)的△H>﹣297.2kJ•mol﹣1 |
| C.S(s)的燃烧热为297.2kJ•mol﹣1 |
| D.形成1mol SO2中的化学键所需能量大于断裂1molS中的化学键所需能量 |
您最近一年使用:0次
【推荐2】下列图示与对应的叙述不相符的是
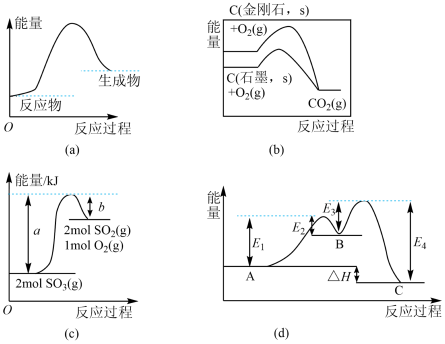

| A.(a)图表示反应物断键吸收的能量大于生成物成键放出的能量 |
B.(b)图是金刚石与石墨分别被氧化生成 的能量关系曲线,说明石墨转化为金刚石的反应的 的能量关系曲线,说明石墨转化为金刚石的反应的 |
C.由(c)图可知,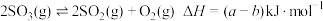 |
D.(d)图是某反应:A→C(由两步反应A→B→C完成,B为中间产物)的能量曲线(E表示能量),整个反应中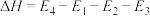 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】合成尿素 是利用
是利用 的途径之一,工业上以
的途径之一,工业上以 和
和 为原料在一定温度和压强下合成尿素的反应历程分如下两步进行(假设每步均为基元反应):
为原料在一定温度和压强下合成尿素的反应历程分如下两步进行(假设每步均为基元反应):
反应a:
反应b:
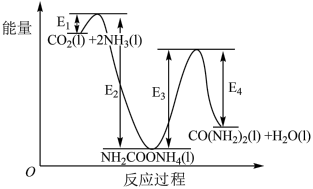
结合反应过程中的能量变化图,下列说法错误的是
 是利用
是利用 的途径之一,工业上以
的途径之一,工业上以 和
和 为原料在一定温度和压强下合成尿素的反应历程分如下两步进行(假设每步均为基元反应):
为原料在一定温度和压强下合成尿素的反应历程分如下两步进行(假设每步均为基元反应):反应a:

反应b:


结合反应过程中的能量变化图,下列说法错误的是
| A.反应a为放热反应,反应b为吸热反应 |
| B.反应a为快反应,反应b为慢反应 |
C.增大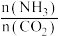 的投料比,二氧化碳的平衡转化率增大 的投料比,二氧化碳的平衡转化率增大 |
D.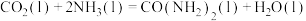 的 的 |
您最近一年使用:0次
【推荐2】在含Fe3+、 和I-的溶液中,发生反应:
和I-的溶液中,发生反应: ,其分解机理及反应进程中的能量变化如下:
,其分解机理及反应进程中的能量变化如下:
步骤①:
步骤②:
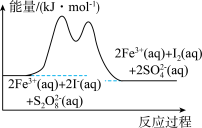
下列有关该反应的说法正确的是
 和I-的溶液中,发生反应:
和I-的溶液中,发生反应: ,其分解机理及反应进程中的能量变化如下:
,其分解机理及反应进程中的能量变化如下:步骤①:

步骤②:


下列有关该反应的说法正确的是
| A.步骤②是整个反应的决速步骤 |
| B.加入Fe3+可以使反应物分子中活化分子百分数增大 |
| C.总反应的∆H>0 |
| D.若不加Fe3+,则正反应的活化能比逆反应的大 |
您最近一年使用:0次

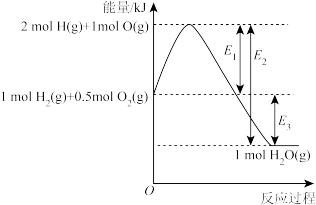
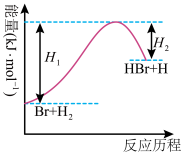
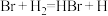 的能量—反应历程的示意图,下列叙述中不正确的是
的能量—反应历程的示意图,下列叙述中不正确的是