 是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。
是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。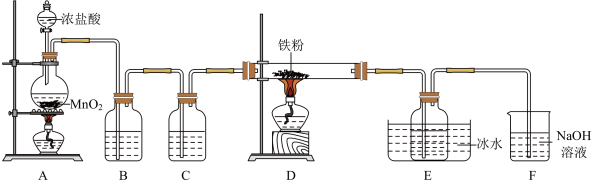
已知:①
 易升华、遇水蒸气易潮解。
易升华、遇水蒸气易潮解。②实验室用铁氰化钾{
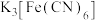 }溶液检验
}溶液检验 ,产生蓝色沉淀。
,产生蓝色沉淀。回答下列问题:
(1)盛装浓盐酸的仪器是
(2)装置A中发生反应的化学方程式为
(3)装置E中冰水浴的作用是
(4)上述实验装置存在两处缺陷导致产品产率偏低,解决方案是:一是加租制备产品的导气管,防堵塞;二是
(5)对实验装置进行改进后,继续完成实验。实验完毕后,取产品探究其性质:
实验 | 操作 | 现象 |
① | 取少量固体溶于蒸馏水,滴加KSCN溶液 | 溶液变红色 |
② | 取少量固体溶于稀硫酸 | 固体溶解,无气泡产生 |
更新时间:2024-01-07 08:40:31
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】如图,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请据图回答下列问题:
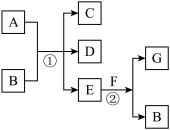
(1)G、A的化学式分别为_______ 、_______ 。
(2)写出反应①的离子方程式:_______ 。
(3)写出反应②的化学方程式:_______
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是_______ 。
②A可以制漂白粉,漂白粉在空气时间长了会失效,失效的原因是_______ (用化学方程式表示)。

(1)G、A的化学式分别为
(2)写出反应①的离子方程式:
(3)写出反应②的化学方程式:
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是
②A可以制漂白粉,漂白粉在空气时间长了会失效,失效的原因是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
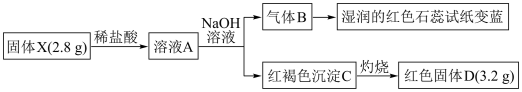
【推荐2】磁性物质X只含两种元素,属于半金属材料,某兴趣小组对化合物X的组成展开如下探究(图中部分产物未标出)。
。
请回答:
(1)固体X含有的元素是_______ (用元素符号表示),其化学式为_______ 。
(2)写出气体B在催化剂存在下被氧气氧化的方程式。_______ 。
(3)写出溶液A中加入足量NaOH溶液的离子方程式_______ 。
(4)请设计简单实验检验红色固体D中的金属元素存在的形式_______ 。
。

请回答:
(1)固体X含有的元素是
(2)写出气体B在催化剂存在下被氧气氧化的方程式。
(3)写出溶液A中加入足量NaOH溶液的离子方程式
(4)请设计简单实验检验红色固体D中的金属元素存在的形式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】硼酸( )为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能提高机械强度,缩短熔融时间。以硼镁矿(含
)为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能提高机械强度,缩短熔融时间。以硼镁矿(含 、
、 及少量
及少量 、
、 )为原料生产硼酸的工艺流程如下:
)为原料生产硼酸的工艺流程如下:

已知:
① 在20℃,40℃,60℃,100℃时溶解度依次为5.0g,8.7g,14.8g,40.2g。
在20℃,40℃,60℃,100℃时溶解度依次为5.0g,8.7g,14.8g,40.2g。
②有关金属离子开始沉淀和沉淀完全的pH见下表
(1)写出硼元素在周期表中的位置___________ ;
(2)“酸浸”时生成 的化学方程式为
的化学方程式为___________ ;
(3)“热过滤”的目的是___________ ;
(4)“固体1”的主要成分是___________ (写化学式);
(5)从绿色化学角度考虑,试剂A宜选择___________ ,作用是___________ (用离子方程式表示);
(6)“氧化”后将溶液pH调节至6,目的是___________ ;
(7)“母液”中的溶质主要有___________ ,___________ 。
 )为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能提高机械强度,缩短熔融时间。以硼镁矿(含
)为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能提高机械强度,缩短熔融时间。以硼镁矿(含 、
、 及少量
及少量 、
、 )为原料生产硼酸的工艺流程如下:
)为原料生产硼酸的工艺流程如下:
已知:
①
 在20℃,40℃,60℃,100℃时溶解度依次为5.0g,8.7g,14.8g,40.2g。
在20℃,40℃,60℃,100℃时溶解度依次为5.0g,8.7g,14.8g,40.2g。②有关金属离子开始沉淀和沉淀完全的pH见下表
 |  |  |  | |
| 开始沉淀时 | 3.8 | 5.8 | 2.2 | 10.6 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 | 12.4 |
(2)“酸浸”时生成
 的化学方程式为
的化学方程式为(3)“热过滤”的目的是
(4)“固体1”的主要成分是
(5)从绿色化学角度考虑,试剂A宜选择
(6)“氧化”后将溶液pH调节至6,目的是
(7)“母液”中的溶质主要有
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】实验室产生的酸性废液中含有Fe3+、Cu2+两种金属离子,某同学设计了如图所示方案对废液进行处理来回收金属,保护环境。
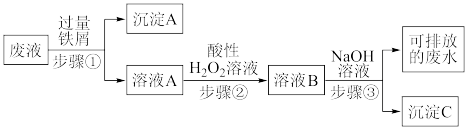
(1)沉淀A的成分是:_____ (写化学式),若步骤①中加入少量铁屑,无沉淀生成,此时发生反应的离子方程式为____ 。
(2)如何检验溶液A中的金属阳离子,简述其方法:_____ 。
(3)写出步骤②发生反应的化学方程式:_____ 。
(4)步骤③的操作名称是____ ,用到的主要玻璃仪器有烧杯、____ ,沉淀C与胶体C的本质区别是:____ 。

(1)沉淀A的成分是:
(2)如何检验溶液A中的金属阳离子,简述其方法:
(3)写出步骤②发生反应的化学方程式:
(4)步骤③的操作名称是
您最近一年使用:0次
【推荐2】以绿矾(主要成分为FeSO4·7H2O,部分Fe2+已被氧化为Fe3+)为原料,生产铁红(Fe2O3)的工艺流程如下:

(1)“转化”过程中,加入Fe粉的作用是___________ 。转化前将绿矾研碎,转化中进行搅拌和加热,目的是___________ 。
(2)“结晶”时,控制温度在75°C左右进行(相关物质的溶解度见下图),从溶液中析出的晶体是___________ (填化学式)。

(3)“滤液”中的溶质为___________ (填化学式)。利用该滤液将工业废水中的Cr2O 还原为Cr3+,然后投加石灰乳,使Cr3+转化为Cr(OH)3沉淀,理论上完全反应消耗的n(Cr2O
还原为Cr3+,然后投加石灰乳,使Cr3+转化为Cr(OH)3沉淀,理论上完全反应消耗的n(Cr2O ):n(FeSO4)=
):n(FeSO4)=___________ 。
(4)“煅烧”过程中,每生成1mol铁红,需消耗___________ molO2,同时生成___________ molSO3和___________ molH2O。

(1)“转化”过程中,加入Fe粉的作用是
(2)“结晶”时,控制温度在75°C左右进行(相关物质的溶解度见下图),从溶液中析出的晶体是

(3)“滤液”中的溶质为
 还原为Cr3+,然后投加石灰乳,使Cr3+转化为Cr(OH)3沉淀,理论上完全反应消耗的n(Cr2O
还原为Cr3+,然后投加石灰乳,使Cr3+转化为Cr(OH)3沉淀,理论上完全反应消耗的n(Cr2O ):n(FeSO4)=
):n(FeSO4)=(4)“煅烧”过程中,每生成1mol铁红,需消耗
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】硫酸亚铁(FeSO4)工业上常用废铁屑和稀硫酸制备。实验室通过如图装置模拟其制备过程。请回答下列问题:
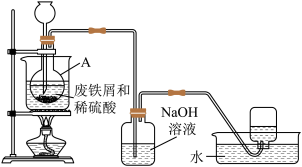
(1)进行实验之前需检查整套装置的_______ 。装置甲中仪器A的名称是_______ 。
(2)常温下废铁屑和稀硫酸反应较慢,而直接加热时温度过高又可能产生Fe3+等副产物,因此,采用水浴加热,并使用过量的 将可能产生的Fe3+还原成Fe2+。
将可能产生的Fe3+还原成Fe2+。 还原Fe3+的离子方程式为
还原Fe3+的离子方程式为_______ 。
(3)废铁屑中含有硫化物杂质,故反应中会生成少量的H2S气体。因此,装置乙中NaOH溶液的主要作用是_______ 。

(1)进行实验之前需检查整套装置的
(2)常温下废铁屑和稀硫酸反应较慢,而直接加热时温度过高又可能产生Fe3+等副产物,因此,采用水浴加热,并使用过量的
 将可能产生的Fe3+还原成Fe2+。
将可能产生的Fe3+还原成Fe2+。 还原Fe3+的离子方程式为
还原Fe3+的离子方程式为(3)废铁屑中含有硫化物杂质,故反应中会生成少量的H2S气体。因此,装置乙中NaOH溶液的主要作用是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】硝酸铜晶体[Cu(NO3)2·6H2O],是一种重要的化工原料,常用于农药、镀铜、搪瓷等工业。以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备硝酸铜晶体的某工艺如图所示:

回答下列问题:
(1)“浸取”时,为了提高浸取率可采取的措施有______ (任写一点),浸取时在生成S的反应中还原剂与氧化剂的物质的量之比为______ 。
(2)薄层层析法是利用溶液各成分对同一吸附剂吸附能力不同,在溶液流过吸附剂时,使各成分互相分离的方法。某实验小组利用薄层层析法监控滤液1加入铁粉过程中溶液的组成,实验结果如下,则还需继续加入Fe粉的是______ (选填编号)。

(3)滤渣2的主要成分是______ ,滤渣2与稀硝酸反应时,需向装置内通入适量空气,这样做的目的是______ 。
(4)调节溶液pH时选用的物质a可以是______ ,几种金属离子沉淀的pH范围如图所示,“调pH”时应将溶液pH调至______ ~______ 。

(5)操作X主要包括______ 、______ 、过滤、洗涤、干燥。

回答下列问题:
(1)“浸取”时,为了提高浸取率可采取的措施有
(2)薄层层析法是利用溶液各成分对同一吸附剂吸附能力不同,在溶液流过吸附剂时,使各成分互相分离的方法。某实验小组利用薄层层析法监控滤液1加入铁粉过程中溶液的组成,实验结果如下,则还需继续加入Fe粉的是

(3)滤渣2的主要成分是
(4)调节溶液pH时选用的物质a可以是

(5)操作X主要包括
您最近一年使用:0次
【推荐2】NaN3是一种易溶于水(NaN3=Na++N )的白色固体,可用于有机合成和汽车安全气囊的产气药等。钠法(液氨法)制备NaN3的工艺流程如图:
)的白色固体,可用于有机合成和汽车安全气囊的产气药等。钠法(液氨法)制备NaN3的工艺流程如图:
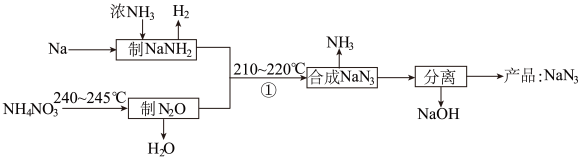
(1)钠元素位于周期表第_______ 周期_______ 族。
(2)NaNH2中氮元素的化合价为_______ ;Na+的结构示意图为_______ 。
(3)NaOH的电子式为_______ 。
(4)反应NH4NO3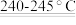 N2O↑+2H2O↑中,每生成1mol N2O转移电子数为
N2O↑+2H2O↑中,每生成1mol N2O转移电子数为_______ 个。
 )的白色固体,可用于有机合成和汽车安全气囊的产气药等。钠法(液氨法)制备NaN3的工艺流程如图:
)的白色固体,可用于有机合成和汽车安全气囊的产气药等。钠法(液氨法)制备NaN3的工艺流程如图: 
(1)钠元素位于周期表第
(2)NaNH2中氮元素的化合价为
(3)NaOH的电子式为
(4)反应NH4NO3
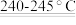 N2O↑+2H2O↑中,每生成1mol N2O转移电子数为
N2O↑+2H2O↑中,每生成1mol N2O转移电子数为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】实验室用卤块(主要成分为 ,含有
,含有 、
、 等杂质)制备少量
等杂质)制备少量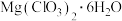 的流程如图:
的流程如图:

已知:①四种化合物的溶解度(S)随温度(T)变化曲线如图所示:

②室温时一些物质的 如表:
如表:
③ 有较强的氧化性,其还原产物是
有较强的氧化性,其还原产物是 ,回答下列问题:
,回答下列问题:
(1) 的电子式为
的电子式为___________ ,滤渣的成分是_____________ (填化学式)。
(2)流程图中所发生的化学反应方程式为______________ ,框图中由反应→…→制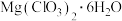 晶体的实验步骤依次为:①加热蒸发;②
晶体的实验步骤依次为:①加热蒸发;②___________ (请补充);③冷却结晶;④过滤洗涤。
 ,含有
,含有 、
、 等杂质)制备少量
等杂质)制备少量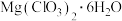 的流程如图:
的流程如图:
已知:①四种化合物的溶解度(S)随温度(T)变化曲线如图所示:

②室温时一些物质的
 如表:
如表:化学式 |
|
|
|
| 8.0×10-18 | 8.0×10-38 | 1.8×10-11 |
③
 有较强的氧化性,其还原产物是
有较强的氧化性,其还原产物是 ,回答下列问题:
,回答下列问题:(1)
 的电子式为
的电子式为(2)流程图中所发生的化学反应方程式为
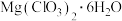 晶体的实验步骤依次为:①加热蒸发;②
晶体的实验步骤依次为:①加热蒸发;②
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某同学设计实验验证非金属元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。他设计了如图所示装置以验证氮、碳、硅元素的非金属性强弱。

该同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:A.___ B.____ C.___
(2)写出烧杯中发生反应的离子方程式:___ 。

该同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:A.
(2)写出烧杯中发生反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】下图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是师生对演示实验改进后的装置:
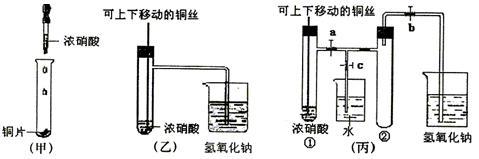
(1) 写出铜和浓硝酸反应的离子方程式________________________________ 。
(2)和甲装置相比,乙装置的优点有_________________________________________
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置,做实验时先关闭弹簧夹
_______ ,再打开弹簧夹___________ ,才能使NO2气体充满②试管。
(4)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管应如何操
作___________________________________________________________________________ 。
(5)②试管中的NO2和水充分反应后,所得溶液物质的量浓度的最大值是_______
(气体体积按标准状况计算)。

(1) 写出铜和浓硝酸反应的离子方程式
(2)和甲装置相比,乙装置的优点有
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置,做实验时先关闭弹簧夹
(4)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管应如何操
作
(5)②试管中的NO2和水充分反应后,所得溶液物质的量浓度的最大值是
(气体体积按标准状况计算)。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某实验小组在实验室中制取 并设计实验验证
并设计实验验证 的某些性质,请回答下列问题:
的某些性质,请回答下列问题:
(1)实验室利用图1制取 ,化学反应方程式为
,化学反应方程式为___________ ,其装置与制取___________ 的装置相同(填“ ”或“
”或“ ”或“
”或“ ”)。
”)。

(2)干燥 时应选用
时应选用___________ 。
(3)可以将 与灼热的CuO反应验证氨的还原性(如图2),现象为
与灼热的CuO反应验证氨的还原性(如图2),现象为___________ 。

(4)利用图3可验证 和HCl的有关性质(实验前a、b、c活塞均关闭):
和HCl的有关性质(实验前a、b、c活塞均关闭):

①若要在烧瓶II中产生“喷泉”现象,烧瓶I中不产生“喷泉”现象,其操作方法为___________ 。
②若先打开a、c活塞,在装置中可以观察到的现象是___________ 。
 并设计实验验证
并设计实验验证 的某些性质,请回答下列问题:
的某些性质,请回答下列问题:(1)实验室利用图1制取
 ,化学反应方程式为
,化学反应方程式为 ”或“
”或“ ”或“
”或“ ”)。
”)。
(2)干燥
 时应选用
时应选用(3)可以将
 与灼热的CuO反应验证氨的还原性(如图2),现象为
与灼热的CuO反应验证氨的还原性(如图2),现象为
(4)利用图3可验证
 和HCl的有关性质(实验前a、b、c活塞均关闭):
和HCl的有关性质(实验前a、b、c活塞均关闭):
①若要在烧瓶II中产生“喷泉”现象,烧瓶I中不产生“喷泉”现象,其操作方法为
②若先打开a、c活塞,在装置中可以观察到的现象是
您最近一年使用:0次



