按要求填空
(1)将含 的废水调至
的废水调至 为2~3,再加入
为2~3,再加入 溶液(转化为
溶液(转化为 ),该反应发生时,每
),该反应发生时,每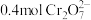 转移
转移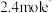 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是___________ (用离子方程式表示)。
(3) 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得: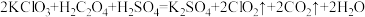 。产生
。产生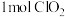 时,转移的电子的物质的量为
时,转移的电子的物质的量为___________ ;该反应中的氧化剂是___________ (填化学式)。
(1)将含
 的废水调至
的废水调至 为2~3,再加入
为2~3,再加入 溶液(转化为
溶液(转化为 ),该反应发生时,每
),该反应发生时,每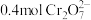 转移
转移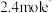 ,该反应的离子方程式为
,该反应的离子方程式为(2)生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是
(3)
 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得: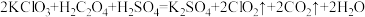 。产生
。产生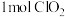 时,转移的电子的物质的量为
时,转移的电子的物质的量为
更新时间:2023-12-16 19:33:22
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某学生用Na2CO3和NaHCO3组成的均匀混合物进行以下实验。(气体体积已折算成标准状况下的体积,不考虑CO2在水中的溶解,不考虑HCl的挥发)
实验1:取2.96 g固体混合物加入质量分数为12.0%,密度为1.065 g/cm3的盐酸40 mL,共产生672 mL气体。
实验2:取8.88 g该固体化合物逐滴加入40 mL该盐酸,则产生a mL的气体。
(1)盐酸的物质的量浓度c(HCl)=___________ (保留两位小数)。
(2)样品中物质的量之比n(Na2CO3):n(NaHCO3)=___________ 。
(3)a=___________ mL。
实验1:取2.96 g固体混合物加入质量分数为12.0%,密度为1.065 g/cm3的盐酸40 mL,共产生672 mL气体。
实验2:取8.88 g该固体化合物逐滴加入40 mL该盐酸,则产生a mL的气体。
(1)盐酸的物质的量浓度c(HCl)=
(2)样品中物质的量之比n(Na2CO3):n(NaHCO3)=
(3)a=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(一)下列物质中:①漂白粉固体 ② 固体 ③
固体 ③ 固体 ④熔融
固体 ④熔融 ⑤食醋⑥
⑤食醋⑥ 片 ⑦
片 ⑦ ⑧盐酸 ⑨石墨 ⑩
⑧盐酸 ⑨石墨 ⑩ 葡萄糖(填序号)
葡萄糖(填序号)
(1)以上物质中属于强电解质且能导电的是___________________________ ;
(2)以上物质中属于非电解质的是___________________________ ;
(二)氨基钠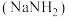 是有机合成中重要的还原剂.金属钠放入液氨中,沉入底部。一部分钠与液氨反应,并缓慢放出气泡;另一部分钠与液氨溶剂化,生成氨合钠离子
是有机合成中重要的还原剂.金属钠放入液氨中,沉入底部。一部分钠与液氨反应,并缓慢放出气泡;另一部分钠与液氨溶剂化,生成氨合钠离子 和蓝色的氨合电子
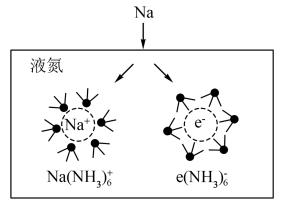
和蓝色的氨合电子 ,钠的溶剂化过程如图所示。
,钠的溶剂化过程如图所示。
(3)导电性:蓝色溶液____________ 液氨(填“>、<、=”)
(4)将 钠投入液氨中,得到
钠投入液氨中,得到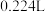 (标准状况下)
(标准状况下) ,与液氨反应产生
,与液氨反应产生 的钠和发生溶剂化作用的钠,两者物质的量之比为
的钠和发生溶剂化作用的钠,两者物质的量之比为______________ 。
(5)钠与液氨反应方程式为:________________________________________ 。
(一)下列物质中:①漂白粉固体 ②
 固体 ③
固体 ③ 固体 ④熔融
固体 ④熔融 ⑤食醋⑥
⑤食醋⑥ 片 ⑦
片 ⑦ ⑧盐酸 ⑨石墨 ⑩
⑧盐酸 ⑨石墨 ⑩ 葡萄糖(填序号)
葡萄糖(填序号)(1)以上物质中属于强电解质且能导电的是
(2)以上物质中属于非电解质的是
(二)氨基钠
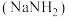 是有机合成中重要的还原剂.金属钠放入液氨中,沉入底部。一部分钠与液氨反应,并缓慢放出气泡;另一部分钠与液氨溶剂化,生成氨合钠离子
是有机合成中重要的还原剂.金属钠放入液氨中,沉入底部。一部分钠与液氨反应,并缓慢放出气泡;另一部分钠与液氨溶剂化,生成氨合钠离子 和蓝色的氨合电子
和蓝色的氨合电子 ,钠的溶剂化过程如图所示。
,钠的溶剂化过程如图所示。
(3)导电性:蓝色溶液
(4)将
 钠投入液氨中,得到
钠投入液氨中,得到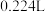 (标准状况下)
(标准状况下) ,与液氨反应产生
,与液氨反应产生 的钠和发生溶剂化作用的钠,两者物质的量之比为
的钠和发生溶剂化作用的钠,两者物质的量之比为(5)钠与液氨反应方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请按要求书写下列离子方程式:
(1)利用FeCl3溶液制备胶体的离子方程式为_______________________________ ;
(2)将过量的 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式________________________ 。
(3)FeSO4的酸性溶液与H2O2反应试写出该反应的离子方程式:____________________ ;
(4)氧化亚铜中加入稀硫酸____________________________ ;
(5)工业上用次氯酸钠和FeCl3在碱性条件下制备新型绿色消毒剂高铁酸钠(Na2FeO4)该反应的离子方程式是:______________________________ 。
(1)利用FeCl3溶液制备胶体的离子方程式为
(2)将过量的
 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式(3)FeSO4的酸性溶液与H2O2反应试写出该反应的离子方程式:
(4)氧化亚铜中加入稀硫酸
(5)工业上用次氯酸钠和FeCl3在碱性条件下制备新型绿色消毒剂高铁酸钠(Na2FeO4)该反应的离子方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
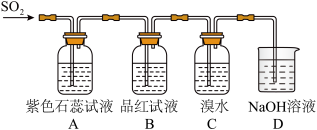
【推荐2】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:___________ 性。从硫元素化合价变化的角度分析,图中只有还原性的物质有___________ (填化学式)。
(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了___________ 。小登觉得可以设计实验验证这一推论,具体操作是___________ 。
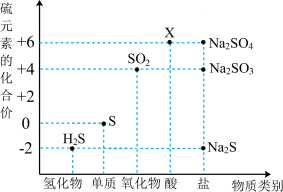
(3)配平下列反应:___________
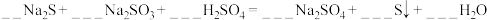 。
。
(4)如图是验证二氧化硫性质的实验装置。___________ (填序号,下同);B中___________ ;C中___________ 。D装置的作用是___________ 。
(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了
(3)配平下列反应:
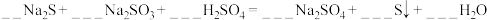 。
。(4)如图是验证二氧化硫性质的实验装置。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)实验室需要用NaOH配制0.2mol/LNaOH溶液450mL。
①完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、胶头滴管、____ 。
②配制该溶液需称取NaOH____ g。
③称量完毕,将药品倒入烧杯中,溶解、冷却,转移、洗涤。
(2)取上述配制的NaOH溶液200mL制取消毒液:向该NaOH溶液通入Cl2,使得NaOH恰好完全反应。完成下列填空。
①该消毒液制备的化学方程式为____ ,该反应消耗的Cl2在标准状况下的体积为____ 。
②该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。若将二者混合,每产生1molCl2,转移电子个数约为____ 。
(1)实验室需要用NaOH配制0.2mol/LNaOH溶液450mL。
①完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、胶头滴管、
②配制该溶液需称取NaOH
③称量完毕,将药品倒入烧杯中,溶解、冷却,转移、洗涤。
(2)取上述配制的NaOH溶液200mL制取消毒液:向该NaOH溶液通入Cl2,使得NaOH恰好完全反应。完成下列填空。
①该消毒液制备的化学方程式为
②该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。若将二者混合,每产生1molCl2,转移电子个数约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。如图为氯元素的“价-类”二维图。
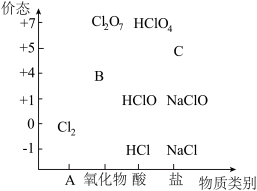
请回答下列问题:
(1)二维图中B可以代替 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是___________ (填化学式,下同);C是一种钠盐,则C是___________ 。
(2)某同学利用①FeO、② 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与________ (填序号)发生反应;从化合价角度看,盐酸中 具有
具有_________ 性,可能与(填序号)___________ 发生反应。
(3)若将84消毒液与双氧水混用给游泳池消毒,反应产生的 会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:
会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:___________ 。
(4)一定温度下, 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为___________ 。

请回答下列问题:
(1)二维图中B可以代替
 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是(2)某同学利用①FeO、②
 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与 具有
具有(3)若将84消毒液与双氧水混用给游泳池消毒,反应产生的
 会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:
会促进藻类快速生长,使池水变绿,写出反应的化学方程式并用单线桥法表示该反应电子转移的方向和数目:(4)一定温度下,
 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯及其化合物形式多样,用途广泛。回答下列问题:
(1)KClO4是一种白色粉末,其化学名称为_______ ;漂白粉的主要成分是_______ 。
(2)气体ClO2是应用较普遍的安全、无毒的消毒剂,可以用KClO3在稀H2SO4中和草酸反应制备,其化学方程式为_______ 。
(3)氨气可以检验输送氯气的管道是否泄漏,试写出化学反应方程式:_______ 。
(4)向200mLNaOH溶液中通入一定量Cl2恰好完全反应,得到0.1molNaClO3和0.1molNaClO,则原NaOH溶液的物质的量浓度为_______ 。
(1)KClO4是一种白色粉末,其化学名称为
(2)气体ClO2是应用较普遍的安全、无毒的消毒剂,可以用KClO3在稀H2SO4中和草酸反应制备,其化学方程式为
(3)氨气可以检验输送氯气的管道是否泄漏,试写出化学反应方程式:
(4)向200mLNaOH溶液中通入一定量Cl2恰好完全反应,得到0.1molNaClO3和0.1molNaClO,则原NaOH溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(1)该反应中氧化剂是___________ (填化学式,下同),在反应中___________ (填“得到”或“失去”电子,还原剂是___________ ,___________ 元素被氧化,还原产物为___________ 。
(2)用单线桥在方程式中标出电子转移情况:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O,___________ 。
(3)当反应中有1个 离子生成时,转移的电子数是
离子生成时,转移的电子数是___________ 个。
(1)该反应中氧化剂是
(2)用单线桥在方程式中标出电子转移情况:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O,
(3)当反应中有1个
 离子生成时,转移的电子数是
离子生成时,转移的电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。
(1)X的化学式是___________ 。
(2)用双线桥法标出,上述反应中电子转移的方向和数目___________ 。
(3)上述反应中的还原剂为___________ (填化学式),被还原的元素是___________ (填元素符号)。
(4)向酸性 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是___________ ,反应后溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)0.2mol 参加上述反应,转移电子
参加上述反应,转移电子___________ mol。
 在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。(1)X的化学式是
(2)用双线桥法标出,上述反应中电子转移的方向和数目
(3)上述反应中的还原剂为
(4)向酸性
 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是(5)0.2mol
 参加上述反应,转移电子
参加上述反应,转移电子
您最近一年使用:0次
【推荐3】钒性能优良,用途广泛,有“金属维生素”之称。完成下列填空:
(1)将废钒催化剂(主要成分为V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是______ 。
(2)向上述所得溶液中加入KClO3溶液,完善并配平反应的离子方程式:______ 。
 ClO
ClO +
+ VO2++
VO2++ ______=
______= Cl-+
Cl-+ VO
VO +
+ ______。
______。
(3)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应从而被吸收,则SO 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是______ 。
(4)在20.00mLc(VO )=0.1mol•L-1的溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
)=0.1mol•L-1的溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是______ (填标号)。
a.VO2+ b.V2+ c.V
(1)将废钒催化剂(主要成分为V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是
(2)向上述所得溶液中加入KClO3溶液,完善并配平反应的离子方程式:
 ClO
ClO +
+ VO2++
VO2++ ______=
______= Cl-+
Cl-+ VO
VO +
+ ______。
______。(3)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应从而被吸收,则SO
 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是(4)在20.00mLc(VO
 )=0.1mol•L-1的溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
)=0.1mol•L-1的溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是a.VO2+ b.V2+ c.V
您最近一年使用:0次

 被溶液中
被溶液中

