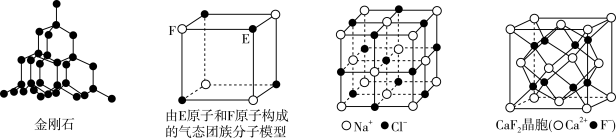
X、Y、Z、Q、W是原子序数依次增大的前四周期元素,X、Z的基态原子2p能级上各有两个未成对电子,Y与Q同主族,W原子N能层只有一个电子,其余能层全充满。下列说法错误的是


| A.电负性为Z>Y>X |
| B.原子半径为r(Q)>r(Y)>r(Z) |
| C.X与Z可以形成含极性键的极性分子 |
| D.W与Z形成的化合物晶胞如图,其化学式为WZ |
2023高三·全国·专题练习 查看更多[2]
更新时间:2023-12-15 19:12:14
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列有关说法正确的是
| A.电子云通常用小点的疏密来表示,小点密表示在该空间的电子数多 |
| B.Se的基态原子电子排布为[Ar]4s24p4 |
C.Cu的核外电子排布式为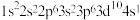 ,所以Cu位于s区 ,所以Cu位于s区 |
| D.原子光谱的特征谱线用于鉴定元素,从1s22s22p33s1跃迁至1s22s22p4时释放能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关描述正确的是
| A.熔点: F2>Cl2>Br2>I2 |
| B.无机含氧酸的酸性:H2SO3 <H2SO4 < HClO4 |
| C.CS2和NO2互为等电子体 |
| D.基态Cr原子的价电子排布式:3d44s2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
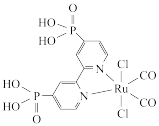
【推荐1】近年来,光催化剂的研究是材料领域的热点。一种Ru配合物(如图所示)复合光催化剂可将 转化为HCOOH。下列说法
转化为HCOOH。下列说法错误 的是
 转化为HCOOH。下列说法
转化为HCOOH。下列说法
| A.Ru配合物中第二周期元素的电负性:O>N>C |
B.吡啶(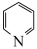 ,原子在同一平面)中C、N原子的杂化方式分别为 ,原子在同一平面)中C、N原子的杂化方式分别为 、 、 |
| C.该配合物中Ru的配位数是6 |
D. 中P的价层电子对数为4,空间结构为正四面体形 中P的价层电子对数为4,空间结构为正四面体形 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】现有三种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是
| A.第一电离能:③>②>① |
| B.原子半径:③>②>① |
| C.电负性:③>②>① |
| D.最高正化合价:③>②>① |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.非极性分子中的原子上一定不含孤电子对 |
| B.平面三角形分子一定是非极性分子 |
| C.二氯甲烷(CH2Cl2)分子的中心原子采取sp3杂化,键角均为109°28′ |
| D.ABn型分子的中心原子最外层满足8电子结构,则ABn不一定是非极性分子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】有X、Y、Z、Q、T五种元素。X原子M层上有2个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )
| A.元素Y和Q可形成化合物Y2Q3 | B.T和Z各有一种单质的空间构型为正四面体形 |
| C.X和Q结合生成的化合物可形成离子晶体 | D.ZQ2是极性键构成的非极性分子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】化合物硼化镁超导转变温度高达39 K,该金属间化合物的晶体结构如图:则它的化学式为


| A.MgB | B.Mg2B |
| C.MgB2 | D.Mg2B3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】铁有δ、γ、α三种同素异形体,其晶胞结构如图所示,下列判断正确的是


| A.δ、γ、α铁晶体中存在金属阳离子和阴离子 |
B. 晶胞中所含有的铁原子数为9 晶胞中所含有的铁原子数为9 |
| C.δ、α两种晶胞中铁原子周围等距离且最近的铁原子个数之比为3∶1 |
D.若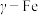 晶胞棱长为acm, 晶胞棱长为acm, 晶胞棱长为bcm,则两种晶体的密度比为 晶胞棱长为bcm,则两种晶体的密度比为 |
您最近一年使用:0次

 、
、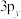 、
、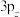 三个轨道相互垂直,能量相等
三个轨道相互垂直,能量相等 )中
)中 的设想,置换过程如图所示,下列说法错误的是
的设想,置换过程如图所示,下列说法错误的是