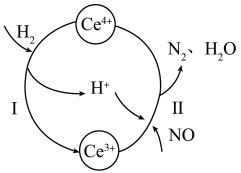
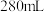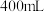还原法可以将硝酸厂烟气中的大量氮氧化物转化为无害物质。常温下,将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,转化过程如图所示。下列说法错误的是

| A.反应过程中4gH2能转化30gNO |
| B.反应II中氧化剂与还原剂的个数比为1:2 |
C.反应I的离子方程式为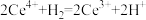 |
| D.反应过程中溶液内Ce3+和Ce4+总数保持不变 |
更新时间:2023-12-04 17:34:56
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3→K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
| A.生成42.0LN2(标准状况) |
| B.有0.250molKNO3被氧化 |
| C.转移电子的物质的量为2.25mol |
| D.被氧化的N原子的物质的量为3.75mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 是精细磷化工产品。工业制备原理如下:
是精细磷化工产品。工业制备原理如下:
(I)
(II)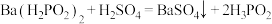
下列说法错误 的是
 是精细磷化工产品。工业制备原理如下:
是精细磷化工产品。工业制备原理如下:(I)

(II)
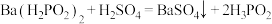
下列说法
A. 中P元素的化合价为 中P元素的化合价为 |
B.反应(I)氧化剂与还原剂的质量之比为 |
| C.反应(I)是氧化还原反应,反应(II)是非氧化还原反应 |
D.标准状况下生成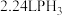 ,同时转移 ,同时转移 电子 电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知反应:
①SO2+2Fe3++2H2O→SO42-+2Fe2++W
②Cr2O72-+aFe2++bH+→Cr3++Fe3++H2O
下列有关说法正确的 ( )
①SO2+2Fe3++2H2O→SO42-+2Fe2++W
②Cr2O72-+aFe2++bH+→Cr3++Fe3++H2O
下列有关说法正确的 ( )
| A.还原性: Cr3+>SO2 |
| B.方程式②中, a=6, b=7 |
| C.Cr2O72-能将 Na2SO3氧化成 Na2SO4 |
| D.方程式①中 W 为 OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氨基钟 是一种化工原料,实验室可用氨气和钠反应制得,某化学实验小组用如图装置制备氨基钠(部分夹持仪器已略去)。
是一种化工原料,实验室可用氨气和钠反应制得,某化学实验小组用如图装置制备氨基钠(部分夹持仪器已略去)。
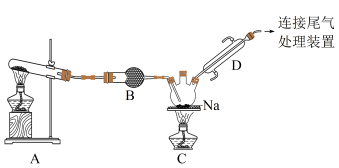
已知:常温下,氨基钠为白色晶体,熔点为210℃,沸点为400℃,露置于空气中易吸收水分而失效。下列说法正确的是
 是一种化工原料,实验室可用氨气和钠反应制得,某化学实验小组用如图装置制备氨基钠(部分夹持仪器已略去)。
是一种化工原料,实验室可用氨气和钠反应制得,某化学实验小组用如图装置制备氨基钠(部分夹持仪器已略去)。
已知:常温下,氨基钠为白色晶体,熔点为210℃,沸点为400℃,露置于空气中易吸收水分而失效。下列说法正确的是
| A.装置A中的试剂为氯化铵 |
| B.实验时,应同时点燃装置A处和装置C处的酒精灯 |
C.装置C中发生反应的化学方程式为 |
| D.连接尾气处理装置时,须防止空气中的水蒸气进入 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】Bi为第VA族元素,铋酸钠是分析化学中的重要试剂,不溶于冷水。测定NaBiO3粗产品纯度的步骤如下:①将NaBiO3粗产品加入足量稀硫酸和稀MnSO4溶液中,充分反应后,溶液变为紫红色,同时生成Bi3+;②向①中反应后的溶液中滴加一定浓度的草酸(H2C2O4)标准溶液,通过消耗草酸标准溶液的体积计算产品纯度。下列有关说法正确的
A.BiO 的空间结构为三角锥形 的空间结构为三角锥形 |
| B.草酸分子中σ键与π键个数之比为3:1 |
C.步骤①中反应的离子方程式为5BiO +2Mn2++14H+=5Bi3++2MnO +2Mn2++14H+=5Bi3++2MnO +7H2O +7H2O |
| D.步骤②中反应的氧化产物和还原产物的物质的量之比为5:1 |
您最近一年使用:0次
【推荐1】某容器中发生一个化学反应,反应过程中存在Fe2+、 、Fe3+、
、Fe3+、 、H+和H2O六种粒子,在反应过程中测得Fe3+、
、H+和H2O六种粒子,在反应过程中测得Fe3+、 的质量分数(W)随时间变化的曲线如图所示,下列有关判断中错误的是
的质量分数(W)随时间变化的曲线如图所示,下列有关判断中错误的是

 、Fe3+、
、Fe3+、 、H+和H2O六种粒子,在反应过程中测得Fe3+、
、H+和H2O六种粒子,在反应过程中测得Fe3+、 的质量分数(W)随时间变化的曲线如图所示,下列有关判断中错误的是
的质量分数(W)随时间变化的曲线如图所示,下列有关判断中错误的是
A.在反应中 被还原,发生还原反应 被还原,发生还原反应 |
B.还原性: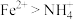 |
| C.该反应中Fe2+被还原为Fe3+ |
| D.在反应中参加反应的还原剂与氧化剂的物质的量之比为8:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】NaOH溶液可用于实验室制取Cl2时的尾气处理。某次实验结束后,发现溶液中的NaOH完全被消耗,溶液中的阴离子只有Cl-、ClO-、ClO ,且ClO-和ClO
,且ClO-和ClO 的微粒个数之比为1:1,则被氧化的氯原子和被还原的氯原子的质量之比为
的微粒个数之比为1:1,则被氧化的氯原子和被还原的氯原子的质量之比为
 ,且ClO-和ClO
,且ClO-和ClO 的微粒个数之比为1:1,则被氧化的氯原子和被还原的氯原子的质量之比为
的微粒个数之比为1:1,则被氧化的氯原子和被还原的氯原子的质量之比为| A.1:1 | B.1:2 | C.1:3 | D.1:4 |
您最近一年使用:0次

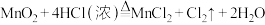 中,氧化剂和还原剂个数之比为1:4
中,氧化剂和还原剂个数之比为1:4 中,被氧化和被还原的氮个数之比为1:2
中,被氧化和被还原的氮个数之比为1:2 中,氧化产物和还原产物个数之比为3:1
中,氧化产物和还原产物个数之比为3:1 中,发生氧化反应和还原反应的氮个数之比为5:3
中,发生氧化反应和还原反应的氮个数之比为5:3 和
和 混合固体投入至
混合固体投入至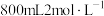 的稀硝酸溶液中,充分反应后无固体剩余,反应过程中只生成
的稀硝酸溶液中,充分反应后无固体剩余,反应过程中只生成 气体,向反应后溶液中滴加
气体,向反应后溶液中滴加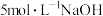 溶液至金属离子恰好完全沉淀时,所加
溶液至金属离子恰好完全沉淀时,所加 溶液的体积为
溶液的体积为