一碳化学是以分子中只含一个碳原子的化合物为原料生产化工产品的方法。合成气( 和
和 的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
I:
II:
III:
(1)当反应I达到平衡后,下列措施可提高正反应速率的是_______(填标号)。
(2)若在恒温恒容容器中仅发生反应II,则下列能说明反应达到平衡状态的是_______。
(3)向容积为 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应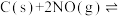
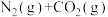 ,
, 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。
① 内,以
内,以 表示的该反应速率
表示的该反应速率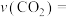
___________ ,最终达平衡时 的转化率
的转化率
___________ ,该温度 ℃下的平衡常数
℃下的平衡常数
___________ 。
②保持温度 ℃不变,向该
℃不变,向该 密闭容器中加入该四种反应混合物各
密闭容器中加入该四种反应混合物各 ,该时刻,正、逆反应速率的大小关系为:
,该时刻,正、逆反应速率的大小关系为: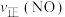
___________ 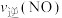 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)已知4CO(g) +2NO2(g) 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行。
 和
和 的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:I:

II:

III:

(1)当反应I达到平衡后,下列措施可提高正反应速率的是_______(填标号)。
| A.加入焦炭 | B.通入CO | C.升高温度 | D.分离出氢气 |
| A.容器内气体的压强不变 |
| B.容器内气体的总质量不变 |
| C.容器内气体的平均相对分子质量不变 |
D.单位时间内,每有2 mol  键断裂,同时有1 mol 键断裂,同时有1 mol  键断裂 键断裂 |
 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应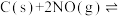
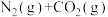 ,
, 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。| 条件 | 保持温度为 /℃ /℃ | ||||||
| 时间 | 0 | 5min | 10min | 15min | 20min | 25min | 30min |
 物质的量 物质的量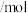 | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
 物质的量 物质的量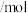 | 0 | 0.3 | 0.50 | 0.65 | 0.75 | 0.80 | 0.80 |
 内,以
内,以 表示的该反应速率
表示的该反应速率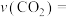
 的转化率
的转化率
 ℃下的平衡常数
℃下的平衡常数
②保持温度
 ℃不变,向该
℃不变,向该 密闭容器中加入该四种反应混合物各
密闭容器中加入该四种反应混合物各 ,该时刻,正、逆反应速率的大小关系为:
,该时刻,正、逆反应速率的大小关系为: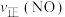
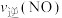 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)已知4CO(g) +2NO2(g)
 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
更新时间:2023/12/14 21:00:53
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】含铁化合物是重要的基础材料。
请问答:
(1)已知: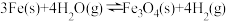
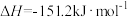 ,
,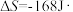
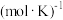 。
。 。当
。当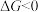 时,正反应是自发的,此时的逆转温度为
时,正反应是自发的,此时的逆转温度为___________ K。
(2)高炉炼铁中发生的基本反应之一为:

①在1100℃时,K=0.263,若此时测得高炉中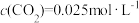 ,
,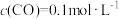 ,判断反应速率
,判断反应速率 (正)
(正)___________  (逆),理由是
(逆),理由是___________ 。
②下列说法不正确的是___________ 。
A.须采用高温高压的反应条件使FeO还原为
B.粉碎FeO能增大接触面积从而提高反应速率
C.平衡时提高CO气体的分压有利于提高Fe的产量
D.加入CaCO3(s)后因分解产生CO2必使平衡逆向移动
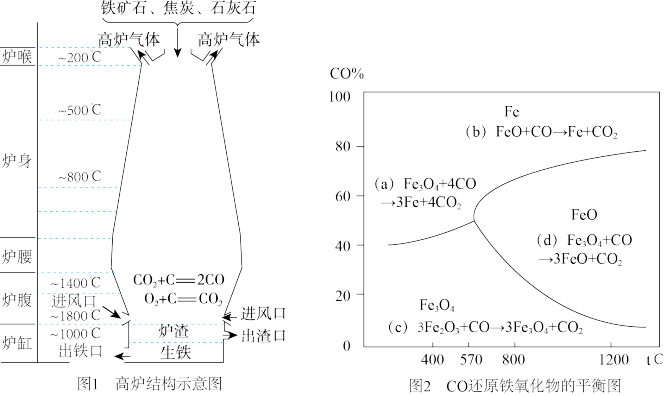
③高炉炉体结构如图1所示,以铁矿石、焦炭、石灰石和空气为原料,由图2推测炉腹中发生的主要反应是___________ (选填:a、b、c、d)。
④若将体积比为1:1的CO和H2混合煤气通入进风口,测得不同温度下FeO还原到 后,还原剂剩余的物质的量n值如下:
后,还原剂剩余的物质的量n值如下:
请结合表格中的数据说明CO和H2分别还原FeO的倾向性大小是___________ 。
(3)一定条件下,FeCl2或FeCl3都可以催化分解H2O2。总反应都是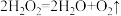 。请写出用FeCl3催化的离子方程式。①
。请写出用FeCl3催化的离子方程式。①___________ ;②___________ 。
请问答:
(1)已知:
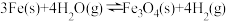
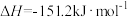 ,
,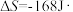
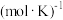 。
。 。当
。当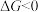 时,正反应是自发的,此时的逆转温度为
时,正反应是自发的,此时的逆转温度为(2)高炉炼铁中发生的基本反应之一为:


①在1100℃时,K=0.263,若此时测得高炉中
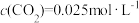 ,
,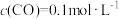 ,判断反应速率
,判断反应速率 (正)
(正) (逆),理由是
(逆),理由是②下列说法不正确的是
A.须采用高温高压的反应条件使FeO还原为

B.粉碎FeO能增大接触面积从而提高反应速率
C.平衡时提高CO气体的分压有利于提高Fe的产量
D.加入CaCO3(s)后因分解产生CO2必使平衡逆向移动
③高炉炉体结构如图1所示,以铁矿石、焦炭、石灰石和空气为原料,由图2推测炉腹中发生的主要反应是

④若将体积比为1:1的CO和H2混合煤气通入进风口,测得不同温度下FeO还原到
 后,还原剂剩余的物质的量n值如下:
后,还原剂剩余的物质的量n值如下:| 还原剂 | 600℃ | 700℃ | 800℃ | 900℃ | 1000℃ | 1100℃ | 1200℃ |
| H2 | 4.18 | 3.34 | 2.94 | 2.60 | 2.32 | 2.30 | 2.25 |
| CO | 1.66 | 2.50 | 2.90 | 3.24 | 3.52 | 3.54 | 3.59 |
请结合表格中的数据说明CO和H2分别还原FeO的倾向性大小是
(3)一定条件下,FeCl2或FeCl3都可以催化分解H2O2。总反应都是
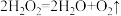 。请写出用FeCl3催化的离子方程式。①
。请写出用FeCl3催化的离子方程式。①
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】二甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效,具有优良的环保性能。也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。请填写下列空白:
(1)二甲醚的核磁共振氢谱图中有_______ 个吸收峰,官能团名称是____________ 。
(2)二甲醚的同分异构体A与浓硫酸混合,加热到170℃时生成有机物B:
①写出A的官能团电子式为__________ ;B与溴水反应生成的物质名称为___________ ;
②德国化学家第尔斯和他的学生阿尔德首次发现和记载一种新型反应而获得1950年诺贝尔化学奖,该反应是一种环加成反应:凡含有双键或三键的不饱和化合物,可以和链状或环状含共轭双烯体系发生1,4加成反应,通常生成一个六元环,该反应条件温和,产率很高,是有机化学合成反应中非常重要的碳碳键形成的手段之一,也是现代有机合成里常用的反应之一请根据以上信息写出2-甲基-1,3-丁二烯(含共轭双烯体系)与B反应化学方程式______________________________________ 。
(3)二甲醚、空气、氢氧化钾溶液、多孔石墨电极构成燃料电池,则负极电极反应式是______ 。
(4)反应2CH3OH(g) CH3OCH3(g) + H2O(g)某温度下的平衡常数为225 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为225 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
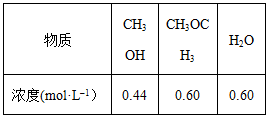
①比较此时正、逆反应速率的大小:v(正)______ v(逆)(填“>”、“<”或“=”);
②若开始只加入CH3OH,经10min后反应达到平衡,计算达到平衡时CH3OH转化率 α(CH3OH)=______ (计算结果用百分数表示,保留小数后一位)。
(1)二甲醚的核磁共振氢谱图中有
(2)二甲醚的同分异构体A与浓硫酸混合,加热到170℃时生成有机物B:
①写出A的官能团电子式为
②德国化学家第尔斯和他的学生阿尔德首次发现和记载一种新型反应而获得1950年诺贝尔化学奖,该反应是一种环加成反应:凡含有双键或三键的不饱和化合物,可以和链状或环状含共轭双烯体系发生1,4加成反应,通常生成一个六元环,该反应条件温和,产率很高,是有机化学合成反应中非常重要的碳碳键形成的手段之一,也是现代有机合成里常用的反应之一请根据以上信息写出2-甲基-1,3-丁二烯(含共轭双烯体系)与B反应化学方程式
(3)二甲醚、空气、氢氧化钾溶液、多孔石墨电极构成燃料电池,则负极电极反应式是
(4)反应2CH3OH(g)
 CH3OCH3(g) + H2O(g)某温度下的平衡常数为225 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为225 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v(正)
②若开始只加入CH3OH,经10min后反应达到平衡,计算达到平衡时CH3OH转化率 α(CH3OH)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在高温高压下 具有极高的化学活性,能与多种单质或化合物反应。
具有极高的化学活性,能与多种单质或化合物反应。
(1)若在恒温恒容的容器内进行反应:

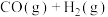 ,则可用来判断该反应达到平衡状态的标志有
,则可用来判断该反应达到平衡状态的标志有_______  填字母
填字母 。
。
a.容器内的压强保持不变 b.容器中 的浓度与
的浓度与 的浓度相等
的浓度相等
c.容器中混合气体的密度保持不变 d. 的生成速率与
的生成速率与 的生成速率相等
的生成速率相等
(2)一定条件下,反应的化学方程式为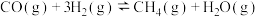 。
。
①一定条件下,该反应能够自发进行的原因是_______ 。
②已知 、
、 和
和  的燃烧热分别为
的燃烧热分别为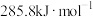 、
、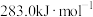 和
和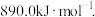 写出
写出  与
与 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:_______ 。
 具有极高的化学活性,能与多种单质或化合物反应。
具有极高的化学活性,能与多种单质或化合物反应。(1)若在恒温恒容的容器内进行反应:


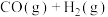 ,则可用来判断该反应达到平衡状态的标志有
,则可用来判断该反应达到平衡状态的标志有 填字母
填字母 。
。a.容器内的压强保持不变 b.容器中
 的浓度与
的浓度与 的浓度相等
的浓度相等c.容器中混合气体的密度保持不变 d.
 的生成速率与
的生成速率与 的生成速率相等
的生成速率相等(2)一定条件下,反应的化学方程式为
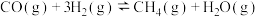 。
。①一定条件下,该反应能够自发进行的原因是
②已知
 、
、 和
和  的燃烧热分别为
的燃烧热分别为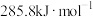 、
、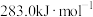 和
和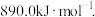 写出
写出  与
与 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在化学反应的研究和实际应用中,人们除了选择合适的化学反应以实现新期特的物质转化或能量转化,还要关注化学反应进行的快慢和程度,以提高生产效率。
(1)控制条件,让反应在恒容密闭容器中进行如下反应: 。用传感器测得不同时间NO和CO的浓度如表。
。用传感器测得不同时间NO和CO的浓度如表。
前2s内的平均反应速率
___________ ,从表格看,已达化学平衡的时间段为:___________ 。
(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的 气体后,发生反应
气体后,发生反应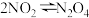 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。反应速率(v)与时间(t)的关系曲线。
是无色气体。反应速率(v)与时间(t)的关系曲线。
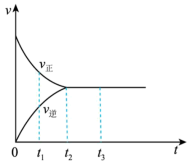
下列叙述正确的是___________ 。
a. 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小
b. 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行
c. 各物质浓度不再变化
各物质浓度不再变化
d. 各物质浓度相等
各物质浓度相等
e. ,
, 浓度增大
浓度增大
f.反应过程中气体的颜色不变
(3)在压强为 条件下,
条件下, 与
与 的混合气体在催化剂作用下能自发放热反应生成甲醇:
的混合气体在催化剂作用下能自发放热反应生成甲醇: 。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
___________ ,
___________ 。
(4)比较相同浓度的 溶液和不同浓度的
溶液和不同浓度的 溶液反应的反应快慢可通过测定
溶液反应的反应快慢可通过测定___________ 来实现。
(5)在四个不同的容器中,在不同的条件下进行合成氨反应: 根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
(1)控制条件,让反应在恒容密闭容器中进行如下反应:
 。用传感器测得不同时间NO和CO的浓度如表。
。用传感器测得不同时间NO和CO的浓度如表。时间 | 0 | 1 | 2 | 3 | 4 | 5 |
 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的
 气体后,发生反应
气体后,发生反应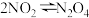 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。反应速率(v)与时间(t)的关系曲线。
是无色气体。反应速率(v)与时间(t)的关系曲线。
下列叙述正确的是
a.
 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小b.
 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行c.
 各物质浓度不再变化
各物质浓度不再变化 d.
 各物质浓度相等
各物质浓度相等e.
 ,
, 浓度增大
浓度增大 f.反应过程中气体的颜色不变
(3)在压强为
 条件下,
条件下, 与
与 的混合气体在催化剂作用下能自发放热反应生成甲醇:
的混合气体在催化剂作用下能自发放热反应生成甲醇: 。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:

| 实验编号 |  (℃) (℃) |  |  |
| ① | 180 |  | 0.1 |
| ② |  |  | 5 |
| ③ | 350 |  | 5 |
 溶液和不同浓度的
溶液和不同浓度的 溶液反应的反应快慢可通过测定
溶液反应的反应快慢可通过测定(5)在四个不同的容器中,在不同的条件下进行合成氨反应:
 根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________A. | B. |
C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】尿素(H2NCONH2)是一种非常重要的高氮化肥,在工农业生产中有着非常重要的地位。合成尿素的第一步反应为:2NH3(g)+CO2(g) H2NCOONH4(氨基甲酸铵)(l) △H1,若加入恒温、恒容容器中的NH3和CO2的物质的量之比为2:1,能说明反应达到化学平衡状态的是
H2NCOONH4(氨基甲酸铵)(l) △H1,若加入恒温、恒容容器中的NH3和CO2的物质的量之比为2:1,能说明反应达到化学平衡状态的是________ 。
a.CO2的浓度不再变化 b.NH3的百分含量不再变化
c.容器内气体的密度不再变化 d.混合气体的平均相对分子质量不再变化
e.2v(NH3)正=v(CO2)逆
 H2NCOONH4(氨基甲酸铵)(l) △H1,若加入恒温、恒容容器中的NH3和CO2的物质的量之比为2:1,能说明反应达到化学平衡状态的是
H2NCOONH4(氨基甲酸铵)(l) △H1,若加入恒温、恒容容器中的NH3和CO2的物质的量之比为2:1,能说明反应达到化学平衡状态的是a.CO2的浓度不再变化 b.NH3的百分含量不再变化
c.容器内气体的密度不再变化 d.混合气体的平均相对分子质量不再变化
e.2v(NH3)正=v(CO2)逆
您最近一年使用:0次
【推荐1】工业废气、汽车尾气排放出的 SO2、NOx等,是形成雾霾的重要因素.霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾.
(1)NOx和 SO2在空气中存在下列平衡:
2NO(g) + O2(g) 2NO2(g) △ H =− 113.0kJ
2NO2(g) △ H =− 113.0kJ mol−1
mol−1
2SO2(g) + O2(g) 2SO3(g) △ H =− 196.6kJ
2SO3(g) △ H =− 196.6kJ mol−1
mol−1
SO2通常在二氧化氮的存在下,进一步被氧化,生成 SO3.
①写出 NO2和 SO2反应的热化学方程式为_____ .
②随温度升高,该反应化学平衡常数变化趋势是_____ .
(2)提高2SO2(g) + O2(g) 2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是
2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是_____ .②在①中条件下,反应达到平衡后,改变下列条件,能使 SO2的转化率提高的是_____ (填字母).
a.温度和容器体积不变,充入 1.0mol He
b.温度和容器体积不变,充入 1.0mol O2
c.在其他条件不变时,减少容器的体积
d.在其他条件不变时,改用高效催化剂
e.在其他条件不变时,升高体系温度

(3)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图
①用溶液A吸收含二氧化硫的废气,其反应的离子方程式是_____ .
②用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是_____ .
(1)NOx和 SO2在空气中存在下列平衡:
2NO(g) + O2(g)
 2NO2(g) △ H =− 113.0kJ
2NO2(g) △ H =− 113.0kJ mol−1
mol−12SO2(g) + O2(g)
 2SO3(g) △ H =− 196.6kJ
2SO3(g) △ H =− 196.6kJ mol−1
mol−1SO2通常在二氧化氮的存在下,进一步被氧化,生成 SO3.
①写出 NO2和 SO2反应的热化学方程式为
②随温度升高,该反应化学平衡常数变化趋势是
(2)提高2SO2(g) + O2(g)
 2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是
2SO3(g)反应中 SO2的转化率,是减少 SO2排放的有效措施:①T 温度时,在 1L 的密闭容器中加入 2.0mol SO2和 1.0mol O2,5min 后反应达到平衡,二氧化硫的转化率为 50%,该反应的平衡常数是a.温度和容器体积不变,充入 1.0mol He
b.温度和容器体积不变,充入 1.0mol O2
c.在其他条件不变时,减少容器的体积
d.在其他条件不变时,改用高效催化剂
e.在其他条件不变时,升高体系温度

(3)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图
①用溶液A吸收含二氧化硫的废气,其反应的离子方程式是
②用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是
您最近一年使用:0次
【推荐2】常温下,在1L的密闭恒容容器中,A(s)、B(g)、C(g)、D (g) 4种物质的物质的量随时间的变化情况如下图所示,其中B(g)为黄色气体,C(g)、D(g)为无色气体。根据要求回答下列问题:
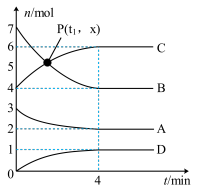
(1)在0 - 4min内,用C表示的化学反应速率v(C)=__________ 。
(2)写出所发生反应的化学方程式:___________ 物质后注明物质状态)。
(3)下列措施能提高上述化学反应速率的是___________ 。
a.升高反应温度 b.冲入氩气来增大压强 c. 加入2mol A d.加入1molB
(4)下列描述中能表明该反应达到平衡的有__________ 。
a.气体的总物质的量不再变化 b.混合气体的颜色不在变化
c. 混合气体的平均摩尔质量不再变化 d. 2v(B)=3v(C)
(5)提高B(g)的转化率的措施有____________________ (任写1条)。
(6)p点对应的物质的量的数值x =__________ ,该反应的平衡常数K=__________ 。

(1)在0 - 4min内,用C表示的化学反应速率v(C)=
(2)写出所发生反应的化学方程式:
(3)下列措施能提高上述化学反应速率的是
a.升高反应温度 b.冲入氩气来增大压强 c. 加入2mol A d.加入1molB
(4)下列描述中能表明该反应达到平衡的有
a.气体的总物质的量不再变化 b.混合气体的颜色不在变化
c. 混合气体的平均摩尔质量不再变化 d. 2v(B)=3v(C)
(5)提高B(g)的转化率的措施有
(6)p点对应的物质的量的数值x =
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)已知NO2和N2O4可以相互转化:2NO2(g) N2O4 (g) ΔH= -57.2k/mol。
N2O4 (g) ΔH= -57.2k/mol。
i.此反应自发进行的条件是___________ (填“低温”、“高温”或“任意温度”) 。
ii.一定温度下,现将1 molN2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是___________ (填序号,下同)。
① ②
②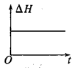 ③
③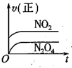 ④
④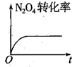
ⅲ.若反应2NO2 (g) N2O4 (g)在体积为1L的恒容密闭容器中进行,保持温度不变,达到平衡后,向反应容器中再充入少量N2O4,平衡向
N2O4 (g)在体积为1L的恒容密闭容器中进行,保持温度不变,达到平衡后,向反应容器中再充入少量N2O4,平衡向___________ 移动(填“左”、“右”或“不”),重新平衡后和原平衡相比,混合气体颜色___________ (填“变深”“变浅”或“不变”),N2O4的体积分数___________ (填“增大”、“减小”或“不变”)。
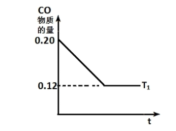
(2)i.温度为T1时,向2L密闭容器中通入0.20 mol CO和0.40 molH2,发生反应CO(g)+2H2(g) CH3OH(g ) ΔH2<0,CO的物质的量与时间的关系如图所示,则该温度时反应的平衡常数K=
CH3OH(g ) ΔH2<0,CO的物质的量与时间的关系如图所示,则该温度时反应的平衡常数K= ___________ ;
ii.已知温度T2>T1,请在原图上画出在温度T2时反应过程中CO的物质的量与时间的关系图________ 。
 N2O4 (g) ΔH= -57.2k/mol。
N2O4 (g) ΔH= -57.2k/mol。i.此反应自发进行的条件是
ii.一定温度下,现将1 molN2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
①
 ②
② ③
③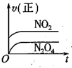 ④
④
ⅲ.若反应2NO2 (g)
 N2O4 (g)在体积为1L的恒容密闭容器中进行,保持温度不变,达到平衡后,向反应容器中再充入少量N2O4,平衡向
N2O4 (g)在体积为1L的恒容密闭容器中进行,保持温度不变,达到平衡后,向反应容器中再充入少量N2O4,平衡向(2)i.温度为T1时,向2L密闭容器中通入0.20 mol CO和0.40 molH2,发生反应CO(g)+2H2(g)
 CH3OH(g ) ΔH2<0,CO的物质的量与时间的关系如图所示,则该温度时反应的平衡常数K=
CH3OH(g ) ΔH2<0,CO的物质的量与时间的关系如图所示,则该温度时反应的平衡常数K= ii.已知温度T2>T1,请在原图上画出在温度T2时反应过程中CO的物质的量与时间的关系图

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】尿素(NH2CONH2)又称碳酰胺,是含氮量最高的氮肥。工业上利用二氧化碳和氨气在一定条件下合成尿素,涉及的反应如下:
反应I:2NH3(g)+ CO2(g) H2NCOONH4(s)(氨基甲酸铵) ΔH1 = -272kJ·mol-1
H2NCOONH4(s)(氨基甲酸铵) ΔH1 = -272kJ·mol-1
反应II:H2NCOONH4(s) NH2CONH2(s)+ H2O(g) ΔH2 = +138kJ·mol-1
NH2CONH2(s)+ H2O(g) ΔH2 = +138kJ·mol-1
请回答:
(1)写出二氧化碳和氨气合成尿素的总热化学方程式_______ ,该反应自发进行的条件是_______ (填“低温”、“高温”或“任意条件”)。
(2)尿素(NH2CONH2)是一种重要的化工产品,有很多用途。化工生产中利用尿素溶液可吸收尾气中的氯气,生成两种无污染气体,其中一种气体是空气的主要成分,且溶液pH明显降低,该反应的化学方程式_______ 。
(3)合成氨工业先驱哈伯(P·Haber)利用N2和H2在Fe催化作用下最早人工合成氨气,该反应为: N2(g)+ 3H2(g) 2NH3(g) ΔH = -92.4 kJ·mol-1
2NH3(g) ΔH = -92.4 kJ·mol-1
①写出该反应的平衡常数表达式K =_______ 。
②关于合成氨工艺的下列理解,正确的是_______ 。
A.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
B.降低温度能使平衡向正反应方向进行且平衡常数不变
C.合成氨反应在不同温度下的ΔH和ΔS都小于零
D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
反应I:2NH3(g)+ CO2(g)
 H2NCOONH4(s)(氨基甲酸铵) ΔH1 = -272kJ·mol-1
H2NCOONH4(s)(氨基甲酸铵) ΔH1 = -272kJ·mol-1反应II:H2NCOONH4(s)
 NH2CONH2(s)+ H2O(g) ΔH2 = +138kJ·mol-1
NH2CONH2(s)+ H2O(g) ΔH2 = +138kJ·mol-1请回答:
(1)写出二氧化碳和氨气合成尿素的总热化学方程式
(2)尿素(NH2CONH2)是一种重要的化工产品,有很多用途。化工生产中利用尿素溶液可吸收尾气中的氯气,生成两种无污染气体,其中一种气体是空气的主要成分,且溶液pH明显降低,该反应的化学方程式
(3)合成氨工业先驱哈伯(P·Haber)利用N2和H2在Fe催化作用下最早人工合成氨气,该反应为: N2(g)+ 3H2(g)
 2NH3(g) ΔH = -92.4 kJ·mol-1
2NH3(g) ΔH = -92.4 kJ·mol-1①写出该反应的平衡常数表达式K =
②关于合成氨工艺的下列理解,正确的是
A.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
B.降低温度能使平衡向正反应方向进行且平衡常数不变
C.合成氨反应在不同温度下的ΔH和ΔS都小于零
D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】节能减排是指节约物质资源和能量资源,减少废弃物和环境有害物的排放。
(1)实现“节能减排”和“低碳经济”的项重要课题就是如何将 转化为可利用的资源。目前工业上有一种方法是用
转化为可利用的资源。目前工业上有一种方法是用 来生产燃料甲醇,一定条件下发生反应:
来生产燃料甲醇,一定条件下发生反应:
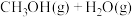 ,如图所示为该反应过程中的能量
,如图所示为该反应过程中的能量 变化:
变化:

下列关于该反应的说法正确的是_____________ (填序号)。
A.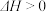 ,
, B.
B.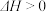 ,
,
C. ,
, D.
D. ,
,
(2)将煤加工成水煤气可降低污染并提高燃料的利用率。将水蒸气通过红热的炭即产生水煤气,反应方程式为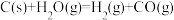 ,该反应的
,该反应的 ,
,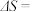
 。该反应在常温下
。该反应在常温下_____________ (填“能”或“不能”)自发进行。
(1)实现“节能减排”和“低碳经济”的项重要课题就是如何将
 转化为可利用的资源。目前工业上有一种方法是用
转化为可利用的资源。目前工业上有一种方法是用 来生产燃料甲醇,一定条件下发生反应:
来生产燃料甲醇,一定条件下发生反应:
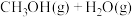 ,如图所示为该反应过程中的能量
,如图所示为该反应过程中的能量 变化:
变化:
下列关于该反应的说法正确的是
A.
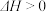 ,
, B.
B.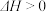 ,
,
C.
 ,
, D.
D. ,
,
(2)将煤加工成水煤气可降低污染并提高燃料的利用率。将水蒸气通过红热的炭即产生水煤气,反应方程式为
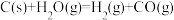 ,该反应的
,该反应的 ,
,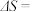
 。该反应在常温下
。该反应在常温下
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮氧化合物是目前造成大气污染的主要气体,而汽车尾气中就含有NO 等多种污染气体。汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致。请结合所学知识回答下列问题:
(1) 已知:N2(g)+2O2(g) 2NO2(g) △H1=+67.8 kJ/mol
2NO2(g) △H1=+67.8 kJ/mol
2NO2(g) O2(g)+2NO(g) △H2=+116.2 kJ/mol
O2(g)+2NO(g) △H2=+116.2 kJ/mol
则N2(g)+O2(g) 2NO(g) △H=
2NO(g) △H=_________ kJ/mol;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为_____________
(2) 若反应N2(g)+O2(g) 2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是
2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是________
a.2υ正(N2)= υ逆(NO) b.混合气体密度不变
c.生成1molO2的同时生成2molNO d.混合气体平均相对分子质量不变
(3) 汽车尾气净化反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
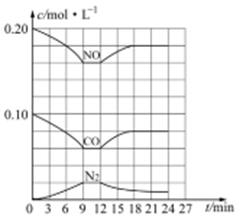
①该反应能自发进行的条件为_____ (填“高温”、“低温”或“任意温度”);
②在6~9 min 内,以CO 表示的平均反应速率 υ(CO)=________ mol·L-l·min-1;
③第12min时改变的反应条件为_________ (填“升高温度”或“降低温度”);
④反应在第24min时的平衡常数K=____________ (只列出计算式,无需计算结果),若保持温度不变,再向容器中充入CO、N2 各0.060mol,平衡将_________ 移动(填“正向”、“逆向”或“不”)。
(1) 已知:N2(g)+2O2(g)
 2NO2(g) △H1=+67.8 kJ/mol
2NO2(g) △H1=+67.8 kJ/mol2NO2(g)
 O2(g)+2NO(g) △H2=+116.2 kJ/mol
O2(g)+2NO(g) △H2=+116.2 kJ/mol则N2(g)+O2(g)
 2NO(g) △H=
2NO(g) △H=(2) 若反应N2(g)+O2(g)
 2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是
2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是a.2υ正(N2)= υ逆(NO) b.混合气体密度不变
c.生成1molO2的同时生成2molNO d.混合气体平均相对分子质量不变
(3) 汽车尾气净化反应:2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
①该反应能自发进行的条件为
②在6~9 min 内,以CO 表示的平均反应速率 υ(CO)=
③第12min时改变的反应条件为
④反应在第24min时的平衡常数K=
您最近一年使用:0次



