合成氨是人类科学技术发展史上的一项重大成就,是化学和技术对社会发展与进步的巨大贡献。
(1)基态氮原子中,能量最高的电子的电子云在空间有___________ 个伸展方向。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为___________ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有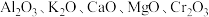 等氧化物中的几种。
等氧化物中的几种。
①Cr原子的价电子排布图为___________ ;第四周期ds区元素中,与基态Cr原子最外层电子数目相同的元素的元素符号为___________ 。
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有___________ (填元素符号)。
(4)我国科研人员研制出了 (M为Fe、Mn等金属)等催化剂,使得合成氨工业温度,压强分别降到了350℃、
(M为Fe、Mn等金属)等催化剂,使得合成氨工业温度,压强分别降到了350℃、 ,这是近年来合成氨反应研究中的重要突破。第三电离能
,这是近年来合成氨反应研究中的重要突破。第三电离能
___________ 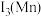 (填“>”或“<”),原因是
(填“>”或“<”),原因是___________ 。
(1)基态氮原子中,能量最高的电子的电子云在空间有
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
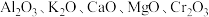 等氧化物中的几种。
等氧化物中的几种。①Cr原子的价电子排布图为
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有
(4)我国科研人员研制出了
 (M为Fe、Mn等金属)等催化剂,使得合成氨工业温度,压强分别降到了350℃、
(M为Fe、Mn等金属)等催化剂,使得合成氨工业温度,压强分别降到了350℃、 ,这是近年来合成氨反应研究中的重要突破。第三电离能
,这是近年来合成氨反应研究中的重要突破。第三电离能
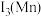 (填“>”或“<”),原因是
(填“>”或“<”),原因是
更新时间:2023-12-29 10:39:28
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】元素周期表中前7周期的元素数目如表所示(假设第7周期已排满):
(1)第6、7周期比第4、5周期多了14种元素,其原因是_______ 。
(2)周期表中_______ 族所含元素最多。
(3)请分析周期数与元素数目的关系后预言第8周期最多可能含有的元素种数为_______ 。
A.18 B.32 C.50 D.64
(4)如将现行族号取消,并按从左到右顺序将原有的各族依次称为1~18纵列,则32号元素锗(Ge)位于第_______ 周期第_______ 纵列。
| 周期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素种数 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
(1)第6、7周期比第4、5周期多了14种元素,其原因是
(2)周期表中
(3)请分析周期数与元素数目的关系后预言第8周期最多可能含有的元素种数为
A.18 B.32 C.50 D.64
(4)如将现行族号取消,并按从左到右顺序将原有的各族依次称为1~18纵列,则32号元素锗(Ge)位于第
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求完成下列填空
(1)某原子的激发态原子的电子排布式为1s22s22p63s23p34s1,则该原子基态原子的电子排布式为______________________ ;元素符号为_________ ;其最高价氧化物对应的水化物的化学式是__________ 。
(2)某原子的电子排布式为 [Ne]3s23p1,则该原子的元素符号为______ ,最高正价为______ ,该原子位于元素周期表第_____ 周期第_____ 族,位于元素周期表______ 区。
(3)某原子位于元素周期表第3周期第IA族,则该原子序数为________ ,位于元素周期表______ 区,电子排布式为________________________ 。
(1)某原子的激发态原子的电子排布式为1s22s22p63s23p34s1,则该原子基态原子的电子排布式为
(2)某原子的电子排布式为 [Ne]3s23p1,则该原子的元素符号为
(3)某原子位于元素周期表第3周期第IA族,则该原子序数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)非金属性最强的元素是______ (填元素符号,下同),形成化合物种类最多的元素是_______ 。
(2)③④⑤⑥元素的离子半径从大到小顺序是___________________ (填离子符号),表中十种元素最高价氧化物对应水化物中具有两性的是____________ (填写化学式)。
(3)⑤⑥⑦单质的活泼性顺序为________________________ (从大到小排列,填元素符号),判断的实验依据是________________________________________________ (写出一种)。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)非金属性最强的元素是
(2)③④⑤⑥元素的离子半径从大到小顺序是
(3)⑤⑥⑦单质的活泼性顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】非金属氮化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态N原子核外电子的运动状态有_____ 种;N、O、F第一电离能由大到小的顺序为_____ 。氟化硝酰NO2F可用作火箭推进剂中的氧化剂,NO2F中心原子的杂化方式为_____ 。气态N2O5的分子结构为 ,而固态N2O5则由一种直线型的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为
,而固态N2O5则由一种直线型的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为_____ ,Y的离域键可表达为_____ 。
(2)人体内氧气的输送主要由红细胞内的血红蛋白负责,而红细胞以及血浆中还有少量的血蓝蛋白也能和氧气反应。用配体L,Cu离子和氧气能合成类似血监蛋白的模型配合物Cu2L2O22,该结构呈现出强烈的OO键断裂趋势,成键形态X与断键形态Y达成快速平衡。(iPr为异丙基)_____ ,含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。1molY离子中通过螯合作用形成的配位键有_____ mol。
(1)基态N原子核外电子的运动状态有
 ,而固态N2O5则由一种直线型的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为
,而固态N2O5则由一种直线型的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为(2)人体内氧气的输送主要由红细胞内的血红蛋白负责,而红细胞以及血浆中还有少量的血蓝蛋白也能和氧气反应。用配体L,Cu离子和氧气能合成类似血监蛋白的模型配合物Cu2L2O22,该结构呈现出强烈的OO键断裂趋势,成键形态X与断键形态Y达成快速平衡。(iPr为异丙基)

您最近一年使用:0次
【推荐2】三元锂电池性能优异、能量密度高,正极材料包含了Ni、Co、Mn三种过渡金属的氧化物。
(1)基态Ni原子有___________ 个未成对电子,Ni2+核外电子排布式为___________ 。
(2)如表是Mn与Fe的部分电离能数据,解释I3(Mn)大于I3(Fe)的主要原因:___________ 。
(1)基态Ni原子有
(2)如表是Mn与Fe的部分电离能数据,解释I3(Mn)大于I3(Fe)的主要原因:
| 元素 | Fe | Mn |
| 第二电离能I2/(kJ·mol-1) | 1561 | 1509 |
| 第三电离能I3/(kJ·mol-1) | 2957 | 3248 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求完成下列填空:
(1)基态 的简化电子排布式为
的简化电子排布式为_______ 。
(2)基态 的价层电子排布式为
的价层电子排布式为_______ 。
(3)基态 的结构示意图为
的结构示意图为_______ 。
(4)基态O的轨道表示式为_______ 。
(5)某元素的原子序数为33,该元素原子核外有_______ 个原子轨道,核外共有_______ 种不同运动状态的电子。
(1)基态
 的简化电子排布式为
的简化电子排布式为(2)基态
 的价层电子排布式为
的价层电子排布式为(3)基态
 的结构示意图为
的结构示意图为(4)基态O的轨道表示式为
(5)某元素的原子序数为33,该元素原子核外有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答下列问题
(1)某元素的原子序数为33,则:此元素原子的电子总数是______ ;有_____ 个不同运动状态的电子,有____ 个电子层,____ 个能级;简化的电子排布式为__________ 。
(2)1s22s22p63s23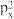 违背了
违背了____________ 。核电荷数为24的元素,其价电子排布的轨道表示式______ ,其原子的最外层电子数和未成对电子数分别为_____ 和_____ 。
(3)电子排布式为1s22s22p63s23p6某微粒的盐溶液能使溴水褪色,并出现浑浊,这种微粒的符号是________ , 原子核外电子云有________ 种不同的伸展方向。
(1)某元素的原子序数为33,则:此元素原子的电子总数是
(2)1s22s22p63s23
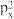 违背了
违背了(3)电子排布式为1s22s22p63s23p6某微粒的盐溶液能使溴水褪色,并出现浑浊,这种微粒的符号是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】综合填空题:
(1)基态砷原子的电子排布式为_______ ,价电子排布图为_______ ,砷元素在周期表的位置为_______ 。
(2)元素锰位于周期表的_______ 区(填“s”、“p”、“d”或“ds”),Mn成为阳离子时首先失去_______ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为_______ ;基态锰原子的第三电离能远大于其第二电离能的原因为:_______ 。
(3)利用CO可以合成化工原料COCl2,COCl2分子的结构式为 ,每个COCl2分子内含有的σ键、π键数目比为
,每个COCl2分子内含有的σ键、π键数目比为_______ ,碳氯键是_______ (填“极性键”或“非极性键”)。
(1)基态砷原子的电子排布式为
(2)元素锰位于周期表的
(3)利用CO可以合成化工原料COCl2,COCl2分子的结构式为
 ,每个COCl2分子内含有的σ键、π键数目比为
,每个COCl2分子内含有的σ键、π键数目比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下图是元素周期表的一部分,所列的字母分别代表一种化学元素。试回答下列问题:
(1)基态n原子中,核外电子占据最高能层的符号是_______ ,占据该能层的电子云轮廓图形状为_______ 。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是_______ 。
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p(序号)两元素的部分电离能数据列于下表:
①o元素价电子的轨道表示式为_______ 。
②比较两元素的 、
、 可知,气态
可知,气态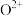 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是_______ 。
(4)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能,c、d、e三元素中,电子亲和能从大到小的顺序为_______ (填元素符号)。
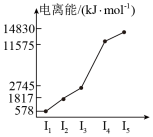
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式_______ 。
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p | |||||||||||||||
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p(序号)两元素的部分电离能数据列于下表:
| 元素 | o | p | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
②比较两元素的
 、
、 可知,气态
可知,气态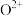 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是(4)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能,c、d、e三元素中,电子亲和能从大到小的顺序为
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】第四周期有14种金属元素,其中4种为主族元素,10种为过渡元素。 回答下列问题:
(1)写出其中原子序数最小的副族元素的元素符号___________ ,主族序数最大的元素名称___________ ;
(2)锰元素在周期表中的位置为___________ ;属于___________ 区元素 填“s”“p”“d”“ds”或“f”
填“s”“p”“d”“ds”或“f” 。
。
(3)基态铬原子的电子排布式为___________ ,与铬同周期的所有元素的基态原子中,最外层电子数与铬原子相同的有___________ 。
(4)基态Fe原子中,电子占据的最高能层的符号为___________ ,该能层具有的原子轨道数为___________ 。
(5)铜、锌两种元素的第一电离能、第二电离能如表所示:
铜的第二电离能 却大于锌的第二电离能,其主要原因是
却大于锌的第二电离能,其主要原因是___________ 。
(1)写出其中原子序数最小的副族元素的元素符号
(2)锰元素在周期表中的位置为
 填“s”“p”“d”“ds”或“f”
填“s”“p”“d”“ds”或“f” 。
。(3)基态铬原子的电子排布式为
(4)基态Fe原子中,电子占据的最高能层的符号为
(5)铜、锌两种元素的第一电离能、第二电离能如表所示:
电离能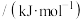 |  |  |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
铜的第二电离能
 却大于锌的第二电离能,其主要原因是
却大于锌的第二电离能,其主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列小题
(1)下列物质变化,只与范德华力有关的是___________。
(2)下面是s能级与p能级的原子轨道图:

请回答下列问题:
s电子的原子轨道呈___________ 形,每个s能级有___________ 个原子轨道;
p电子的原子轨道呈___________ 形,每个p能级有___________ 个原子轨道。
(3)Na、Mg、Al第一电离能的由大到小的顺序:___________ 。
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:①2s②3d③4s④3s⑤4p⑥3p
轨道能量由低到高排列顺序是___________ 。
(5)乙炔HC≡CH中C原子以___________ 方式杂化,实验室中一般用CaC2以水反应制取,同时生成一种碱;写出CaC2以水反应的化学方程式___________ 。
(6)用电子式表示CaCl2的形成过程:___________ 。
(1)下列物质变化,只与范德华力有关的是___________。
| A.干冰熔化 | B.乙酸汽化 | C.乙醇溶于水 | D.碘溶于四氯化碳 |

请回答下列问题:
s电子的原子轨道呈
p电子的原子轨道呈
(3)Na、Mg、Al第一电离能的由大到小的顺序:
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:①2s②3d③4s④3s⑤4p⑥3p
轨道能量由低到高排列顺序是
(5)乙炔HC≡CH中C原子以
(6)用电子式表示CaCl2的形成过程:
您最近一年使用:0次



