工业上制备硫酸的一步重要反应是 在400~500℃下的催化氧化反应
在400~500℃下的催化氧化反应 △H<0。下列有关说法错误的是
△H<0。下列有关说法错误的是
 在400~500℃下的催化氧化反应
在400~500℃下的催化氧化反应 △H<0。下列有关说法错误的是
△H<0。下列有关说法错误的是A.实际生产中, 、 、 再循环使用提高原料利用率 再循环使用提高原料利用率 |
B.在实际生产中控制温度为400~500℃,温度过低速率慢,温度过高 转化率低 转化率低 |
C.为提高反应速率和平衡时 的转化率,实际生产中采用的压强越大越好 的转化率,实际生产中采用的压强越大越好 |
| D.要综合考虑影响速率与平衡的各种因素、设备条件和经济成本等,寻找适宜的生产条件 |
更新时间:2024-01-08 11:15:35
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定温度下,100mL 硫酸溶液和过量的锌粉反应,为了减慢该反应速率,但又不影响生成氢气的总量。可向反应体系中加入适量的
硫酸溶液和过量的锌粉反应,为了减慢该反应速率,但又不影响生成氢气的总量。可向反应体系中加入适量的
 硫酸溶液和过量的锌粉反应,为了减慢该反应速率,但又不影响生成氢气的总量。可向反应体系中加入适量的
硫酸溶液和过量的锌粉反应,为了减慢该反应速率,但又不影响生成氢气的总量。可向反应体系中加入适量的A. 固体 固体 | B. 固体 固体 | C. 硫酸 硫酸 | D.NaOH溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】“氯化反应”通常指将氯元素引入化合物中的反应。计算机模拟单个乙炔分子和氯化氢分子在催化剂表面的反应历程如图所示。下列说法正确的是
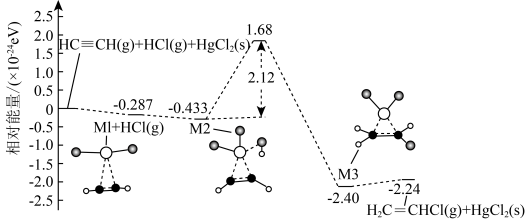

| A.升高温度有利于该反应正向进行 |
B.M1为 与 与 形成的中间体 形成的中间体 |
| C.生产中将催化剂处理成纳米级颗粒可提高乙炔的平衡转化率 |
D.该反应的热化学方程式为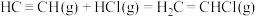 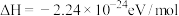 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】二氧化硫的催化氧化反应:2SO2(g)+O2(g) 2SO3(g)是工业制硫酸的重要反应之一,下列说法
2SO3(g)是工业制硫酸的重要反应之一,下列说法错误 的是
 2SO3(g)是工业制硫酸的重要反应之一,下列说法
2SO3(g)是工业制硫酸的重要反应之一,下列说法| A.该反应加入催化剂是为了加快反应速率 |
| B.已知该催化氧化反应K(300 ℃)>K(350 ℃),则该反应正向是放热反应 |
| C.煅烧硫铁矿(主要成分FeS2)可获得SO2,将矿石粉碎成小颗粒可提高反应的平衡转化率 |
| D.保持温度不变,平衡后增大O2的浓度,该反应的平衡常数K不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】K2FeO4在水中不稳定,发生反应:4FeO +10H2O
+10H2O 4Fe(OH)3(胶体)+8OH- +3O2
4Fe(OH)3(胶体)+8OH- +3O2 ,其稳定性与温度(T)和溶液 pH 的关系分别如图所示。下列说法正确的是
,其稳定性与温度(T)和溶液 pH 的关系分别如图所示。下列说法正确的是

图 IK2FeO4 的稳定性与温度的关系 图 IIK2FeO4 的稳定性与溶液 pH 的关系
 +10H2O
+10H2O 4Fe(OH)3(胶体)+8OH- +3O2
4Fe(OH)3(胶体)+8OH- +3O2 ,其稳定性与温度(T)和溶液 pH 的关系分别如图所示。下列说法正确的是
,其稳定性与温度(T)和溶液 pH 的关系分别如图所示。下列说法正确的是
图 IK2FeO4 的稳定性与温度的关系 图 IIK2FeO4 的稳定性与溶液 pH 的关系
| A.由图 I 可知 K2FeO4的稳定性随温度的升高而升高 | B.由图 II 可知图中 a>c |
| C.由图 I 可知温度:T1>T2>T3 | D.由图 I 可知上述反应ΔH<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知FeCl3溶液与KSCN溶液混合后发生反应FeCl3+3KSCN Fe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是
Fe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是
 Fe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是
Fe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是| A.向溶液中加入少许KC1固体,溶液颜色变浅 |
| B.升高温度,平衡一定发生移动 |
| C.加入少许KC1固体或者加入少许FeCl3固体平衡常数均发生变化,且变化方向相反 |
| D.平衡常数表达式为K=c[Fe(SCN)3]·c3(KCl)/[c(FeCl3)·c3(KSCN)] |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】以二氧化钛表面覆盖Cu2Al2O4为催化剂,可将CO2和CH4直接转化成乙酸,如图为反应过程中催化剂的催化效率(实线)与乙酸的生成速率(虚线)随温度的变化情况。下列说法不正确的是
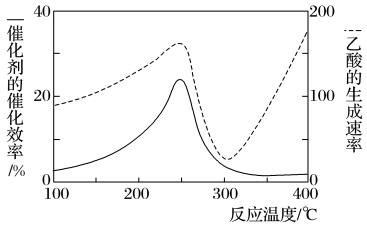

| A.该制备乙酸的反应中,原子利用率为100% |
| B.Cu2Al2O4写成氧化物的形式是Cu2O·Al2O3 |
| C.由图可知,工业上制备乙酸最适宜的温度应为250℃或者400℃ |
| D.250~300℃时,温度升高而乙酸的生成速率降低的主要原因是催化剂的催化效率降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】科学家研究N2在催化剂表面与水能生成NH3:2N2(g)+6H2O(l) 4NH3(g)+3O2(g),下表是同一时间段(2h)NH3生成量与温度的关系,下列说法正确的是
4NH3(g)+3O2(g),下表是同一时间段(2h)NH3生成量与温度的关系,下列说法正确的是
 4NH3(g)+3O2(g),下表是同一时间段(2h)NH3生成量与温度的关系,下列说法正确的是
4NH3(g)+3O2(g),下表是同一时间段(2h)NH3生成量与温度的关系,下列说法正确的是 | T/K | 313 | 323 | 333 | 383 |
| NH3生成量/(mol) | 4.5 | 5.2 | 6.0 | 2.0 |
| A.该反应为吸热反应 |
| B.可通过适当增大压强来提高该反应速率 |
| C.323K时,该反应已经达到平衡状态 |
| D.333K时,该反应的平均反应速率为v(NH3)=6.0mol•h-1 |
您最近一年使用:0次

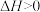 自发进行的化学反应,其
自发进行的化学反应,其
 的可逆反应来说,升高温度可加快反应速率,增大反应物转化率
的可逆反应来说,升高温度可加快反应速率,增大反应物转化率 时,说明该反应已进行得比较完全
时,说明该反应已进行得比较完全


