工业生产过程中产生的含硫化合物( ,
, 等)会造成环境问题,可用多种方法脱除。
等)会造成环境问题,可用多种方法脱除。
Ⅰ.由次氯酸钠碱性废水(含有杂质 )处理硫酸工业尾气的流程如下:
)处理硫酸工业尾气的流程如下:
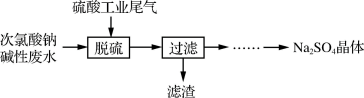
(1)控制合适的条件有利于提高 的吸收率(脱硫率)。
的吸收率(脱硫率)。
①脱硫时需保持溶液呈碱性,此过程的主要反应之一为: ;另一个为氧化还原反应,请写出该反应的离子方程式:
;另一个为氧化还原反应,请写出该反应的离子方程式:___________ 。
②提高脱硫率的可行措施有______ (填序号)。
a.加快通入尾气的速率 b.吸收塔中喷淋的碱液与气体逆向接触 c.提高碱液pH
③温度控制在40-60℃之间,脱硫率较高,原因是___________ 。
(2)滤渣的主要成分为______ (填化学式)。
Ⅱ.一种铁基脱硫剂脱除硫化氢( )的方法包括吸收和再生两个阶段,其工艺流程原理如下:
)的方法包括吸收和再生两个阶段,其工艺流程原理如下:
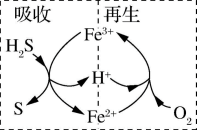
(3)写出“吸收”反应的离子方程式:___________ 。
(4)当吸收224mL(标准状况) 时,若要保持脱硫液中
时,若要保持脱硫液中 的物质的量不变,则所通入的氧气的物质的量为
的物质的量不变,则所通入的氧气的物质的量为______ mol。
 ,
, 等)会造成环境问题,可用多种方法脱除。
等)会造成环境问题,可用多种方法脱除。Ⅰ.由次氯酸钠碱性废水(含有杂质
 )处理硫酸工业尾气的流程如下:
)处理硫酸工业尾气的流程如下:
(1)控制合适的条件有利于提高
 的吸收率(脱硫率)。
的吸收率(脱硫率)。①脱硫时需保持溶液呈碱性,此过程的主要反应之一为:
 ;另一个为氧化还原反应,请写出该反应的离子方程式:
;另一个为氧化还原反应,请写出该反应的离子方程式:②提高脱硫率的可行措施有
a.加快通入尾气的速率 b.吸收塔中喷淋的碱液与气体逆向接触 c.提高碱液pH
③温度控制在40-60℃之间,脱硫率较高,原因是
(2)滤渣的主要成分为
Ⅱ.一种铁基脱硫剂脱除硫化氢(
 )的方法包括吸收和再生两个阶段,其工艺流程原理如下:
)的方法包括吸收和再生两个阶段,其工艺流程原理如下:
(3)写出“吸收”反应的离子方程式:
(4)当吸收224mL(标准状况)
 时,若要保持脱硫液中
时,若要保持脱硫液中 的物质的量不变,则所通入的氧气的物质的量为
的物质的量不变,则所通入的氧气的物质的量为
更新时间:2024-01-10 16:38:31
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.现有以下物质:①石墨;②乙醇;③氨水;④二氧化碳;⑤碳酸钠固体;⑥氢氧化钡溶液;⑦纯醋酸;⑧氯化氢气体。(填序号)
(1)其中能导电的是_______ ;属于非电解质的是_______ ;属于电解质的是_______ 。
Ⅱ.某100mL溶液可能含有 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知 和
和 反应有气体产生且全部逸出)。
反应有气体产生且全部逸出)。
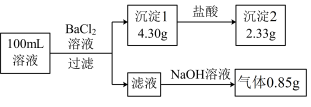
(2)原溶液中除含有 外,一定还含有
外,一定还含有_______ 离子,可能含有_______ 离子;
(3)实验中生成碳酸钡的离子方程式为_______ 。
(1)其中能导电的是
Ⅱ.某100mL溶液可能含有
 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知 和
和 反应有气体产生且全部逸出)。
反应有气体产生且全部逸出)。
(2)原溶液中除含有
 外,一定还含有
外,一定还含有(3)实验中生成碳酸钡的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】MnCO3可用于制备活性电极材料MnO2。以菱锰矿(含MnCO3、SiO2、FeCO3和少量Al2O3等)为原料制备碳酸锰粗产品的流程如下:

已知:①常温下,Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=4.0×10-34。
②氢氧化物沉淀的条件:Al3+、Fe3+完全沉淀的pH分别为4.6、3.4;Mn2+开始沉淀的pH为8.1。
(1)“酸浸”过程中不能用浓盐酸替代硫酸,原因是_________________________________ 。
(2)用离子方程式表示“氧化”过程中加MnO2的目的:_______________________________ 。
(3)“调pH”时,向含有硫酸铁和硫酸铝的混合溶液中滴加氢氧化钠溶液至两种沉淀共存,当c(Fe3+)=1.0×10-5mol·L-1时,c(Al3+)=______________ mol·L-1。
(4)①“沉锰”过程中,反应的离子方程式为_____________________ 。
②“沉锰”过程中沉锰速率与温度的关系如图所示。当温度高于60℃时,沉锰速率随着温度升高而减慢的原因可能是_____________________________ 。

(5)从滤液3中可分离出一种不含碳元素的氮肥,它的化学式为_____________________________ 。
(6)工业上,可以将碳酸锰制成硫酸锰,再用惰性电极电解酸性硫酸锰溶液来制备活性二氧化锰,电解时的阳极反应式为________________________________ 。

已知:①常温下,Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=4.0×10-34。
②氢氧化物沉淀的条件:Al3+、Fe3+完全沉淀的pH分别为4.6、3.4;Mn2+开始沉淀的pH为8.1。
(1)“酸浸”过程中不能用浓盐酸替代硫酸,原因是
(2)用离子方程式表示“氧化”过程中加MnO2的目的:
(3)“调pH”时,向含有硫酸铁和硫酸铝的混合溶液中滴加氢氧化钠溶液至两种沉淀共存,当c(Fe3+)=1.0×10-5mol·L-1时,c(Al3+)=
(4)①“沉锰”过程中,反应的离子方程式为
②“沉锰”过程中沉锰速率与温度的关系如图所示。当温度高于60℃时,沉锰速率随着温度升高而减慢的原因可能是

(5)从滤液3中可分离出一种不含碳元素的氮肥,它的化学式为
(6)工业上,可以将碳酸锰制成硫酸锰,再用惰性电极电解酸性硫酸锰溶液来制备活性二氧化锰,电解时的阳极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】工业上以浓缩海水为原料提取溴的部分流程如下:

已知:Br2常温下呈液态,易挥发,有毒;3Br2+3CO =5Br-+BrO
=5Br-+BrO +3CO2。
+3CO2。

(1)上述流程中,步骤①~③的目的是________ 。
(2)反应釜2中发生反应的离子方程式为____________ 。
(3)实验室使用右图所示装置模拟上述过程。A装置中先通入Cl2一段时间后,再通入热空气。通入热空气的目的是____________ ;B装置中导管D的作用是________ ;C装置中溶液X为________ 。
(4)对反应后烧瓶B中的溶液进行如下实验,请补充完整相关实验步骤。
限选用的试剂为:稀硫酸、四氯化碳、澄清石灰水。
①检验烧瓶B的溶液中是否含有CO 。
。
取烧瓶B中的溶液适量,加入试管中,再加入过量的稀硫酸酸化;____ 。
②提取反应后烧瓶B溶液中的溴单质。
向烧瓶B中加入过量的稀硫酸酸化;____ 。

已知:Br2常温下呈液态,易挥发,有毒;3Br2+3CO
 =5Br-+BrO
=5Br-+BrO +3CO2。
+3CO2。
(1)上述流程中,步骤①~③的目的是
(2)反应釜2中发生反应的离子方程式为
(3)实验室使用右图所示装置模拟上述过程。A装置中先通入Cl2一段时间后,再通入热空气。通入热空气的目的是
(4)对反应后烧瓶B中的溶液进行如下实验,请补充完整相关实验步骤。
限选用的试剂为:稀硫酸、四氯化碳、澄清石灰水。
①检验烧瓶B的溶液中是否含有CO
 。
。取烧瓶B中的溶液适量,加入试管中,再加入过量的稀硫酸酸化;
②提取反应后烧瓶B溶液中的溴单质。
向烧瓶B中加入过量的稀硫酸酸化;
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】利用钛白废酸[含 、
、 、
、 等]和粉煤灰可资源再利用制备无机高分子絮凝剂−聚合硫酸硅酸铁铝(PFASS),工艺流程如下:
等]和粉煤灰可资源再利用制备无机高分子絮凝剂−聚合硫酸硅酸铁铝(PFASS),工艺流程如下:
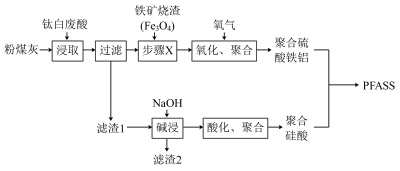
已知:①粉煤灰在酸中只有有限的溶解能力;
②粉煤灰的化学组成:
回答下列问题:
(1)一种铁−铝合金晶胞结构如图所示,该晶体的化学式为_______ 。其中基态铁原子价层电子排布式为_______ 。

(2)为提高浸取率,可采取的措施有_______ (填序号)。
A.加入合适的助溶剂 B.将粉煤灰加热处理 C.适当延长浸取时间
(3)“酸化、聚合”步骤加入的最佳试剂为_______ ;“碱浸”后所得滤液的主要成分为_______ 。
(4)通入氧气时发生反应的离子方程式:_______ 。
(5)步骤X加入铁矿烧渣的目的是_______ 。
(6)根据所学知识推测,与传统净水剂PAC(聚合氯化铝)相比,聚合硫酸硅酸铁铝聚合程度更_______ (填“大”或“小”),理由是_______ 。
(7)聚合硫酸硅酸铁铝可表示成 ,则
,则
_______ 。
 、
、 、
、 等]和粉煤灰可资源再利用制备无机高分子絮凝剂−聚合硫酸硅酸铁铝(PFASS),工艺流程如下:
等]和粉煤灰可资源再利用制备无机高分子絮凝剂−聚合硫酸硅酸铁铝(PFASS),工艺流程如下:
已知:①粉煤灰在酸中只有有限的溶解能力;
②粉煤灰的化学组成:
| 化学成分 |  |  |  | 其他 |
| 质量分数/% | 52.26 | 22.42 | 11.96 | 13.36 |
(1)一种铁−铝合金晶胞结构如图所示,该晶体的化学式为

(2)为提高浸取率,可采取的措施有
A.加入合适的助溶剂 B.将粉煤灰加热处理 C.适当延长浸取时间
(3)“酸化、聚合”步骤加入的最佳试剂为
(4)通入氧气时发生反应的离子方程式:
(5)步骤X加入铁矿烧渣的目的是
(6)根据所学知识推测,与传统净水剂PAC(聚合氯化铝)相比,聚合硫酸硅酸铁铝聚合程度更
(7)聚合硫酸硅酸铁铝可表示成
 ,则
,则
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室用KMnO4固体配制1000 mL0.05 mol·L-1的KMnO4溶液。
回答下列问题:
(1)计算并称量KMnO4固体的质量为_____ g,该实验中必须用到的标有温度的玻璃仪器是_____ 。
(2)下列实验操作规范的是________ (填标号)。
A.称量 B.转移溶液
B.转移溶液
C.溶解 D.定容
D.定容
(3)下列情况会使所配制的KMnO4溶液浓度偏大的是_________ (填标号)。
A.未洗涤烧杯和玻璃棒
B.将溶解后的溶液转移至容量瓶之前,容量瓶未干燥,含有少量蒸馏水
C.定容时俯视刻度线
D.定容时,发现液面超过刻度线,用吸管将多余的溶液吸出
(4)取所配制的KMnO4溶液1.0 mL于试管中,向其中滴加稀硫酸和KI溶液,发现溶液由紫色变成棕黄色,测知有I2和Mn2+生成,则反应的离子方程式为_________________ 。
回答下列问题:
(1)计算并称量KMnO4固体的质量为
(2)下列实验操作规范的是
A.称量
 B.转移溶液
B.转移溶液
C.溶解
 D.定容
D.定容
(3)下列情况会使所配制的KMnO4溶液浓度偏大的是
A.未洗涤烧杯和玻璃棒
B.将溶解后的溶液转移至容量瓶之前,容量瓶未干燥,含有少量蒸馏水
C.定容时俯视刻度线
D.定容时,发现液面超过刻度线,用吸管将多余的溶液吸出
(4)取所配制的KMnO4溶液1.0 mL于试管中,向其中滴加稀硫酸和KI溶液,发现溶液由紫色变成棕黄色,测知有I2和Mn2+生成,则反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是______ (填图中数字序号)
(2)下列关于海洋氮循环的说法正确的是______ (填字母序号)
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量
(3)有氧时,在硝化细菌作用下, 可实现过程④的转化,将过程④的离子方程式补充完整:
可实现过程④的转化,将过程④的离子方程式补充完整:___  +5O2=2
+5O2=2 +
+___ H++______ +______
(4)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放。如图是电解产物氧化工业废水中氨氮( )的示意图。
)的示意图。
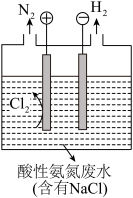
①阳极的电极反应式:______ ;
②写出电解产物氧化去除氨氮的离子方程式:______ ;
③若生成H2和N2的物质的量之比为3:1,则处理后废水的c(H+)将______ (填“增大”“不变”或“减小”)。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含
 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量(3)有氧时,在硝化细菌作用下,
 可实现过程④的转化,将过程④的离子方程式补充完整:
可实现过程④的转化,将过程④的离子方程式补充完整: +5O2=2
+5O2=2 +
+(4)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放。如图是电解产物氧化工业废水中氨氮(
 )的示意图。
)的示意图。
①阳极的电极反应式:
②写出电解产物氧化去除氨氮的离子方程式:
③若生成H2和N2的物质的量之比为3:1,则处理后废水的c(H+)将
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)制取MnSO4·H2O并回收单质硫的工艺流程如下:
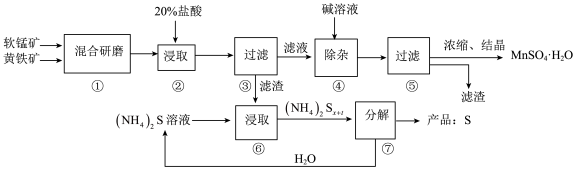
回答下列问题:
(1)步骤②浸取时若生成S、MnSO4及Fe2(SO4)3的化学方程式为_________ 。
(2)步骤③所得酸性滤液可能含有Fe2+,除去Fe2+可用的物质是________ ;步骤④需将溶液加热至沸然后在不断搅拌下加入碱调节pH4~5,再继续煮沸一段时间,“继续煮沸”的目的是_____ 。步骤⑤所得滤渣为_____ (填化学式)。
(3)步骤⑦需在90~100℃下进行,该反应的化学方程式为____________ 。
(4)测定产品MnSO4·H2O的方法之一是:准确称取ag产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用 c mol·L-1 KMnO4标准溶液滴定至浅红色且半分钟不褪,消耗标准溶液VmL,滴定反应的离子方程式为______ ,产品中Mn2+的质量分数为w(Mn2+)=_________ 。

回答下列问题:
(1)步骤②浸取时若生成S、MnSO4及Fe2(SO4)3的化学方程式为
(2)步骤③所得酸性滤液可能含有Fe2+,除去Fe2+可用的物质是
(3)步骤⑦需在90~100℃下进行,该反应的化学方程式为
(4)测定产品MnSO4·H2O的方法之一是:准确称取ag产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用 c mol·L-1 KMnO4标准溶液滴定至浅红色且半分钟不褪,消耗标准溶液VmL,滴定反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】利用废旧锂离子电池的正极材料(主要成分为LiCoO2、Al以及少量Ca、Mg、Cu、Fe等)制备Co3O4微球的工艺流程如下: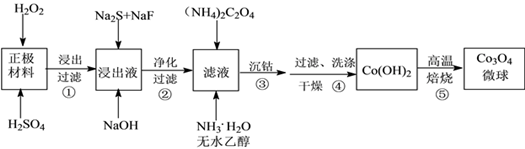
回答下列问题:
(1)LiCoO2 中Co元素的化合价为_______ 。
(2)步骤①中生成Co2+的离子方程式为_______ 。此过程中若用浓盐酸代替H2SO4和H2O2的混合溶液,除因挥发使其利用率降低外,还有的缺点是_______ 。
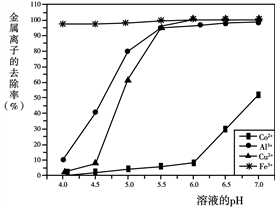
(3)步骤②中,不同pH下溶液中金属离子的去除效果如下图所示。该过程加入NaOH调节溶液pH的最佳范围是_______ ,理由是_______ 。
(4)步骤④中,过滤、洗涤操作均需用到的玻璃仪器有烧杯、玻璃棒、_______ 。
(5)步骤⑤中,Co(OH)2在空气中高温焙烧生成Co3O4的化学方程式为_______ 。
(6)若以钴为电极,控制一定条件,电解NaCl溶液也可制取Co3O4的前驱体Co(OH)2。写出电解的总反应方程式_______ 。
(7)实验室测得“浸出液”中钴元素的含量为a mg/L,取20 mL“浸出液”模拟上述流程进行实验,得到“Co3O4微球”产品b g,又测得产品中钴元素的质量分数为w%。计算钴的回收率为_______ (列式表示)。
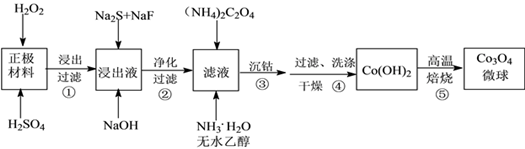
回答下列问题:
(1)LiCoO2 中Co元素的化合价为
(2)步骤①中生成Co2+的离子方程式为
(3)步骤②中,不同pH下溶液中金属离子的去除效果如下图所示。该过程加入NaOH调节溶液pH的最佳范围是

(4)步骤④中,过滤、洗涤操作均需用到的玻璃仪器有烧杯、玻璃棒、
(5)步骤⑤中,Co(OH)2在空气中高温焙烧生成Co3O4的化学方程式为
(6)若以钴为电极,控制一定条件,电解NaCl溶液也可制取Co3O4的前驱体Co(OH)2。写出电解的总反应方程式
(7)实验室测得“浸出液”中钴元素的含量为a mg/L,取20 mL“浸出液”模拟上述流程进行实验,得到“Co3O4微球”产品b g,又测得产品中钴元素的质量分数为w%。计算钴的回收率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],煅烧可获得钛酸钡粉体。

(1)“酸浸”应选择_________ (填标号);为提高酸浸率,可采取的措施_________ (至少答两点)
a. 硫酸 b. 盐酸 c. 硝酸
(2)实验室要完成操作1需要的玻璃仪器有_________ 。
(3)加入H2C2O4溶液时,发生的反应为______ +______ TiCl4+_____ H2C2O4+ _____ H2O= BaTiO(C2O4)2·4H2O↓ + _________ ;可循环使用的物质X是(写名称)_________ 。
(4)请简述检验草酸氧钛钡晶体是否洗涤干净的方法_________ 。
(5)高温煅烧草酸氧钛钡晶体得到BaTiO3的同时,生成的气体产物有CO、和_________ 。
(6)测定钛酸钡粉体中BaTiO3的质量分数。
已知:Ba2++CrO42-=BaCrO4↓ 2CrO42-+2H+=Cr2O72-+H2O
现取a g煅烧后的BaTiO3粉末酸溶得到100.0 mL含Ba2+的溶液,取25.00 mL于锥形瓶,加入x mL 浓度为C1 mol/ L的Na2CrO4溶液(Na2CrO4过量)充分反应后,用浓度为C2 mol/ L标准盐酸滴定至CrO42-被完全反应,消耗盐酸体积为y mL。(钛元素不干扰测定过程)已知BaTiO3的摩尔质量为M g/mol,试写出粉体中BaTiO3质量分数的表达式。_________

(1)“酸浸”应选择
a. 硫酸 b. 盐酸 c. 硝酸
(2)实验室要完成操作1需要的玻璃仪器有
(3)加入H2C2O4溶液时,发生的反应为
(4)请简述检验草酸氧钛钡晶体是否洗涤干净的方法
(5)高温煅烧草酸氧钛钡晶体得到BaTiO3的同时,生成的气体产物有CO、和
(6)测定钛酸钡粉体中BaTiO3的质量分数。
已知:Ba2++CrO42-=BaCrO4↓ 2CrO42-+2H+=Cr2O72-+H2O
现取a g煅烧后的BaTiO3粉末酸溶得到100.0 mL含Ba2+的溶液,取25.00 mL于锥形瓶,加入x mL 浓度为C1 mol/ L的Na2CrO4溶液(Na2CrO4过量)充分反应后,用浓度为C2 mol/ L标准盐酸滴定至CrO42-被完全反应,消耗盐酸体积为y mL。(钛元素不干扰测定过程)已知BaTiO3的摩尔质量为M g/mol,试写出粉体中BaTiO3质量分数的表达式。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
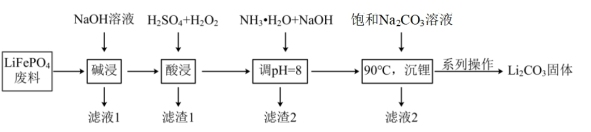
【推荐1】磷酸亚铁锂( )常用作动力锂离子电池的正极材料,利用
)常用作动力锂离子电池的正极材料,利用 废料(还含铝、石墨等成分)回收锂、铁等元素的工艺流程如下。
废料(还含铝、石墨等成分)回收锂、铁等元素的工艺流程如下。
已知: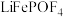 不溶于
不溶于 溶液。
溶液。
回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为_______ ;
(2)“滤液1”含有的阴离子主要有: 、
、_______ ;
(3)在“酸浸”中,磷元素转化为 。
。
①实际操作时,所加 的量要比理论计算值多,可能原因是
的量要比理论计算值多,可能原因是_______ ;
② 发生反应的离子方程式为
发生反应的离子方程式为_______ ;
(4)“滤渣2”的主要成分是_______ ;
(5)碳酸锂溶解度(用溶液中溶质的物质的量分数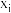 表示)曲线如下图所示。.
表示)曲线如下图所示。.
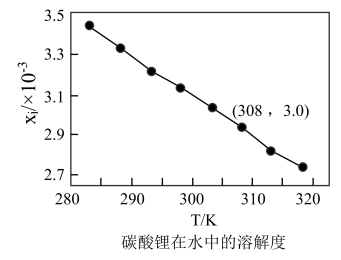
①“沉锂”采用90℃的优点有_______ ;
②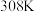 时,碳酸锂溶解度为
时,碳酸锂溶解度为_______ g;
 )常用作动力锂离子电池的正极材料,利用
)常用作动力锂离子电池的正极材料,利用 废料(还含铝、石墨等成分)回收锂、铁等元素的工艺流程如下。
废料(还含铝、石墨等成分)回收锂、铁等元素的工艺流程如下。
已知:
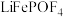 不溶于
不溶于 溶液。
溶液。回答下列问题:
(1)
 中
中 元素的化合价为
元素的化合价为(2)“滤液1”含有的阴离子主要有:
 、
、(3)在“酸浸”中,磷元素转化为
 。
。①实际操作时,所加
 的量要比理论计算值多,可能原因是
的量要比理论计算值多,可能原因是②
 发生反应的离子方程式为
发生反应的离子方程式为(4)“滤渣2”的主要成分是
(5)碳酸锂溶解度(用溶液中溶质的物质的量分数
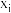 表示)曲线如下图所示。.
表示)曲线如下图所示。.
①“沉锂”采用90℃的优点有
②
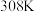 时,碳酸锂溶解度为
时,碳酸锂溶解度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫及其化合物在生产及生活中有着广泛的应用。回答下列问题:
I.二氯砜( )是一种发烟液体,遇水剧烈水解,69.1℃时沸腾。某小组拟用干燥的
)是一种发烟液体,遇水剧烈水解,69.1℃时沸腾。某小组拟用干燥的 和
和 在活性炭催化作用下制备二氯砜。反应的化学方程式为
在活性炭催化作用下制备二氯砜。反应的化学方程式为 ,实验装置如图1所示(部分夹持装置已略去):
,实验装置如图1所示(部分夹持装置已略去):
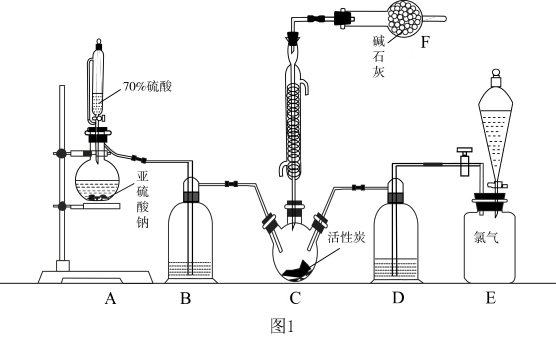
(1)装置A中盛装70%硫酸的仪器名称为_______ ,该仪器使用前必须进行的操作为_______ 。
(2)装置B和D的作用为_______ ;装置F的作用为_______ 。
(3)分液漏斗中盛放的最佳试剂为_______ 。
Ⅱ.二氯亚砜( )是一种无色易挥发的液体,遇水剧烈反应生成两种气体,常用作脱水剂。
)是一种无色易挥发的液体,遇水剧烈反应生成两种气体,常用作脱水剂。
(4)写出二氯亚砜与水反应的化学方程式:_______ 。
(5)二氯亚砜中心原子的杂化方式为_______ ,二氯亚砜是_______ 分子(填“极性”或“非极性”)。
(6)利用如图2所示装置(加热和夹持装置已略去)用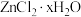 制备无水
制备无水 ,并回收剩余的
,并回收剩余的 。在加热条件下,三颈烧瓶中发生反应的化学方程式为
。在加热条件下,三颈烧瓶中发生反应的化学方程式为_______ 。

I.二氯砜(
 )是一种发烟液体,遇水剧烈水解,69.1℃时沸腾。某小组拟用干燥的
)是一种发烟液体,遇水剧烈水解,69.1℃时沸腾。某小组拟用干燥的 和
和 在活性炭催化作用下制备二氯砜。反应的化学方程式为
在活性炭催化作用下制备二氯砜。反应的化学方程式为 ,实验装置如图1所示(部分夹持装置已略去):
,实验装置如图1所示(部分夹持装置已略去):
(1)装置A中盛装70%硫酸的仪器名称为
(2)装置B和D的作用为
(3)分液漏斗中盛放的最佳试剂为
Ⅱ.二氯亚砜(
 )是一种无色易挥发的液体,遇水剧烈反应生成两种气体,常用作脱水剂。
)是一种无色易挥发的液体,遇水剧烈反应生成两种气体,常用作脱水剂。(4)写出二氯亚砜与水反应的化学方程式:
(5)二氯亚砜中心原子的杂化方式为
(6)利用如图2所示装置(加热和夹持装置已略去)用
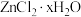 制备无水
制备无水 ,并回收剩余的
,并回收剩余的 。在加热条件下,三颈烧瓶中发生反应的化学方程式为
。在加热条件下,三颈烧瓶中发生反应的化学方程式为
您最近一年使用:0次
【推荐3】碲(Te)是重要的稀有元素,被誉为“现代高新技术材料的维生素”。一种从碲化镉废料中(主要成分为CdTe、CdS、SiO2)回收Te和Cd的工艺流程如图所示。

已知:室温下,饱和 溶液的浓度为0.01 mol⋅L
溶液的浓度为0.01 mol⋅L ,
, ,
,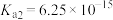 ;
; ;
;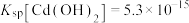 。
。
回答下列问题:
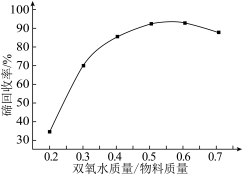
(1)碲与氧同族,基态碲原子价电子排布式为___________ ,“氧化浸出”时,温度控制在80℃的原因是___________ 。“氧化浸出”过程中CdTe反应的离子方程式为___________ ,其他条件不变,该过程中双氧水与物料质量比对碲回收率的影响如图所示。质量比高于0.6时,碲回收率降低的原因是___________ 。
(2)“溶浸”过程中,“浸渣”的主要成分___________ ;还原过程中发生反应的方程式为___________ 。
(3)“沉镉”需在酸性环境中进行的原因是___________ 。 完全沉淀时,为防止
完全沉淀时,为防止 气体逸出,溶液中
气体逸出,溶液中 应控制在
应控制在___________ mol⋅L-1以下(离子浓度低于 mol⋅L-1视为完全沉淀)。
mol⋅L-1视为完全沉淀)。
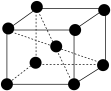
(4)已知:镉晶胞如图所示。晶胞参数为a pm, 为阿伏加德罗常数的值。两个Cd之间最近距离为
为阿伏加德罗常数的值。两个Cd之间最近距离为___________ pm,镉晶体密度为___________ g⋅cm-3(用含a、 的代数式表示)。
的代数式表示)。

已知:室温下,饱和
 溶液的浓度为0.01 mol⋅L
溶液的浓度为0.01 mol⋅L ,
, ,
,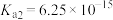 ;
; ;
;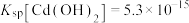 。
。回答下列问题:
(1)碲与氧同族,基态碲原子价电子排布式为

(2)“溶浸”过程中,“浸渣”的主要成分
(3)“沉镉”需在酸性环境中进行的原因是
 完全沉淀时,为防止
完全沉淀时,为防止 气体逸出,溶液中
气体逸出,溶液中 应控制在
应控制在 mol⋅L-1视为完全沉淀)。
mol⋅L-1视为完全沉淀)。(4)已知:镉晶胞如图所示。晶胞参数为a pm,
 为阿伏加德罗常数的值。两个Cd之间最近距离为
为阿伏加德罗常数的值。两个Cd之间最近距离为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次



