利用钛白废酸[含 、
、 、
、 等]和粉煤灰可资源再利用制备无机高分子絮凝剂−聚合硫酸硅酸铁铝(PFASS),工艺流程如下:
等]和粉煤灰可资源再利用制备无机高分子絮凝剂−聚合硫酸硅酸铁铝(PFASS),工艺流程如下:
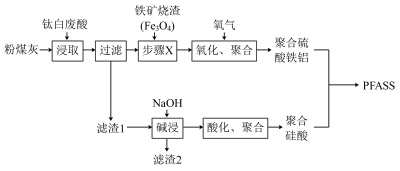
已知:①粉煤灰在酸中只有有限的溶解能力;
②粉煤灰的化学组成:
回答下列问题:
(1)一种铁−铝合金晶胞结构如图所示,该晶体的化学式为_______ 。其中基态铁原子价层电子排布式为_______ 。

(2)为提高浸取率,可采取的措施有_______ (填序号)。
A.加入合适的助溶剂 B.将粉煤灰加热处理 C.适当延长浸取时间
(3)“酸化、聚合”步骤加入的最佳试剂为_______ ;“碱浸”后所得滤液的主要成分为_______ 。
(4)通入氧气时发生反应的离子方程式:_______ 。
(5)步骤X加入铁矿烧渣的目的是_______ 。
(6)根据所学知识推测,与传统净水剂PAC(聚合氯化铝)相比,聚合硫酸硅酸铁铝聚合程度更_______ (填“大”或“小”),理由是_______ 。
(7)聚合硫酸硅酸铁铝可表示成 ,则
,则
_______ 。
 、
、 、
、 等]和粉煤灰可资源再利用制备无机高分子絮凝剂−聚合硫酸硅酸铁铝(PFASS),工艺流程如下:
等]和粉煤灰可资源再利用制备无机高分子絮凝剂−聚合硫酸硅酸铁铝(PFASS),工艺流程如下:
已知:①粉煤灰在酸中只有有限的溶解能力;
②粉煤灰的化学组成:
| 化学成分 |  |  |  | 其他 |
| 质量分数/% | 52.26 | 22.42 | 11.96 | 13.36 |
(1)一种铁−铝合金晶胞结构如图所示,该晶体的化学式为

(2)为提高浸取率,可采取的措施有
A.加入合适的助溶剂 B.将粉煤灰加热处理 C.适当延长浸取时间
(3)“酸化、聚合”步骤加入的最佳试剂为
(4)通入氧气时发生反应的离子方程式:
(5)步骤X加入铁矿烧渣的目的是
(6)根据所学知识推测,与传统净水剂PAC(聚合氯化铝)相比,聚合硫酸硅酸铁铝聚合程度更
(7)聚合硫酸硅酸铁铝可表示成
 ,则
,则
2023·全国·模拟预测 查看更多[3]
(已下线)化学押题卷(六)(已下线)化学-2023年高考押题预测卷02(云南,安徽,黑龙江,山西,吉林五省通用)(含考试版、全解全析、参考答案、答题卡)河北省沧州市沧县中学2023届高三下学期模拟预测化学试题
更新时间:2023-04-11 16:11:44
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】含硫化合物在生产生活中有广泛应用,其吸收处理也十分重要。
(1)完成并配平下列离子方程式_____ 。
Fe3++ SO2+ → Fe2++ SO42-+
(2)标明电子转移的方向和数目______ : Fe3++ SO2……。
(3)在Na2SO3溶液中滴加酚酞,溶液呈红色,若在该溶液中滴入过量的BaCl2溶液,实验现象为:_____ 。请结合离子方程式,运用平衡原理进行解释_____ 。
(4)在NaClO溶液中通入SO2,写出反应的离子方程式:_____ 。
(5)在0.1mol/LNa2SO3溶液中,下列关系式正确的是_____ 。
a.[Na+]+[H+]=[SO32-]+[HSO3-]+[OH-] b.[Na+]>[SO32-]>[OH-]>[H+]
c.[Na+]=2[SO32-]+2[HSO3-]+2[H2SO3] d.[Na+]=2[SO32-]>[OH-]=[H+]
(6)向该溶液中加入少量Na2SO3固体,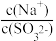
___ (填“增大”“减小”或“不变”)。
(1)完成并配平下列离子方程式
Fe3++ SO2+ → Fe2++ SO42-+
(2)标明电子转移的方向和数目
(3)在Na2SO3溶液中滴加酚酞,溶液呈红色,若在该溶液中滴入过量的BaCl2溶液,实验现象为:
(4)在NaClO溶液中通入SO2,写出反应的离子方程式:
(5)在0.1mol/LNa2SO3溶液中,下列关系式正确的是
a.[Na+]+[H+]=[SO32-]+[HSO3-]+[OH-] b.[Na+]>[SO32-]>[OH-]>[H+]
c.[Na+]=2[SO32-]+2[HSO3-]+2[H2SO3] d.[Na+]=2[SO32-]>[OH-]=[H+]
(6)向该溶液中加入少量Na2SO3固体,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氯酸钾在工业上具有广泛的应用,是焰火、照明弹等的主要成分。某研究性学习小组利用如图所示的实验装置制备氯酸钾。回答下列问题:
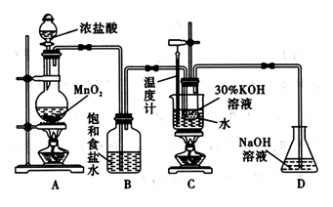
(1)写出装置A中发生反应的离子方程式:________________________________ ;写出装置C中发生反应的离子方程式:________________________________________ 。
(2)若无B装置,则装置C中氯酸钾的产率将________ (填“提高” “降低”或“无影响”)。
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究体系中硫酸浓度对反应产物的影响,实验的记录表如下表(实验在室温下进行):
①实验设计表中V1=____________ ; V3 =_______________ 。
②设计1号试管实验的作用是_________________________ 。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色。假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为_____________________________ 。
(4)工业上可用KC1O3与Na2SO3在H2SO4存在下制备高效、低毒的消毒剂ClO2,该反应的化学方程式为_________________________________ 。

(1)写出装置A中发生反应的离子方程式:
(2)若无B装置,则装置C中氯酸钾的产率将
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究体系中硫酸浓度对反应产物的影响,实验的记录表如下表(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0. 20mol • L-1KI/mL | V1 | 1.0 | 1.0 | 1.0 |
| KC1O3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol • L-1H2SO4/mL | 0 | 3.0 | V2 | 9.0 |
| 蒸馏水 | 9.0 | V3 | 3.0 | 0 |
| 实验现象 |
②设计1号试管实验的作用是
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色。假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为
(4)工业上可用KC1O3与Na2SO3在H2SO4存在下制备高效、低毒的消毒剂ClO2,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】二氧化氯 是黄绿色气体,有毒,沸点为11℃,极易溶于水且不与水反应,具有杀菌、漂白等作用,工业上可用于处理含硫离子废水。
是黄绿色气体,有毒,沸点为11℃,极易溶于水且不与水反应,具有杀菌、漂白等作用,工业上可用于处理含硫离子废水。
已知:①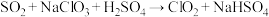 (未配平)
(未配平)
②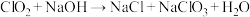 (未配平)
(未配平)
某学习小组在实验室中制备 并探究
并探究 与
与 的反应。请回答下列问题:
的反应。请回答下列问题:
(1)设计如下装置制备

①装置A中反应的化学方程式为___________ 。
②装置B中反应的氧化剂与还原剂的物质的量之比为___________ 。
③欲收集一定量的 ,选择上图中的装置并连接:a→g→h→
,选择上图中的装置并连接:a→g→h→_________ →d。
(2)探究 与
与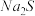 的反应
的反应
将上述收集到的 用
用 稀释以增强其稳定性,利用以下装置,将适量的稀释后的
稀释以增强其稳定性,利用以下装置,将适量的稀释后的 通入
通入 溶液中充分反应,在中得到无色澄清溶液。
溶液中充分反应,在中得到无色澄清溶液。

拟通过下列实验探究Ⅰ中反应的产物。
④ 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(3)另一学习小组将装置A中产生的气体溶于蒸馏水,再将该水溶液滴入 溶液中,振荡,观察到的现象是
溶液中,振荡,观察到的现象是___________ ,发生反应的离方程式为___________ 。
 是黄绿色气体,有毒,沸点为11℃,极易溶于水且不与水反应,具有杀菌、漂白等作用,工业上可用于处理含硫离子废水。
是黄绿色气体,有毒,沸点为11℃,极易溶于水且不与水反应,具有杀菌、漂白等作用,工业上可用于处理含硫离子废水。已知:①
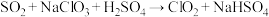 (未配平)
(未配平)②
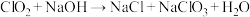 (未配平)
(未配平)某学习小组在实验室中制备
 并探究
并探究 与
与 的反应。请回答下列问题:
的反应。请回答下列问题:(1)设计如下装置制备


①装置A中反应的化学方程式为
②装置B中反应的氧化剂与还原剂的物质的量之比为
③欲收集一定量的
 ,选择上图中的装置并连接:a→g→h→
,选择上图中的装置并连接:a→g→h→(2)探究
 与
与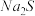 的反应
的反应将上述收集到的
 用
用 稀释以增强其稳定性,利用以下装置,将适量的稀释后的
稀释以增强其稳定性,利用以下装置,将适量的稀释后的 通入
通入 溶液中充分反应,在中得到无色澄清溶液。
溶液中充分反应,在中得到无色澄清溶液。
拟通过下列实验探究Ⅰ中反应的产物。
| 操作步骤 | 实验现象 | 结论 |
| 取少量Ⅰ中溶液放入试管甲中,滴加品红溶液和盐酸。 | 品红溶液始终不褪色 | ①无 |
另取少量Ⅰ中溶液放入试管乙中,加入 溶液和足量盐酸,振荡。 溶液和足量盐酸,振荡。 | ② | 有 生成 生成 |
另取少量Ⅰ中溶液放入试管丙中,加入 溶液至过量,静置,取少量上层清液放入试管丁中,③ 溶液至过量,静置,取少量上层清液放入试管丁中,③ | 有白色沉淀生成 | 有 生成 生成 |
 与
与 反应的离子方程式为
反应的离子方程式为(3)另一学习小组将装置A中产生的气体溶于蒸馏水,再将该水溶液滴入
 溶液中,振荡,观察到的现象是
溶液中,振荡,观察到的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】自然资源的开发是利用化学服务社会的重要努力方向。以铝土矿(主要成分为 ,含少量
,含少量 和
和 等杂质)为原料制备铝的一种工艺流程如下:
等杂质)为原料制备铝的一种工艺流程如下:

(1)“碱溶”时生成偏铝酸钠的离子方程式为_______ ,“滤渣”的成分主要是_______ (填化学式)。
(2)向“过滤I”所得滤液中加入 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为_______ 。
(3)用化学方程式表示“电解I”发生的变化_______ 。
(4)以金红石(主要成分为 为原料生产金属钛的步骤主要为:高温下,向金红石和焦炭的混合物中通入
为原料生产金属钛的步骤主要为:高温下,向金红石和焦炭的混合物中通入 ,得到
,得到 ,和一种可燃性气体,在稀有气体(如氩)氛围和加热的条件下。用
,和一种可燃性气体,在稀有气体(如氩)氛围和加热的条件下。用 和
和 ,反应可得到单质钛。请写出上述生产步骤中发生反应的化学方程式
,反应可得到单质钛。请写出上述生产步骤中发生反应的化学方程式_______ ,_______ ,稀有气体氛围的作用是_______ 。
 ,含少量
,含少量 和
和 等杂质)为原料制备铝的一种工艺流程如下:
等杂质)为原料制备铝的一种工艺流程如下:
(1)“碱溶”时生成偏铝酸钠的离子方程式为
(2)向“过滤I”所得滤液中加入
 溶液发生反应的化学方程式为
溶液发生反应的化学方程式为(3)用化学方程式表示“电解I”发生的变化
(4)以金红石(主要成分为
 为原料生产金属钛的步骤主要为:高温下,向金红石和焦炭的混合物中通入
为原料生产金属钛的步骤主要为:高温下,向金红石和焦炭的混合物中通入 ,得到
,得到 ,和一种可燃性气体,在稀有气体(如氩)氛围和加热的条件下。用
,和一种可燃性气体,在稀有气体(如氩)氛围和加热的条件下。用 和
和 ,反应可得到单质钛。请写出上述生产步骤中发生反应的化学方程式
,反应可得到单质钛。请写出上述生产步骤中发生反应的化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是______________ ;Y与过量浓硝酸反应后溶液中含有的盐的化学式为___________ 。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___ 。
A.Mg2+B.Fe2+C.Al3+D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
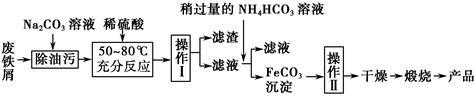
回答下列问题:
①操作Ⅰ的名称是________ ;操作Ⅱ的名称是________ ;操作Ⅱ的方法为_____________________ 。
②请写出生成FeCO3沉淀的离子方程式:____________________________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
A.Mg2+B.Fe2+C.Al3+D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:

回答下列问题:
①操作Ⅰ的名称是
②请写出生成FeCO3沉淀的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】镍催化剂的主要成分为Ni,还含有一定量Al、Fe及Fe2O3、少量其他不溶性物质,回收废镍催化剂制备硫酸镍晶体(NiSO4·7H2O)的工艺流程如下:

已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)提高“碱浸”速率的措施是_______ (任写一点即可)。
(2)“碱浸”溶解的物质是_______ 。“滤液②”可能含有的金属离子有Fe2+、Fe3+和_______ 。
(3)“转化”步骤中加入H2O2的目的是_______ ,反应的离子方程式是_______ ,选择________ (填“铁氰化钾”或“硫氰化钾”)试剂,能证明添加的H2O2已过量。
(4)“调pH”时,最适宜的pH范围是_______ 。
(5)滤液③可用于电镀镍,电镀镍时阴极反应式为_______ 。

已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Ni2+ |
| 开始沉淀的pH(c=0.01mol/L) | 2.2 | 7.5 | 7.2 |
| 沉淀完全的pH(c=1.0×10-5mol/L) | 3.2 | 9.0 | 8.7 |
(1)提高“碱浸”速率的措施是
(2)“碱浸”溶解的物质是
(3)“转化”步骤中加入H2O2的目的是
(4)“调pH”时,最适宜的pH范围是
(5)滤液③可用于电镀镍,电镀镍时阴极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)砷酸 分步电离的平衡常数(25℃)为
分步电离的平衡常数(25℃)为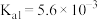 ,
,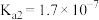 ,
,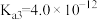 。
。 第一步水解的离子方程式为
第一步水解的离子方程式为___________ ,该步水解的平衡常数(25℃)为___________ 。
(2)以镁铝复合氧化物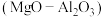 为载体的负载型镍铜双金属催化剂
为载体的负载型镍铜双金属催化剂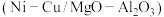 是一种新型高效加氢或脱氢催化剂,其制备流程如下:
是一种新型高效加氢或脱氢催化剂,其制备流程如下:
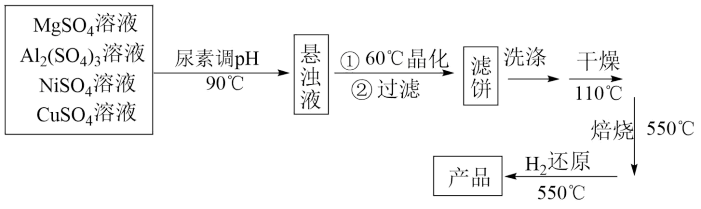
已知:常温下,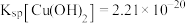 ,
,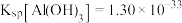 。回答下列问题:
。回答下列问题:
①在加热条件下,尿素 在水中发生水解反应,放出
在水中发生水解反应,放出___________ 和___________ 两种气体(写化学式)。
②“晶化”过程中,需保持恒温60℃,可采用的加热方式为___________
③“洗涤”过程中,检验滤饼是否洗净的方法是___________ 。
④常温下,若“悬浊液”中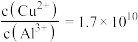 ,则溶液的
,则溶液的
___________ 。
(3)请写出泡沫灭火器灭火的原理___________ (用离子方程式表示)
(1)砷酸
 分步电离的平衡常数(25℃)为
分步电离的平衡常数(25℃)为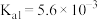 ,
,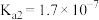 ,
,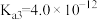 。
。 第一步水解的离子方程式为
第一步水解的离子方程式为(2)以镁铝复合氧化物
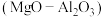 为载体的负载型镍铜双金属催化剂
为载体的负载型镍铜双金属催化剂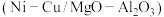 是一种新型高效加氢或脱氢催化剂,其制备流程如下:
是一种新型高效加氢或脱氢催化剂,其制备流程如下:
已知:常温下,
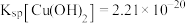 ,
,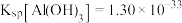 。回答下列问题:
。回答下列问题:①在加热条件下,尿素
 在水中发生水解反应,放出
在水中发生水解反应,放出②“晶化”过程中,需保持恒温60℃,可采用的加热方式为
③“洗涤”过程中,检验滤饼是否洗净的方法是
④常温下,若“悬浊液”中
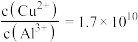 ,则溶液的
,则溶液的
(3)请写出泡沫灭火器灭火的原理
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】弱电解质的电离平衡、盐类的水解平衡均属于化学平衡。根据要求回答问题:
(1)铝盐的水解原理在生活中应用广泛,如明矾常作净水剂,其净水的原理是___________ (用离子方程式表示);如硫酸铝常作泡沫灭火器原料之一,其原理是___________ (用离子方程式表示)
(2)在氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其溶于水后加少量盐酸配制成水溶液,然后按下图所示的操作步骤进行提纯。
已知:在pH=4~5时,Cu2+、Fe2+不水解,而Fe3+几乎完全水解而沉淀
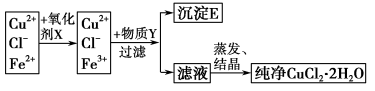
回答下列问题:
①下列物质都可以作为氧化剂,其中适合本实验的X是___________ (填字母)
A.H2O2 B.KMnO4 C.氯水 D.K2Cr2O7
②加入Y调节溶液的pH至4~5,物质Y可能是___________ (填字母)
A.氨水 B.Cu C.Cu(OH)2 D.CuO
③欲将CuCl2·2H2O加热制得无水CuCl2,可在HCl气氛下蒸发,否则得不到纯净CuCl2固体,试用简要的文字和相应化学方程式解释这样操作的原因:___
(3)常温下,浓度均为0.1mol·L-1的六种溶液的pH如下表:
①上述盐溶液中的阴离子,结合质子能力最强的是______
②根据表中数据,浓度均为0.01mol·L-1的下列五种物质的溶液中,酸性最强的是___________ (填字母);将各溶液分别稀释100倍,pH变化最小的是___________ (填字母)
A.HCN B.HClO C.H2SO4 D.CH3COOH E.H2CO3
③向NaClO溶液中通入少量二氧化碳气体,写出发生反应的离子方程式___________
(1)铝盐的水解原理在生活中应用广泛,如明矾常作净水剂,其净水的原理是
(2)在氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其溶于水后加少量盐酸配制成水溶液,然后按下图所示的操作步骤进行提纯。
已知:在pH=4~5时,Cu2+、Fe2+不水解,而Fe3+几乎完全水解而沉淀

回答下列问题:
①下列物质都可以作为氧化剂,其中适合本实验的X是
A.H2O2 B.KMnO4 C.氯水 D.K2Cr2O7
②加入Y调节溶液的pH至4~5,物质Y可能是
A.氨水 B.Cu C.Cu(OH)2 D.CuO
③欲将CuCl2·2H2O加热制得无水CuCl2,可在HCl气氛下蒸发,否则得不到纯净CuCl2固体,试用简要的文字和相应化学方程式解释这样操作的原因:
(3)常温下,浓度均为0.1mol·L-1的六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | Na2SO4 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 7.0 |
①上述盐溶液中的阴离子,结合质子能力最强的是
②根据表中数据,浓度均为0.01mol·L-1的下列五种物质的溶液中,酸性最强的是
A.HCN B.HClO C.H2SO4 D.CH3COOH E.H2CO3
③向NaClO溶液中通入少量二氧化碳气体,写出发生反应的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(化学---选修3:物质结构和性质)锂—磷酸氧铜电池正极的的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的核外电子排布式:____________,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有___________(填元素符号),上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为________________。
(2)PO43-的空间构型是___________。
(3)与NH3具有相同空间构型和键合形成的分子或离子有_________、___________(各举一例)
(4)氨基乙酸铜的分子结构如图,氮原子的杂化方式为______________。
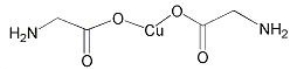
(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1molCN-中含有的π键的数目为___________。
(6)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式
为______________________。
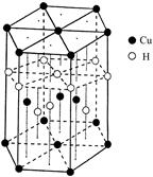
(7)铜晶体为面心立方最密堆积,铜的原子半径为127.8pm,列出晶体铜的密度表达式____________。
(1)写出基态Cu2+的核外电子排布式:____________,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有___________(填元素符号),上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为________________。
(2)PO43-的空间构型是___________。
(3)与NH3具有相同空间构型和键合形成的分子或离子有_________、___________(各举一例)
(4)氨基乙酸铜的分子结构如图,氮原子的杂化方式为______________。

(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1molCN-中含有的π键的数目为___________。
(6)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式
为______________________。

(7)铜晶体为面心立方最密堆积,铜的原子半径为127.8pm,列出晶体铜的密度表达式____________。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】2020年12月17日凌晨1时59分,“嫦娥五号”首次实现了我国地外天体采样返回目标,标志着我国航天事业迈出了一大步。带回的月壤中包含了H、O、N、Al、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。回答下列问题:

(1) 极易溶于水的原因是
极易溶于水的原因是___________ 。
(2) 的结构如图所示。则该离子中
的结构如图所示。则该离子中 键与
键与 键的个数比为
键的个数比为___________ 。
(3) 中配体分子
中配体分子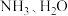 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。

 的键角小于
的键角小于 的键角,原因是
的键角,原因是___________ 。
(4)冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并且随着环的大小不同而与不同金属离子作用。

① 与X的空腔大小相近,恰好能进入到X的环内,且与氧原子的一对孤电子对作用形成如图所示的稳定结构W。W中
与X的空腔大小相近,恰好能进入到X的环内,且与氧原子的一对孤电子对作用形成如图所示的稳定结构W。W中 与孤对电子之间的作用属于
与孤对电子之间的作用属于___________ (填标号)。
A.离子键 B.金属键 C.氢键 D.配位键
②冠醚Y能与 形成稳定结构,但不能与
形成稳定结构,但不能与 形成稳定结构,理由是
形成稳定结构,理由是___________ 。
(5)已知 与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子的化学式为
与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子的化学式为___________ ,阴离子的空间构型为___________ 。

(6)已知TiN晶体的晶胞结构如图所示,若该晶胞中Ti原子与N原子的最近距离为apm,阿伏加德罗常数的值为 ,则晶胞的密度为
,则晶胞的密度为___________  。[
。[ ,用含a、
,用含a、 的代数式表示]。
的代数式表示]。


(1)
 极易溶于水的原因是
极易溶于水的原因是(2)
 的结构如图所示。则该离子中
的结构如图所示。则该离子中 键与
键与 键的个数比为
键的个数比为(3)
 中配体分子
中配体分子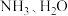 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。
 的键角小于
的键角小于 的键角,原因是
的键角,原因是(4)冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并且随着环的大小不同而与不同金属离子作用。

①
 与X的空腔大小相近,恰好能进入到X的环内,且与氧原子的一对孤电子对作用形成如图所示的稳定结构W。W中
与X的空腔大小相近,恰好能进入到X的环内,且与氧原子的一对孤电子对作用形成如图所示的稳定结构W。W中 与孤对电子之间的作用属于
与孤对电子之间的作用属于A.离子键 B.金属键 C.氢键 D.配位键
②冠醚Y能与
 形成稳定结构,但不能与
形成稳定结构,但不能与 形成稳定结构,理由是
形成稳定结构,理由是(5)已知
 与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子的化学式为
与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子的化学式为
(6)已知TiN晶体的晶胞结构如图所示,若该晶胞中Ti原子与N原子的最近距离为apm,阿伏加德罗常数的值为
 ,则晶胞的密度为
,则晶胞的密度为 。[
。[ ,用含a、
,用含a、 的代数式表示]。
的代数式表示]。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.
(1)基态砷原子的电子排布式为 .
(2)K3[Fe(CN)5]晶体中Fe3+与CN﹣之间的化学键类型为 键,与CN﹣互为等电子体的化合物的分子式为 .
(3)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B﹣N﹣B之间的夹角是 (填角度).
(4)对硝基苯酚水合物(化学式为C4H5NO3•1.5H2O)是一种含氮化合物.实验表明:加热至94℃时该晶体会失去结晶水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性.
①该晶体中四种基本元素的电负性由大到小的顺序是 .
②对硝基苯酚分子中氮原子的杂化轨道类型是 .
(5)磷化硼(BP)是一种有价值的耐磨硬涂层材料,这种陶瓷材料可作为金属表面的保护薄膜,它是通过在高温(T>750℃)氢气氛围下三溴化硼和三溴化磷反应制得的,三溴化硼分子的空间构型为 ,BP晶胞的结构如图所示,当晶胞晶格参数为478pm(即图中立方体的每条边长为478pm)时,磷化硼中硼原子和磷原子之间的最近距离为 .

(1)基态砷原子的电子排布式为 .
(2)K3[Fe(CN)5]晶体中Fe3+与CN﹣之间的化学键类型为 键,与CN﹣互为等电子体的化合物的分子式为 .
(3)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B﹣N﹣B之间的夹角是 (填角度).
(4)对硝基苯酚水合物(化学式为C4H5NO3•1.5H2O)是一种含氮化合物.实验表明:加热至94℃时该晶体会失去结晶水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性.
①该晶体中四种基本元素的电负性由大到小的顺序是 .
②对硝基苯酚分子中氮原子的杂化轨道类型是 .
(5)磷化硼(BP)是一种有价值的耐磨硬涂层材料,这种陶瓷材料可作为金属表面的保护薄膜,它是通过在高温(T>750℃)氢气氛围下三溴化硼和三溴化磷反应制得的,三溴化硼分子的空间构型为 ,BP晶胞的结构如图所示,当晶胞晶格参数为478pm(即图中立方体的每条边长为478pm)时,磷化硼中硼原子和磷原子之间的最近距离为 .

您最近一年使用:0次

 和
和 和
和 溶液,设三者中的一种为A试剂,则其他为B,C.现将B溶液滴入A中,有蓝色沉淀生成,并有时带有绿色沉淀,将B滴入C中则有气体生成。
溶液,设三者中的一种为A试剂,则其他为B,C.现将B溶液滴入A中,有蓝色沉淀生成,并有时带有绿色沉淀,将B滴入C中则有气体生成。

