下列分子结构图中的“○”表示氢原子,“●”表示短周期中相邻的三种元素原子。小黑点表示没有形成共价键的最外层电子,短线表示共价键。

(1)以上分子中,中心原子采用 杂化的是
杂化的是_____ (填化学式)。
(2)③的分子中有_____ 个 键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的
键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的_____ 键(填“ ”或“
”或“ ),形成的是
),形成的是_____ 键(填“ ”或“
”或“ ”)。
”)。
(3)4种分子中,属于极性分子的是_____ (填序号,下同)。键角由大到小的顺序是_____ ,能结合质子(即 )形成稳定离子的是
)形成稳定离子的是_____ 。
(4)已知液态①和④相似,也可发生微弱的电离,电离出含有相同电子数的微粒,则①的电离方程式为_____ 。

(1)以上分子中,中心原子采用
 杂化的是
杂化的是(2)③的分子中有
 键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的
键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的 ”或“
”或“ ),形成的是
),形成的是 ”或“
”或“ ”)。
”)。(3)4种分子中,属于极性分子的是
 )形成稳定离子的是
)形成稳定离子的是(4)已知液态①和④相似,也可发生微弱的电离,电离出含有相同电子数的微粒,则①的电离方程式为
更新时间:2024-01-17 20:04:28
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】肼(N2H4)是一种重要的火箭燃料。
(1)已知水电离成H3O+和OH-叫做水的自偶电离。同水一样,N2H4也有微弱的自偶电离,自偶电离的方程式为:_______ 。
(2)已知NH3为一元碱,N2H4为二元碱,N2H4在水溶液中的一级电离方程式可表示为N2H4•H2O N2H
N2H +OH—,N2H4的二级电离方程式
+OH—,N2H4的二级电离方程式_______ 。
(1)已知水电离成H3O+和OH-叫做水的自偶电离。同水一样,N2H4也有微弱的自偶电离,自偶电离的方程式为:
(2)已知NH3为一元碱,N2H4为二元碱,N2H4在水溶液中的一级电离方程式可表示为N2H4•H2O
 N2H
N2H +OH—,N2H4的二级电离方程式
+OH—,N2H4的二级电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】实验表明,液态时,纯硫酸的电离能力强于硝酸,纯硫酸的导电性也显著强于纯水。已知液态纯酸都能像水那样进行自身电离H2O+H2O H3O++OH-而建立平衡,且在一定温度下都有各自的离子积常数。纯硫酸在液态时自身电离的方程式是
H3O++OH-而建立平衡,且在一定温度下都有各自的离子积常数。纯硫酸在液态时自身电离的方程式是_______ ,纯硝酸的离子积常数表达式为K(HNO3)=_______ 。
 H3O++OH-而建立平衡,且在一定温度下都有各自的离子积常数。纯硫酸在液态时自身电离的方程式是
H3O++OH-而建立平衡,且在一定温度下都有各自的离子积常数。纯硫酸在液态时自身电离的方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮原子核外电子排布式为______________ ,有3个未成对电子,当结合成分子时, _________ 轨道“________ ”方式重叠,______________________ 轨道“__________ ”方式重叠,我们把原子轨道间沿核间连线方向以“头碰头”方式重叠形成的共价键叫σ键;原子轨道在核间连线两侧以“肩并肩”的方式重叠形成的共价键叫π键。所以在N2分子中有______ 个σ键和______ 个π键。结构式为______________ ,电子式为____________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.双氰胺结构简式如图。
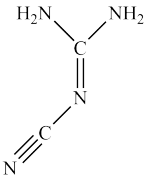
(1)双氰胺的晶体类型为_______ 。
(2)双氰胺所含元素中,_______ (填元素名称)元素基态原子核外未成对电子数最多。
(3)双氰胺分子中σ键和π键数目之比为_______ 。
Ⅱ.硼的最简单氢化物——乙硼烷球棍模型如下图,由它制取硼氢化锂的反应为2LiH+B2H6=2LiBH4
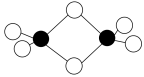
(4)乙硼烷分子中硼原子的杂化轨道类型为_______ 。
(5)BH 为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为
为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为_______ (填序号)。
A.离子键 B.金属键 C.氢键 D.配位键 E.极性键 F.非极性键
(6)根据以上反应判断,其中涉及元素的电负性从小到大的顺序为_______ (填元素符号)。
(7)碳的最简单氢化物是CH4,而硼的最简单氢化物不是BH3,其原因为_______ 。

(1)双氰胺的晶体类型为
(2)双氰胺所含元素中,
(3)双氰胺分子中σ键和π键数目之比为
Ⅱ.硼的最简单氢化物——乙硼烷球棍模型如下图,由它制取硼氢化锂的反应为2LiH+B2H6=2LiBH4

(4)乙硼烷分子中硼原子的杂化轨道类型为
(5)BH
 为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为
为正四面体结构,LiBH4中硼原子和氢原子之间的化学键为A.离子键 B.金属键 C.氢键 D.配位键 E.极性键 F.非极性键
(6)根据以上反应判断,其中涉及元素的电负性从小到大的顺序为
(7)碳的最简单氢化物是CH4,而硼的最简单氢化物不是BH3,其原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下列反应曾用于检测司机是否酒后驾驶:2Cr2O + 3CH3CH2OH + 16H+ + 13H2O→4[Cr(H2O)6]3+ + 3CH3COOH
+ 3CH3CH2OH + 16H+ + 13H2O→4[Cr(H2O)6]3+ + 3CH3COOH
(1)Cr基态核外价电子排布式为_______ ; 配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是_______ (填元素符号)。
(2)CH3COOH中C原子轨道杂化类型为_______ ,1mol CH3COOH含有的σ键的数目为_______ 。
(3)与H2O互为等电子体的一种阳离子为_______ (填化学式); H2O与CH3CH2OH可以任意比例互溶,除因为它们都是极性分子外,还因为_______ 。
 + 3CH3CH2OH + 16H+ + 13H2O→4[Cr(H2O)6]3+ + 3CH3COOH
+ 3CH3CH2OH + 16H+ + 13H2O→4[Cr(H2O)6]3+ + 3CH3COOH(1)Cr基态核外价电子排布式为
(2)CH3COOH中C原子轨道杂化类型为
(3)与H2O互为等电子体的一种阳离子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以合成诸多化合物。
(1)乙炔的电子式为___________ 。
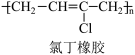
(2)以乙炔为原料可制氯丁橡胶,其过程包括如下反应:

①已知A的分子式为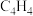 ,A的结构简式为
,A的结构简式为___________ 。
②用系统命名法为B命名,则B的名称为___________ 。
③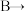 氯丁橡胶的反应的化学方程式为
氯丁橡胶的反应的化学方程式为___________ 。
(3)聚丙烯腈俗称人造羊毛,以乙炔为原料制聚丙烯腈的过程包括如下反应:

①M的化学式为___________ ;
②C的结构简式为___________ ,分子中碳原子的杂化方式为___________ 。
(1)乙炔的电子式为
(2)以乙炔为原料可制氯丁橡胶,其过程包括如下反应:


①已知A的分子式为
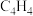 ,A的结构简式为
,A的结构简式为②用系统命名法为B命名,则B的名称为
③
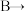 氯丁橡胶的反应的化学方程式为
氯丁橡胶的反应的化学方程式为(3)聚丙烯腈俗称人造羊毛,以乙炔为原料制聚丙烯腈的过程包括如下反应:

①M的化学式为
②C的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】无机物可根据其组成和性质进行分类。现有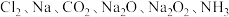 六种物质,完成下列填空:
六种物质,完成下列填空:
(1)由分子构成的单质是
(2)既有离子键又有共价键的物质的电子式为
(3)上述化合物中组成元素的原子半径由大到小的顺序是
(4)
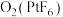 是离子化合物,其中
是离子化合物,其中 为
为 价。正确判断是___________。
价。正确判断是___________。| A.常温下为固体 | B.不存在共价键 | C.属于极性分子 | D.由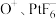 构成 构成 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】乙烯在空气中燃烧的化学方程式是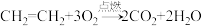 。回答下列问题:
。回答下列问题:
(1)CH2=CH2分子为_______ (填“极性”或“非极性)分子,一个CH2=CH2分子中含有的σ键为_______ 个。
(2)CO2分子中,碳原子的杂化方式是_______ ,分子的立体构型名称是_______ 。
(3)在第VIA族元素的简单氢化物中,H2O的沸点最高,原因是:_______ 。
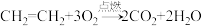 。回答下列问题:
。回答下列问题:(1)CH2=CH2分子为
(2)CO2分子中,碳原子的杂化方式是
(3)在第VIA族元素的简单氢化物中,H2O的沸点最高,原因是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知N、P同属于元素周期表的第ⅤA族元素,N在第二周期,P在第三周期。 分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是
分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是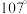 。
。
(1) 分子的空间结构为
分子的空间结构为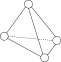 ,它是一种
,它是一种_____ (填“极性”或“非极性”)分子。
(2) 分子与
分子与 分子的构型关系
分子的构型关系_____ (填“相同”“相似”或“不相似”),P—H键_____ (填“有”或“无”)极性, 分子
分子_______ (填“有”或“无”)极性。
(3) 是一种淡黄色油状液体,下列对
是一种淡黄色油状液体,下列对 的有关描述不正确的是
的有关描述不正确的是___ (填字母)。
a.该分子呈平面三角形
b.该分子中的化学键为极性键
c.该分子为极性分子
d.因N—Cl键的键能大,故 稳定
稳定
 分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是
分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是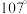 。
。(1)
 分子的空间结构为
分子的空间结构为 ,它是一种
,它是一种(2)
 分子与
分子与 分子的构型关系
分子的构型关系 分子
分子(3)
 是一种淡黄色油状液体,下列对
是一种淡黄色油状液体,下列对 的有关描述不正确的是
的有关描述不正确的是a.该分子呈平面三角形
b.该分子中的化学键为极性键
c.该分子为极性分子
d.因N—Cl键的键能大,故
 稳定
稳定
您最近一年使用:0次

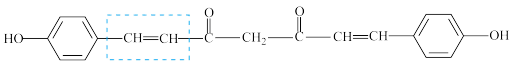
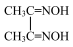 )作用生成腥红色配合物沉淀A。丁二酮肟分子中碳原子的杂化轨道类型有
)作用生成腥红色配合物沉淀A。丁二酮肟分子中碳原子的杂化轨道类型有

