黑火药的主要成分为木炭(C)、硫黄(S)和火硝 。请回答下列问题。
。请回答下列问题。
(1)基态碳原子的电子排布式为_______ 。
(2)下列轨道表示式能表示基态氮原子的核外电子排布的是_______(填标号)。
(3)C、N、O三种元素的第一电离能由大到小的顺序为_______ 。
(4)Se元素位于第4周期,与O、S同主族。
①基态Se原子中具有_______ 种运动状态不同的电子。其中能量最高的电子占据轨道的形状为_______ 。
②O、S、Se三种元素的电负性依次_______ (填“增大”或“减小”)。
(5)用铂丝蘸取 溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是
溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是_______ 。第4周期元素的基态原子中,与基态K原子具有相同最外层电子数的是_______ (填元素符号)。
 。请回答下列问题。
。请回答下列问题。(1)基态碳原子的电子排布式为
(2)下列轨道表示式能表示基态氮原子的核外电子排布的是_______(填标号)。
A.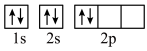 | B.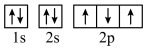 |
C.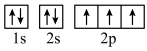 | D.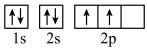 |
(3)C、N、O三种元素的第一电离能由大到小的顺序为
(4)Se元素位于第4周期,与O、S同主族。
①基态Se原子中具有
②O、S、Se三种元素的电负性依次
(5)用铂丝蘸取
 溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是
溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,从微观角度解释产生该现象的原因是
更新时间:2024-01-22 17:20:43
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】 是一种化工原料,可以制备多种物质,如下图所示
是一种化工原料,可以制备多种物质,如下图所示

请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式为_____ ;氢气在氯气中燃烧的现象是_____ 。
(2) 与
与 反应的化学方程式为
反应的化学方程式为_____ ;反应生成的_____ (填名称)是漂白粉的有效成分。
(3)灼烧 时,呈现的火焰颜色为
时,呈现的火焰颜色为_____ ;
写出 溶液与Na反应的离子方程式
溶液与Na反应的离子方程式_____ 。
写出 溶液与
溶液与 反应的离子方程式
反应的离子方程式_____ 。
(4)写出 受热分解的化学方程式
受热分解的化学方程式_____ 。
 是一种化工原料,可以制备多种物质,如下图所示
是一种化工原料,可以制备多种物质,如下图所示
请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式为
(2)
 与
与 反应的化学方程式为
反应的化学方程式为(3)灼烧
 时,呈现的火焰颜色为
时,呈现的火焰颜色为写出
 溶液与Na反应的离子方程式
溶液与Na反应的离子方程式写出
 溶液与
溶液与 反应的离子方程式
反应的离子方程式(4)写出
 受热分解的化学方程式
受热分解的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具。如图是钠的价类二维图:
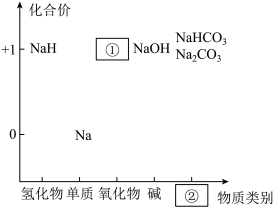
(1)②处应填的物质类别为_____ 。
(2)某同学欲进行钠在空气中燃烧的实验,可将钠放入_____ (填字母)中进行加热。
A.蒸发皿 B.坩埚 C.烧杯
(3)如图在盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,观察到的现象是_____ (填字母)。发生反应的离子方程式为_____ 。
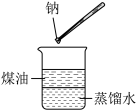
A.钠在水层中反应并四处游动 B.钠停留在煤油层中不发生反应
C.钠在煤油的液面上反应并四处游动 D.钠在煤油与水的界面处反应并上下跳动
(4)若①是一种淡黄色固体,其在呼吸面具中作供氧剂的原理是_____ (用化学方程式表示)。
(5)用洁净的铂丝蘸取碳酸钠溶液进行焰色试验,火焰呈_____ 色。
(6)利用如图装置可实现NaHCO3向Na2CO3的转化,试管中发生反应的化学方程式为_____ ,利用该反应NaHCO3在生活中可用于_____ 。


(1)②处应填的物质类别为
(2)某同学欲进行钠在空气中燃烧的实验,可将钠放入
A.蒸发皿 B.坩埚 C.烧杯
(3)如图在盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,观察到的现象是

A.钠在水层中反应并四处游动 B.钠停留在煤油层中不发生反应
C.钠在煤油的液面上反应并四处游动 D.钠在煤油与水的界面处反应并上下跳动
(4)若①是一种淡黄色固体,其在呼吸面具中作供氧剂的原理是
(5)用洁净的铂丝蘸取碳酸钠溶液进行焰色试验,火焰呈
(6)利用如图装置可实现NaHCO3向Na2CO3的转化,试管中发生反应的化学方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】立德粉 (也称锌钡白),是一种常用白色颜料。回答下列问题:
(也称锌钡白),是一种常用白色颜料。回答下列问题:
(1)利用焰色试验的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧立德粉样品时,钡的焰色为___________ (填标号)。
A.黄色B.红色C.紫色D.绿色
(2)以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:

在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为___________ 。回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO2和一种清洁能源气体,该反应的化学方程式为___________ 。
 (也称锌钡白),是一种常用白色颜料。回答下列问题:
(也称锌钡白),是一种常用白色颜料。回答下列问题:(1)利用焰色试验的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧立德粉样品时,钡的焰色为
A.黄色B.红色C.紫色D.绿色
(2)以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:

在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请在标有序号的空白处填空。
(1)可正确表示原子轨道的是_____ 。
A.2s B.2d C.3Px D.3f
(2)写出基态镓(31Ga)原子的电子排布式:__________________ 。
(3)下列物质变化,只与范德华力有关的是__________ 。
A.干冰熔化 B.乙酸汽化 C.乙醇溶于水 D.碘溶于四氯化碳
(4)下列物质中,只含有极性键的分子是___________ ,既含离子键又含共价键的化合物是_______ ;只存在σ键的分子是________ ,同时存在σ键和π键的分子是_____ 。
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl
(5)Na、Mg、Al第一电离能的由大到小的顺序:__________________ ;
(1)可正确表示原子轨道的是
A.2s B.2d C.3Px D.3f
(2)写出基态镓(31Ga)原子的电子排布式:
(3)下列物质变化,只与范德华力有关的是
A.干冰熔化 B.乙酸汽化 C.乙醇溶于水 D.碘溶于四氯化碳
(4)下列物质中,只含有极性键的分子是
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl
(5)Na、Mg、Al第一电离能的由大到小的顺序:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E代表五种元素,请填空:
(1)A元素基态原子的最外层有2个未成对电子和1个空轨道,次外层有两个电子,A元素原子价电子的轨道表示式为___________ 。
(2)B元素的带一个单位负电荷的简单离子和C元素带一个单位正电荷的简单离子的电子层结构都与氩相同,B与C形成的化合物的化学式为___________ 。
(3)D为过渡金属元素,其+1价简单离子的3d轨道为全充满状态,D的元素符号为___________ ,其基态原子的价电子排布式为___________ ,D在元素周期表分区中属于___________ 区。
(4)E元素基态原子的M层全充满,N层有4个电子,其基态原子的简化核外电子排布式为___________ 。
(1)A元素基态原子的最外层有2个未成对电子和1个空轨道,次外层有两个电子,A元素原子价电子的轨道表示式为
(2)B元素的带一个单位负电荷的简单离子和C元素带一个单位正电荷的简单离子的电子层结构都与氩相同,B与C形成的化合物的化学式为
(3)D为过渡金属元素,其+1价简单离子的3d轨道为全充满状态,D的元素符号为
(4)E元素基态原子的M层全充满,N层有4个电子,其基态原子的简化核外电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】三聚氰胺可以用以下三个反应合成:CaO+3C=CaC2+CO↑,CaC2+N2=CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排
布式:_____________________________________________ 。
CaCN2中阴离子为CN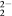 ,与CN
,与CN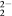 互为等电子体的分子有
互为等电子体的分子有________ (填两种化学式),由此可以推知CN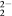 的空间构型为
的空间构型为________ ,画出CN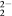 电子式
电子式___________ 。
(2)尿素分子中C原子采取________ 杂化。尿素分子的结构简式是________ 。
(3)三聚氰胺(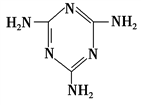 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(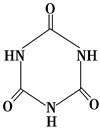 )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过________ 结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________ 。CaO晶体和NaCl晶体的晶格能分别为:CaO 3401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是______________ 。

(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排
布式:
CaCN2中阴离子为CN
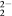 ,与CN
,与CN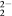 互为等电子体的分子有
互为等电子体的分子有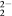 的空间构型为
的空间构型为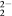 电子式
电子式(2)尿素分子中C原子采取
(3)三聚氰胺(
 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸( )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题
(1)基态硫原子核外电子的空间运动状态有___________ 种;其核外电子运动最高能级的电子云轮廓图的形状为___________ 。
(2)基态砷原子的价层电子的轨道表示式为___________ 。
(3)元素Mg的第一电离能大于Al的第一电离能的原因是___________ 。
(4)硫化氢和水分子结构相似,硫化氢晶体中,一个硫化氢分子周围有12个紧邻分子,而冰中一个水分子周围只有4个紧邻分子,原因为:___________ 。
(5) 是离子晶体,其晶格能可通过图(a)的Born−Haber循环计算得到。
是离子晶体,其晶格能可通过图(a)的Born−Haber循环计算得到。

可知,Li原子的第一电离能为___________  ,
, 键键能为
键键能为___________ 
(6) 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ ,键角由大到小的顺序为___________ ,已知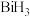 的沸点高于
的沸点高于 ,其原因是
,其原因是___________ 。
(1)基态硫原子核外电子的空间运动状态有
(2)基态砷原子的价层电子的轨道表示式为
(3)元素Mg的第一电离能大于Al的第一电离能的原因是
(4)硫化氢和水分子结构相似,硫化氢晶体中,一个硫化氢分子周围有12个紧邻分子,而冰中一个水分子周围只有4个紧邻分子,原因为:
(5)
 是离子晶体,其晶格能可通过图(a)的Born−Haber循环计算得到。
是离子晶体,其晶格能可通过图(a)的Born−Haber循环计算得到。
可知,Li原子的第一电离能为
 ,
, 键键能为
键键能为
(6)
 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为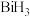 的沸点高于
的沸点高于 ,其原因是
,其原因是
您最近一年使用:0次
【推荐3】铁(Fe)钴(Co)镍(Ni)合金是一种典型的软磁材料,具有优异的磁导率和饱和磁感应强度,可用于电感器、传感器和电磁设备等领域。
(1)中国古代就对磁性材料有研究,四大发明之一的司南是由天然磁石制成的,其主要成分是___________ (选填编号)。
a.Fe b.FeO c. d.
d.
(2)铁的原子结构示意图为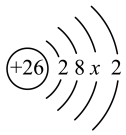 。由此可知,铁是第
。由此可知,铁是第___________ 周期元素,铁原子核外3d轨道上共填充了___________ 个电子。
(3)钴(Co)元素基态原子的电子排布式为___________ ,处于元素周期表的___________ 区。
(4)基态镍(Ni)原子的价电子轨道表示式为___________ 。
(5)磁性材料原子中的未配对电子对其磁性起主要作用,含 磁性材料的磁性比含
磁性材料的磁性比含 的更强,试从结构角度分析原因
的更强,试从结构角度分析原因___________ 。
(6)与Fe、Co、Ni同周期的铜、锌两种元素的第一电离能( ),第二电离能(
),第二电离能( )数据如下表所示:
)数据如下表所示:
请解释铜的 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是___________ 。
(1)中国古代就对磁性材料有研究,四大发明之一的司南是由天然磁石制成的,其主要成分是
a.Fe b.FeO c.
 d.
d.
(2)铁的原子结构示意图为
 。由此可知,铁是第
。由此可知,铁是第(3)钴(Co)元素基态原子的电子排布式为
(4)基态镍(Ni)原子的价电子轨道表示式为
(5)磁性材料原子中的未配对电子对其磁性起主要作用,含
 磁性材料的磁性比含
磁性材料的磁性比含 的更强,试从结构角度分析原因
的更强,试从结构角度分析原因(6)与Fe、Co、Ni同周期的铜、锌两种元素的第一电离能(
 ),第二电离能(
),第二电离能( )数据如下表所示:
)数据如下表所示:电离能/(kJ·mol ) ) |  |  |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有___________ 种。
(2)O、F、Cl电负性最小的是___________ ;HClO的电子式为___________ ;OF2的沸点低于Cl2O,原因是___________ 。
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为___________ 。XeF2与水反应时放出氧气和氙气,氟以化合态留在溶液中,该反应的化学方程式为___________ 。
(1)基态F原子核外电子的运动状态有
(2)O、F、Cl电负性最小的是
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】哈尔滨工业大学的李惠等人和加州大学洛杉矶分校的黄昱、段镶锋合作合成了具备超轻、高力学强度和超级隔热三大特点的氮化硼(hBNAGs)以及碳化硅( -SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
-SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
(1)硅原子的价电子排布图为___________ 。B、N、O、Al的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(2)硼元素深受配位化学家的喜爱,其原因在于B容易与配体形成配位键,如BF 。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O
。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O H+ + [B(OH)4]−。
H+ + [B(OH)4]−。
① 从原子结构分析B容易与配体形成配位键的原因___________ 。
② 下列有关硼酸及其相关化合物的说法正确的是___________ (填标号)。
A.硼酸的电离过程中有配位键形成
B.硼酸为三元酸
C.Na[B(OH)4]的水溶液呈碱性
D.硼酸和[B(OH)4]−中的键角相同
(3)氨硼烷(NH3BH3)具有良好的储氢能力。已知B、N、H三种元素的电负性如下:
① 下列有关氨硼烷(NH3BH3)的说法中错误的是___________ (填标号)。
A.H元素为+1价
B.氨硼烷中有配位键
C.N和B原子均为sp3杂化
D.氨硼烷在一定条件下能与水反应产生氢气
② 氨硼烷的电子式为___________ ,氨硼烷中H−N−H的键角___________ (填“>”“<”或“=”)H−B−H的键角。
 -SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
-SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:(1)硅原子的价电子排布图为
(2)硼元素深受配位化学家的喜爱,其原因在于B容易与配体形成配位键,如BF
 。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O
。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O H+ + [B(OH)4]−。
H+ + [B(OH)4]−。① 从原子结构分析B容易与配体形成配位键的原因
② 下列有关硼酸及其相关化合物的说法正确的是
A.硼酸的电离过程中有配位键形成
B.硼酸为三元酸
C.Na[B(OH)4]的水溶液呈碱性
D.硼酸和[B(OH)4]−中的键角相同
(3)氨硼烷(NH3BH3)具有良好的储氢能力。已知B、N、H三种元素的电负性如下:
| 元素符号 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
① 下列有关氨硼烷(NH3BH3)的说法中错误的是
A.H元素为+1价
B.氨硼烷中有配位键
C.N和B原子均为sp3杂化
D.氨硼烷在一定条件下能与水反应产生氢气
② 氨硼烷的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】雌黄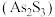 和雄黄
和雄黄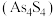 是一对共生矿物,有“矿物鸳鸯”的说法。我国古代书画家曾用其作绘画颜料,因有抗病毒疗效,故在中医治疗中也有非常广泛的用途。
是一对共生矿物,有“矿物鸳鸯”的说法。我国古代书画家曾用其作绘画颜料,因有抗病毒疗效,故在中医治疗中也有非常广泛的用途。
(1)基态砷原子电子排布式为__________ ,砷元素位于周期表的位置__________ 。
(2)同主族元素N、P、As,第一电离能最大的为__________ ;同周期元素Si、P、S,电负性最小的为__________ 。
(3)雌黄可以转化为用于治疗白血病的亚砷酸 ,亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示:
,亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示:
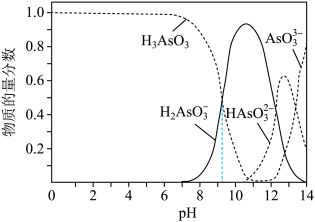
①人体血液的pH为7.35~7.45,用药后人体所含砷元素的主要微粒是__________ 。
②将KOH溶液滴入 溶液中,当pH从11调至12时,反应的离子方程式是
溶液中,当pH从11调至12时,反应的离子方程式是__________ 。
③ 的数量级是
的数量级是_______ 。
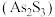 和雄黄
和雄黄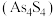 是一对共生矿物,有“矿物鸳鸯”的说法。我国古代书画家曾用其作绘画颜料,因有抗病毒疗效,故在中医治疗中也有非常广泛的用途。
是一对共生矿物,有“矿物鸳鸯”的说法。我国古代书画家曾用其作绘画颜料,因有抗病毒疗效,故在中医治疗中也有非常广泛的用途。(1)基态砷原子电子排布式为
(2)同主族元素N、P、As,第一电离能最大的为
(3)雌黄可以转化为用于治疗白血病的亚砷酸
 ,亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示:
,亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示:
①人体血液的pH为7.35~7.45,用药后人体所含砷元素的主要微粒是
②将KOH溶液滴入
 溶液中,当pH从11调至12时,反应的离子方程式是
溶液中,当pH从11调至12时,反应的离子方程式是③
 的数量级是
的数量级是
您最近一年使用:0次



