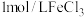某化学兴趣小组探究 溶液与
溶液与 的反应历程。
的反应历程。
Ⅰ.药品制备。
(1)实验室制备 的装置如图,仪器a中的试剂是
的装置如图,仪器a中的试剂是__________ 。 溶液的方法是
溶液的方法是__________ 。
Ⅱ.探究 溶液与
溶液与 的反应
的反应
(3)兴趣小组预测, 能使
能使 溶液由黄色变为浅绿色,反应的离子方程式为
溶液由黄色变为浅绿色,反应的离子方程式为__________ 。
向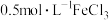 溶液中通入
溶液中通入 至饱和后,用橡皮塞封闭试管,观察到溶液由黄色迅速变为血红色,静置
至饱和后,用橡皮塞封闭试管,观察到溶液由黄色迅速变为血红色,静置 后变回黄色,静置
后变回黄色,静置 后,变为浅绿色。
后,变为浅绿色。
查阅资料:血红色物质可能与 饱和溶液中的主要微粒:
饱和溶液中的主要微粒: 、
、 、
、 、
、 、
、 有关。
有关。
①取少量上述血红色溶液,立即滴加几滴 溶液A,溶液又褪为黄色。据此推测:红色物质的产生与
溶液A,溶液又褪为黄色。据此推测:红色物质的产生与 无关。物质A的化学式为
无关。物质A的化学式为__________ 。
②向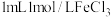 溶液中滴加
溶液中滴加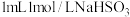 溶液,溶液变为血红色,滴加几滴
溶液,溶液变为血红色,滴加几滴 溶液A,褪成黄色。据此推测:红色物质的产生与
溶液A,褪成黄色。据此推测:红色物质的产生与 和
和 无关,主要与
无关,主要与 或
或 有关。
有关。
③利用分光光度仪测定红色物质的浓度(吸光度越高,浓度越大),实验数据如下:
结论:溶液变血红色的主要原因是 和
和__________ 发生配合反应。
(5)由以上探究结果说明该条件下, 与
与 溶液反应的活化能:配合反应
溶液反应的活化能:配合反应__________ (填“大于”“小于”“等于”)氧化还原反应。
(6)兴趣小组在某次实验中,通入 后未封闭试管,发现血红色更快变回黄色。其可能原因是
后未封闭试管,发现血红色更快变回黄色。其可能原因是__________ (用离子方程式表示)。
 溶液与
溶液与 的反应历程。
的反应历程。Ⅰ.药品制备。
(1)实验室制备
 的装置如图,仪器a中的试剂是
的装置如图,仪器a中的试剂是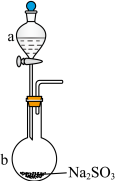
 溶液的方法是
溶液的方法是Ⅱ.探究
 溶液与
溶液与 的反应
的反应(3)兴趣小组预测,
 能使
能使 溶液由黄色变为浅绿色,反应的离子方程式为
溶液由黄色变为浅绿色,反应的离子方程式为向
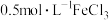 溶液中通入
溶液中通入 至饱和后,用橡皮塞封闭试管,观察到溶液由黄色迅速变为血红色,静置
至饱和后,用橡皮塞封闭试管,观察到溶液由黄色迅速变为血红色,静置 后变回黄色,静置
后变回黄色,静置 后,变为浅绿色。
后,变为浅绿色。
查阅资料:血红色物质可能与
 饱和溶液中的主要微粒:
饱和溶液中的主要微粒: 、
、 、
、 、
、 、
、 有关。
有关。①取少量上述血红色溶液,立即滴加几滴
 溶液A,溶液又褪为黄色。据此推测:红色物质的产生与
溶液A,溶液又褪为黄色。据此推测:红色物质的产生与 无关。物质A的化学式为
无关。物质A的化学式为②向
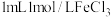 溶液中滴加
溶液中滴加 溶液,溶液变为血红色,滴加几滴
溶液,溶液变为血红色,滴加几滴 溶液A,褪成黄色。据此推测:红色物质的产生与
溶液A,褪成黄色。据此推测:红色物质的产生与 和
和 无关,主要与
无关,主要与 或
或 有关。
有关。③利用分光光度仪测定红色物质的浓度(吸光度越高,浓度越大),实验数据如下:
| 吸光度 | ||
|
|
| |
0.5 | 4.0 | 0.0 | 0.412 |
0.5 | 3.6 | 0.4 | 0.359 |
0.5 | 3.2 | 0.8 | 0.331 |
0.5 | 2.8 | 1.2 | 0.297 |
 和
和(5)由以上探究结果说明该条件下,
 与
与 溶液反应的活化能:配合反应
溶液反应的活化能:配合反应(6)兴趣小组在某次实验中,通入
 后未封闭试管,发现血红色更快变回黄色。其可能原因是
后未封闭试管,发现血红色更快变回黄色。其可能原因是
23-24高三上·辽宁沈阳·阶段练习 查看更多[2]
辽宁省沈阳市第一二0中学2023-2024学年高三上学期第五次质量监测化学试题(已下线)大题02 化学实验综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
更新时间:2024-01-21 08:26:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某小组同学用如图所示装置来完成浓硫酸和木炭反应的实验以及检验生成的CO2和SO2气体。
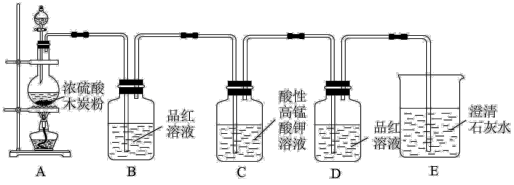
(1)装置A中反生反应的化学方程式为______________ ;
(2)装置B中观察到的现象是_________ ,说明这种物质具有____________ (填“酸性”或“漂白性”);
(3)装置C中酸性KMnO4溶液用于除去SO2,是利用了SO2具有____________ 填“氧化性”或“还原性”),其目的是___________ (填“甲”或“乙”);
甲:防止SO2干扰CO2的检验 乙:可吸收CO2气体
(4)装置E中观察到的现象是__________ ,反应的离子方程式为 ______________ 。

(1)装置A中反生反应的化学方程式为
(2)装置B中观察到的现象是
(3)装置C中酸性KMnO4溶液用于除去SO2,是利用了SO2具有
甲:防止SO2干扰CO2的检验 乙:可吸收CO2气体
(4)装置E中观察到的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】碲(52Te)被誉为“国防与尖端技术的维生素”。工业上常用铜阳极泥(主要成分是Cu2Te、含Ag、Au等杂质)为原料提取碲并回收金属,其工艺流程如下:

已知:TeO2微溶于水,易与较浓的强酸、强碱反应。回答下列问题:
(1)已知Te为VIA族元素,TeO2被浓NaOH溶液溶解,所生成盐的化学式为____________ 。
(2)“酸浸2”时温度过高会使Te的浸出率降低,原因是________________________ 。
(3)“酸浸1”过程中,控制溶液的酸度使Cu2Te转化为TeO2,反应的化学方程式为____________ ;
“还原”过程中,发生反应的离子方程式为_____________________________ 。
(4)工业上也可用电解法从铜阳极泥中提取碲,方法是:将铜阳极泥在空气中焙烧使碲转化为TeO2,再用NaOH溶液碱浸,以石墨为电极电解所得溶液获得Te。电解过程中阴极上发生反应的电极方程式为____________________ 。在阳极区溶液中检验出有TeO42-存在,生成TeO42-的原因是_____________________ 。
(5)常温下,向l mol·L-1 Na2TeO3溶液中滴加盐酸,当溶液pH=5时,c(TeO32-):c(H2TeO3)=__________ 。(已知:H2TeO3的Ka1=1.0×10-3 Ka2=2.0×10-8)

已知:TeO2微溶于水,易与较浓的强酸、强碱反应。回答下列问题:
(1)已知Te为VIA族元素,TeO2被浓NaOH溶液溶解,所生成盐的化学式为
(2)“酸浸2”时温度过高会使Te的浸出率降低,原因是
(3)“酸浸1”过程中,控制溶液的酸度使Cu2Te转化为TeO2,反应的化学方程式为
“还原”过程中,发生反应的离子方程式为
(4)工业上也可用电解法从铜阳极泥中提取碲,方法是:将铜阳极泥在空气中焙烧使碲转化为TeO2,再用NaOH溶液碱浸,以石墨为电极电解所得溶液获得Te。电解过程中阴极上发生反应的电极方程式为
(5)常温下,向l mol·L-1 Na2TeO3溶液中滴加盐酸,当溶液pH=5时,c(TeO32-):c(H2TeO3)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了如图所示实验装置(锌与浓硫酸共热时产生的气体为X,且该装置略去)。
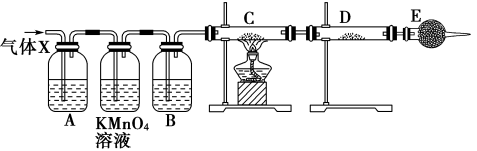
(1)上述反应中生成二氧化硫的化学方程式为_____ 。
(2)乙同学认为还可能产生氢气的理由是____ 。
(3)丙同学在安装好装置后,必须首先进行的一步操作____ 。
(4)A中加入的试剂可能是____ ,作用是____ 。
(5)如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?____ (填“能”或“不能”),原因是____ 。

(1)上述反应中生成二氧化硫的化学方程式为
(2)乙同学认为还可能产生氢气的理由是
(3)丙同学在安装好装置后,必须首先进行的一步操作
(4)A中加入的试剂可能是
(5)如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】CO 变换反应为:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ·mol⁻1。
(1)一定温度下,反应后测得各组分的平衡压强(即该组分的物质的量分数×总压): p(CO)=0.25 MPa、p(H2O)=0.25 MPa、p(CO2)=0.75 MPa 和 p(H2)=0.75 MPa,则该反应的平衡常数 Kp=___________ 。维持相同的温度和总压,提高水蒸气的投料比例,使 CO 的平衡转化率提高到 90%,则原料气中水蒸气和 CO 的物质的量之比为___________ 。
(2)生产过程中,为了提高变换反应的速率,下列措施中合适的是___________。
(3)以固体催化剂 M 催化 CO 变换反应,能量-反应过程关系如下图所示。步骤___________ 为决速步。(选填“I”或“II”)

用化学方程式表示该催化反应历程:
步骤 I: M(s)+H2O(g)=MO(s)+H2(g), 步骤 II:___________ 。
(1)一定温度下,反应后测得各组分的平衡压强(即该组分的物质的量分数×总压): p(CO)=0.25 MPa、p(H2O)=0.25 MPa、p(CO2)=0.75 MPa 和 p(H2)=0.75 MPa,则该反应的平衡常数 Kp=
(2)生产过程中,为了提高变换反应的速率,下列措施中合适的是___________。
| A.反应温度越高越好 | B.适当提高反应物压强 |
| C.选择合适的催化剂 | D.通入一定量的 N2 |

用化学方程式表示该催化反应历程:
步骤 I: M(s)+H2O(g)=MO(s)+H2(g), 步骤 II:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】合成氨技术的创立开辟了人工固氮的重要途径。回答下列问题:
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3.在1.01×105 Pa、250 ℃时,将1 mol N2和1 mol H2加入a L刚性容器中充分反应,测得NH3体积分数为0.04;其他条件不变,温度升高至450 ℃,测得NH3体积分数为0.025,则可判断合成氨反应为_______ (填“吸热”或“放热”)反应。
(2)在1.01×105 Pa、250 ℃时,将2 mol N2和2 mol H2加入a L密闭容器中充分反应,H2平衡转化率可能为_______(填标号)。
(3)我国科学家结合实验与计算机模拟结果,研究了在铁掺杂W18049纳米反应器催化剂表面上实现常温低电位合成氨,获得较高的氨产量和法拉第效率。反应历程如图所示,其中吸附在催化剂表面的物种用*标注。
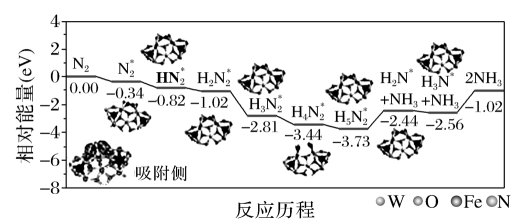
需要吸收能量最大的能垒(活化能)E=_______ eV,该步骤的化学方程式为_______
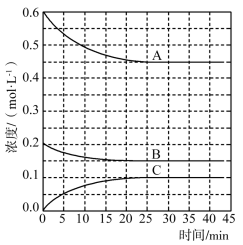
(4)T ℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g) 2NH3(g)反应过程中各物质浓度的变化曲线如图所示:表示N2浓度变化的曲线是
2NH3(g)反应过程中各物质浓度的变化曲线如图所示:表示N2浓度变化的曲线是_______ (填“A”、“B”或“C”)。与(1)中的实验条件(1.01×105 Pa、450 ℃)相比,改变的条件可能是_______ 。
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3.在1.01×105 Pa、250 ℃时,将1 mol N2和1 mol H2加入a L刚性容器中充分反应,测得NH3体积分数为0.04;其他条件不变,温度升高至450 ℃,测得NH3体积分数为0.025,则可判断合成氨反应为
(2)在1.01×105 Pa、250 ℃时,将2 mol N2和2 mol H2加入a L密闭容器中充分反应,H2平衡转化率可能为_______(填标号)。
| A.=4% | B.<4% | C.4%~7% | D.>11.5% |

需要吸收能量最大的能垒(活化能)E=
(4)T ℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g)
 2NH3(g)反应过程中各物质浓度的变化曲线如图所示:表示N2浓度变化的曲线是
2NH3(g)反应过程中各物质浓度的变化曲线如图所示:表示N2浓度变化的曲线是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】工业上,可以用 处理烟气中
处理烟气中 、
、 ,总反应式为
,总反应式为 .已知:有关反应的能量变化曲线如图所示。
.已知:有关反应的能量变化曲线如图所示。 和
和 反应的热化学方程式:
反应的热化学方程式:________________ 。上述总反应中
________  。
。
(2)其他条件不变,增大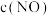 ,对总反应速率几乎没有影响,其原因可能是
,对总反应速率几乎没有影响,其原因可能是________________ 。
(3)一定条件下, 速率方程为
速率方程为 (k为速率常数,只与温度有关)。阿仑尼乌斯经验公式:
(k为速率常数,只与温度有关)。阿仑尼乌斯经验公式: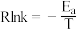 (R为常数,
(R为常数, 为活化能,不随温度改变;T为温度)。
为活化能,不随温度改变;T为温度)。 和
和 反应在不同催化剂Cat1、Cat2作用下,
反应在不同催化剂Cat1、Cat2作用下,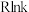 与
与 的关系如图所示。
的关系如图所示。________ (填“Cat1”或“Cat2”),判断依据是________________ 。
(4)在恒容密闭容器中保持总物质的量不变,充入NO和 。NO平衡转化率与温度(T)、投料比
。NO平衡转化率与温度(T)、投料比 关系如图所示。
关系如图所示。
________  (填“
(填“ ”“
”“ ”或“
”或“ ”);平衡常数
”);平衡常数 、
、 和
和 由大到小排序为
由大到小排序为________________ 。
②已知: ,
, 温度下该反应的平衡常数
温度下该反应的平衡常数
________________ 。( 为用分压表示的平衡常数,分压
为用分压表示的平衡常数,分压 总压
总压 物质的量分数)
物质的量分数)
(5)在恒容密闭容器中充入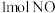 和
和 ,发生反应,测得部分物质的平衡浓度变化如图所示。M点对应的反应体系中
,发生反应,测得部分物质的平衡浓度变化如图所示。M点对应的反应体系中 体积分数为
体积分数为________________ 。
 处理烟气中
处理烟气中 、
、 ,总反应式为
,总反应式为 .已知:有关反应的能量变化曲线如图所示。
.已知:有关反应的能量变化曲线如图所示。
 和
和 反应的热化学方程式:
反应的热化学方程式:
 。
。(2)其他条件不变,增大
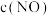 ,对总反应速率几乎没有影响,其原因可能是
,对总反应速率几乎没有影响,其原因可能是(3)一定条件下,
 速率方程为
速率方程为 (k为速率常数,只与温度有关)。阿仑尼乌斯经验公式:
(k为速率常数,只与温度有关)。阿仑尼乌斯经验公式: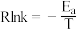 (R为常数,
(R为常数, 为活化能,不随温度改变;T为温度)。
为活化能,不随温度改变;T为温度)。 和
和 反应在不同催化剂Cat1、Cat2作用下,
反应在不同催化剂Cat1、Cat2作用下,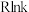 与
与 的关系如图所示。
的关系如图所示。
(4)在恒容密闭容器中保持总物质的量不变,充入NO和
 。NO平衡转化率与温度(T)、投料比
。NO平衡转化率与温度(T)、投料比 关系如图所示。
关系如图所示。

 (填“
(填“ ”“
”“ ”或“
”或“ ”);平衡常数
”);平衡常数 、
、 和
和 由大到小排序为
由大到小排序为②已知:
 ,
, 温度下该反应的平衡常数
温度下该反应的平衡常数
 为用分压表示的平衡常数,分压
为用分压表示的平衡常数,分压 总压
总压 物质的量分数)
物质的量分数)(5)在恒容密闭容器中充入
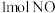 和
和 ,发生反应,测得部分物质的平衡浓度变化如图所示。M点对应的反应体系中
,发生反应,测得部分物质的平衡浓度变化如图所示。M点对应的反应体系中 体积分数为
体积分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
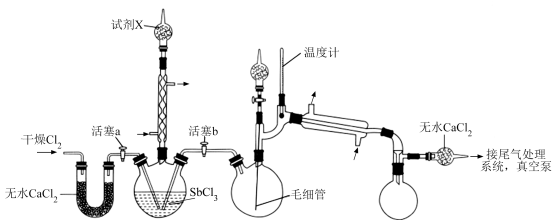
【推荐1】超酸是一类比纯硫酸更强的酸。某兴趣小组的同学对超酸 的制备及性质进行了探究。制备
的制备及性质进行了探究。制备 的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸),夹持、加热及搅拌装置略。
的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸),夹持、加热及搅拌装置略。
已知:①制备 的反应为
的反应为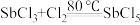 ,
,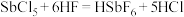 。
。
②有关物质的性质如表。
回答下列问题:
(1) 和浓盐酸制取
和浓盐酸制取 的离子方程式为
的离子方程式为_______ 。
(2)实验装置中,两个冷凝管_______ (填“能”或“不能”)交换使用。
(3)试剂X的成分是_______ (填化学名称);若无盛试剂X的装置, 可能发生水解生成
可能发生水解生成 ,其水解反应的化学方程式为
,其水解反应的化学方程式为_______ 。
(4)用真空泵抽气将 转移至双口烧瓶前,必须关闭的活塞是
转移至双口烧瓶前,必须关闭的活塞是_______ (填“a”或“b”),再减压蒸馏而不是常压蒸馏的主要原因是_______ 。
(5)由 制备
制备 时,应选用_______材质的仪器。(填标号)
时,应选用_______材质的仪器。(填标号)
(6)为更好地理解超酸的强酸性,该兴趣小组的同学查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸反应: ,以此类推,
,以此类推, 与
与 反应的化学方程式为
反应的化学方程式为_______ 。
 的制备及性质进行了探究。制备
的制备及性质进行了探究。制备 的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸),夹持、加热及搅拌装置略。
的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸),夹持、加热及搅拌装置略。
已知:①制备
 的反应为
的反应为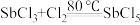 ,
,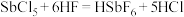 。
。②有关物质的性质如表。
| 物质 | 熔点 | 沸点 | 性质 |
 | 73.4℃ | 223.5℃ | 极易水解 |
 | 2.8℃ | 140℃分解,79℃/2.9kPa | 极易水解 |
(1)
 和浓盐酸制取
和浓盐酸制取 的离子方程式为
的离子方程式为(2)实验装置中,两个冷凝管
(3)试剂X的成分是
 可能发生水解生成
可能发生水解生成 ,其水解反应的化学方程式为
,其水解反应的化学方程式为(4)用真空泵抽气将
 转移至双口烧瓶前,必须关闭的活塞是
转移至双口烧瓶前,必须关闭的活塞是(5)由
 制备
制备 时,应选用_______材质的仪器。(填标号)
时,应选用_______材质的仪器。(填标号)| A.玻璃 | B.陶瓷 | C.铁或铝 | D.聚四氟乙烯 |
 ,以此类推,
,以此类推, 与
与 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.影响化学平衡的因素
 溶液中存在平衡:
溶液中存在平衡: (蓝色)
(蓝色)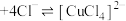 (黄色)
(黄色)
(1)取两支试管,分别加入2 mL 0.5 mol/L 溶液,溶液呈绿色,其原因为
溶液,溶液呈绿色,其原因为____________ 。
(2)将其中一支试管加热,溶液变为黄绿色,则该反应的
______ 0(填“>”或“<”),在另一支试管中加入5滴 溶液,静置,上层清液呈
溶液,静置,上层清液呈______ 色。
Ⅱ.电离平衡常数
(3) 是二元弱酸,其电离平衡常数
是二元弱酸,其电离平衡常数 的表达式为
的表达式为______ 。
(4)向盛有2 mL 1 mol/L醋酸的试管中滴加1 mol/L 溶液,观察到试管中有气泡产生,由此推断的
溶液,观察到试管中有气泡产生,由此推断的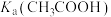
______ 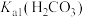 (填“>”或“<”),发生反应的离子方程式为
(填“>”或“<”),发生反应的离子方程式为____________ 。
Ⅲ.盐类水解的应用
(5)向一支试管中加入少量 晶体,然后加入5 mL蒸馏水、振荡,观察到
晶体,然后加入5 mL蒸馏水、振荡,观察到 慢慢溶解,但有少量浑浊,此溶液的pH
慢慢溶解,但有少量浑浊,此溶液的pH______ 7(填“>”“<”或“=”),配制 溶液的正确方法是
溶液的正确方法是____________ 。
(6)向一个烧杯中加入40 mL蒸馏水,加热至水沸腾,然后向沸水中逐滴加入5~6滴饱和 溶液,继续煮沸制得
溶液,继续煮沸制得 胶体。该反应的化学方程式为
胶体。该反应的化学方程式为____________ , 胶体呈
胶体呈______ 色。
Ⅳ.亚铁离子的检验
(7) 与
与______ 色的 溶液反应有特征蓝色沉淀产生,这是检验溶液中
溶液反应有特征蓝色沉淀产生,这是检验溶液中 的常用方法。写出该反应的离子方程式:
的常用方法。写出该反应的离子方程式:____________ 。
Ⅰ.影响化学平衡的因素
 溶液中存在平衡:
溶液中存在平衡: (蓝色)
(蓝色)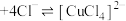 (黄色)
(黄色)
(1)取两支试管,分别加入2 mL 0.5 mol/L
 溶液,溶液呈绿色,其原因为
溶液,溶液呈绿色,其原因为(2)将其中一支试管加热,溶液变为黄绿色,则该反应的

 溶液,静置,上层清液呈
溶液,静置,上层清液呈Ⅱ.电离平衡常数
(3)
 是二元弱酸,其电离平衡常数
是二元弱酸,其电离平衡常数 的表达式为
的表达式为(4)向盛有2 mL 1 mol/L醋酸的试管中滴加1 mol/L
 溶液,观察到试管中有气泡产生,由此推断的
溶液,观察到试管中有气泡产生,由此推断的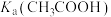
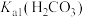 (填“>”或“<”),发生反应的离子方程式为
(填“>”或“<”),发生反应的离子方程式为Ⅲ.盐类水解的应用
(5)向一支试管中加入少量
 晶体,然后加入5 mL蒸馏水、振荡,观察到
晶体,然后加入5 mL蒸馏水、振荡,观察到 慢慢溶解,但有少量浑浊,此溶液的pH
慢慢溶解,但有少量浑浊,此溶液的pH 溶液的正确方法是
溶液的正确方法是(6)向一个烧杯中加入40 mL蒸馏水,加热至水沸腾,然后向沸水中逐滴加入5~6滴饱和
 溶液,继续煮沸制得
溶液,继续煮沸制得 胶体。该反应的化学方程式为
胶体。该反应的化学方程式为 胶体呈
胶体呈Ⅳ.亚铁离子的检验
(7)
 与
与 溶液反应有特征蓝色沉淀产生,这是检验溶液中
溶液反应有特征蓝色沉淀产生,这是检验溶液中 的常用方法。写出该反应的离子方程式:
的常用方法。写出该反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。

已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。
回答下列问题:
(1)在下列提供的试剂中,试剂B可以选用_________(填编号)。
(2)操作②加热浓缩时,同时通入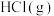 的目的是
的目的是_________ 。
(3)反应D→E的化学方程式为_________ 。
(4)由D转化成E的过程中可能产生少量亚铁盐,写出一种可能的还原剂_________ ,该副反应的反应的离子方程式为_________ 。
(5)按照你对还原剂的判断,设计实验验证是该还原剂将 还原
还原_________ 。
 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。
已知:氯化亚砜(
 )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。回答下列问题:
(1)在下列提供的试剂中,试剂B可以选用_________(填编号)。
| A.NaClO溶液 | B.氯水 | C.溴水 | D. 溶液 溶液 |
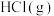 的目的是
的目的是(3)反应D→E的化学方程式为
(4)由D转化成E的过程中可能产生少量亚铁盐,写出一种可能的还原剂
(5)按照你对还原剂的判断,设计实验验证是该还原剂将
 还原
还原
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学小组欲测定酸性条件下KClO3溶液与NaHSO3溶液反应的化学反应速率,所用的试剂为10mL 0.1mol/L KClO3溶液和10mL 0.3mol/L NaHSO3溶液,所得溶液中c(Cl-)随时间变化的曲线和Cl-的速率时间关系如图所示:
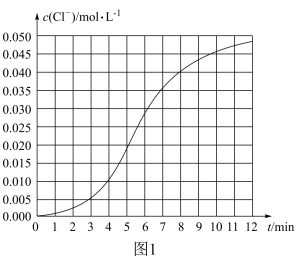

(1)该反应的化学方程式是:________________________ 。
(2)根据实验数据可知,该反应在 0~4min 的平均反应速率v(Cl-)=___________ 。
(3)下列说法中正确的是________________
A.纵坐标为v(ClO3 -)的v-t曲线与图中曲线不重合
B.图中阴影部分的面积表示t1—t2时间内n(Cl-)的增大
C.后期反应速率下降的主要原因是反应物浓度减少
(4)0~t1段,该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
已知:SO 对该反应速率无影响;
对该反应速率无影响;
可供选择的试剂有:
A.NaCl固体 B.Na2SO4固体 C.0.2mol/L HCl D.0.1mol/L H2SO4 E.0.2mol/L HNO3
①完成表格Ⅰ:_______________ ,Ⅱ:___________________
②方案Ⅱ烧杯①中加入1mL水的作用是________________________ 。
③除方案Ⅰ、Ⅱ外,请再提出一个可能使化学反应速率增大的假设_____________ 。


(1)该反应的化学方程式是:
(2)根据实验数据可知,该反应在 0~4min 的平均反应速率v(Cl-)=
(3)下列说法中正确的是
A.纵坐标为v(ClO3 -)的v-t曲线与图中曲线不重合
B.图中阴影部分的面积表示t1—t2时间内n(Cl-)的增大
C.后期反应速率下降的主要原因是反应物浓度减少
(4)0~t1段,该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
已知:SO
 对该反应速率无影响;
对该反应速率无影响;可供选择的试剂有:
A.NaCl固体 B.Na2SO4固体 C.0.2mol/L HCl D.0.1mol/L H2SO4 E.0.2mol/L HNO3
| 方案 | 假设 | 具体实验操作 | 数据处理 |
| Ⅰ | 反应产物Cl- 对反应有催化作用 | 取 10mL 0.1mol/L KClO3溶液于烧杯中,先加入___ (填代号),再加入10mL 0.3mol/L NaHSO3溶液。 | 绘制溶液中c(Cl-) 随时间变化的曲线并与图 1 对比 |
| Ⅱ | 反应中溶液酸性增强,加快了化学反应速率 | 分别向2个烧杯中加入10mL 0.1mol/L KClO3溶液。烧杯①:加入1mL水,烧杯②:加入1mL_____(填代号)。再分别向2个烧杯中加入10mL 0.3mol/L NaHSO3溶液。 |
②方案Ⅱ烧杯①中加入1mL水的作用是
③除方案Ⅰ、Ⅱ外,请再提出一个可能使化学反应速率增大的假设
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学在实验室研究Na2CO3和NaHCO3的性质及相互转化。
(1)分别向浓度均为0.1 mol/L Na2CO3及NaHCO3溶液中滴加几滴酚酞试剂:
①Na2CO3溶液由无色变为红色,其原因是_____________________________________________ 。
②NaHCO3溶液也由无色变为红色,其原因是_______________________________________________ 。
③比较两份溶液的颜色,红色较浅的是________ (填化学式)。
(2)研究NaHCO3与CaCl2的反应。
①实验1中没有出现白色浑浊的原因是________________________________________________ 。
②实验2中形成的分散系属于________ 。
③用离子方程式表示实验2中发生的反应_______________________________________________ 。
(3)在不引入其他杂质的前提下,实现Na2CO3与NaHCO3之间的转化,请在下图中标出所用的试剂、用量或物质的浓度(反应前后溶液体积的变化可忽略)________ 、________ 、________ 、________ 。
(1)分别向浓度均为0.1 mol/L Na2CO3及NaHCO3溶液中滴加几滴酚酞试剂:
①Na2CO3溶液由无色变为红色,其原因是
②NaHCO3溶液也由无色变为红色,其原因是
③比较两份溶液的颜色,红色较浅的是
(2)研究NaHCO3与CaCl2的反应。
| 实验序号 | 实验操作 | 实验现象 |
| 实验1 | 向2 mL 0.001 mol/L NaHCO3溶液中加入1 mL 0.1 mol/L CaCl2溶液 | 无明显变化。用激光笔照射,没有出现光亮的通路。 |
| 实验2 | 向2 mL 0.1 mol/L NaHCO3溶液中加入1 mL 0.1 mol/L CaCl2溶液 | 略显白色均匀的浑浊,用激光笔照射,出现光亮的通路。 |
②实验2中形成的分散系属于
③用离子方程式表示实验2中发生的反应
(3)在不引入其他杂质的前提下,实现Na2CO3与NaHCO3之间的转化,请在下图中标出所用的试剂、用量或物质的浓度(反应前后溶液体积的变化可忽略)

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分,将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1:该气体为CO2;
猜想2:该气体为SO2;
猜想3:_________________________________________ 。
为了验证猜想,该小组设计实验加以探究:
[实验探究]该小组同学按如图所示装置,将气体从a端通入,则

(1)B中应该装下列________ 试剂(填编号)。
A.NaCl溶液 B.酸性KMnO4溶液 C.盐酸 D.澄清石灰水
(2)A中品红溶液的作用是____________________________________ 。
(3)D中澄清石灰水的作用是________________________________________ 。
通过该实验,该小组同学观察到以下三个实验现象:①A中品红溶液褪色;②C中品红溶液不褪色;③D中澄清石灰水变浑浊,由上述现象该小组同学确认该气体的成分为________________ 。
[提出猜想]
猜想1:该气体为CO2;
猜想2:该气体为SO2;
猜想3:
为了验证猜想,该小组设计实验加以探究:
[实验探究]该小组同学按如图所示装置,将气体从a端通入,则

(1)B中应该装下列
A.NaCl溶液 B.酸性KMnO4溶液 C.盐酸 D.澄清石灰水
(2)A中品红溶液的作用是
(3)D中澄清石灰水的作用是
通过该实验,该小组同学观察到以下三个实验现象:①A中品红溶液褪色;②C中品红溶液不褪色;③D中澄清石灰水变浑浊,由上述现象该小组同学确认该气体的成分为
您最近一年使用:0次