下列实验操作和实验结论或目的均正确的是
选项 | 实验操作 | 实验结论或目的 |
A | 向含有酚酞的 | 证明 |
B | 等体积 | 证明HX酸性比HY强 |
C | 将氯水滴在湿润的pH试纸上,与标准比色卡对照 | 测定氯水的pH |
D | D.向 | 证明在相同温度下: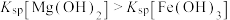 |
| A.A | B.B | C.C | D.D |
更新时间:2024-01-24 09:54:50
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】利用平衡移动原理,分析一定温度下 在不同pH的Na2CO3体系中的可能产物。
在不同pH的Na2CO3体系中的可能产物。
已知:①图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系。
②图2中曲线I的离子浓度关系符合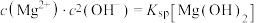 ;曲线II的离子浓度关系符合
;曲线II的离子浓度关系符合 。
。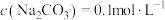 ,不同pH下
,不同pH下 由图1得到。
由图1得到。
下列说法不正确的是
 在不同pH的Na2CO3体系中的可能产物。
在不同pH的Na2CO3体系中的可能产物。已知:①图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系。
②图2中曲线I的离子浓度关系符合
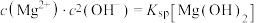 ;曲线II的离子浓度关系符合
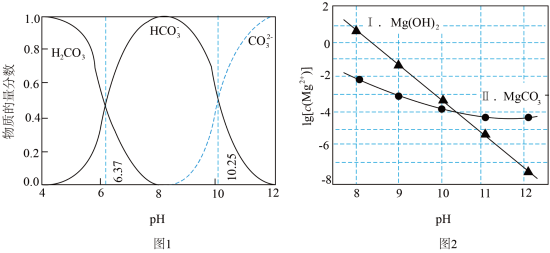
;曲线II的离子浓度关系符合 。
。
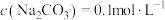 ,不同pH下
,不同pH下 由图1得到。
由图1得到。下列说法不正确的是
A.由图1,NaHCO3的水解平衡常数的数量级是 |
B.由图2,初始状态pH=12、 时,主要产生氢氧化镁沉淀 时,主要产生氢氧化镁沉淀 |
C.由图2,初始状态pH=9、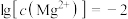 时,平衡后溶液中存在 时,平衡后溶液中存在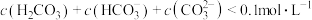 |
D.由图1和图2,初始状态pH=9、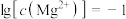 时,发生反应: 时,发生反应: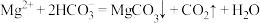 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列叙述与盐类的水解有关的是
①氯化铝溶液加热蒸干得到氢氧化铝
②保存硫酸亚铁溶液时需加入少量铁粉
③草木灰与铵态氮肥不能混合施用
④常用可溶性铝盐、铁盐作为净水剂
⑤用食醋除水垢[成分 和
和 ]
]
①氯化铝溶液加热蒸干得到氢氧化铝
②保存硫酸亚铁溶液时需加入少量铁粉
③草木灰与铵态氮肥不能混合施用
④常用可溶性铝盐、铁盐作为净水剂
⑤用食醋除水垢[成分
 和
和 ]
]| A.①③④ | B.②③④ | C.①③⑤ | D.③④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】向两份等体积、等浓度,pH不同的FeSO4溶液中逐滴加入NaClO溶液,实验测得溶液pH随加入NaClO(NaClO溶液pH>7)溶液体积变化曲线如下图,实验现象如下表。下列说法不正确 的是
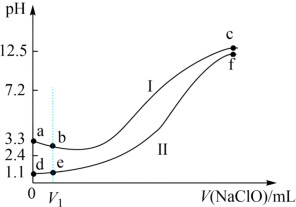
| 实验 | 实验现象 |
| Ⅰ | 滴入V1mLNaClO溶液产生大量红褐色沉淀 |
| Ⅱ | 滴入V1mLNaClO溶液,溶液变黄,未见沉淀,继续滴加出现红褐色沉淀 |

| A.a~b段主要反应的离子方程式为:2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+ |
| B.d~e段主要反应的离子方程式为:ClO-+H+=HClO |
| C.c、f点溶液呈碱性的原因是NaClO溶液过量 |
| D.向c点溶液中加入过量的浓盐酸,沉淀溶解并有刺激性气味的气体放出 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验操作对应的现象与结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 常温下将Ba(OH)2·8H2O晶体与NH4Cl晶体在小烧杯中混合 | 烧杯壁变凉 | 该反应正向是熵增的反应 |
| B | 常温下,用pH计分别测定1mol·L-1的CH3COONH4溶液和0.1mol·L-1的CH3COONH4溶液的pH | 测得pH都等于7 | 同温下,不同浓度的CH3COONH4溶液中水的电离程度相同 |
| C | 用Pt电极电解等浓度的足量 Fe(NO3)3、Cu(NO3)2混合溶液 | 阴极有红色固体物质析出 | 金属活动性:Fe>Cu |
| D | 常温下向物质的量浓度均为0.1mol·L-1的NaCl和NaI混合溶液中逐滴滴入AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验操作和现象及所得到的结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向蛋白质溶液中滴加过量的氯化铵,有固体析出 | 蛋白质变性 |
| B | 向NaI和NaCl混合液中加入大量AgNO3溶液,出现了黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向蔗糖溶液中加入稀H2SO4,加热几分钟,冷却后加入新制Cu(OH)2,加热后没有红色沉淀生成 | 蔗糖还未水解 |
| D | 用pH测得:0.1mol/LCH3COOH溶液的pH约为3 | 发生电离CH3COOH分子约为1% |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】完成下列实验目的所采取的实验方法和对应原理都正确的是
| 选项 | 目的 | 实验方法 | 原理 |
| A | 除去蛋白质溶液中混有的(NH4)2SO4 | 将混合物倒入过滤器中过滤 | 胶体不能透过滤纸 |
| B | 提取溴水中 的溴单质 | 用乙醇萃取 | 溴在乙醇中的溶解度较大 |
| C | 检验FeSO4溶液是否在空气中氧化变质 | 向盛有FeSO4溶液的试管中滴入KSCN溶液,观察溶液是否变红色 | Fe3+和SCN-反应生成Fe(SCN)3,溶液显红色 |
| D | 证明:Ksp[ Fe(OH)3]< Ksp[ Mg(OH)2] | 向盛有2 mL浓度均为0.1 mol/L的FeCl3和MgCl2的混合溶液的试管中滴加1 mol/L NaOH溶液,观察到析出红褐色沉淀 | Ksp越小的物质越容易沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】用下列装置进行相应实验,能达到实验目的是
| A | B | C | D |
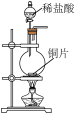 | 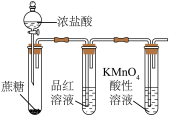 |  |  |
制取 | 验证浓 的脱水性、强氧化性 的脱水性、强氧化性 | 完成喷泉实验 |  的尾气吸收 的尾气吸收 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】现有如下所示4个装置图,以下说法中正确的是
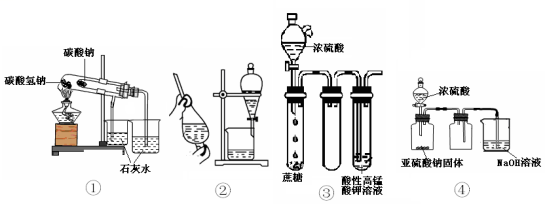

| A.①装置可用于比较NaHCO3和Na2CO3的稳定性 | B.用酒精萃取溴水中的溴可选择②装置 |
| C.如③装置进行实验可看到酸性KMnO4溶液褪色 | D.④装置可用于实验室制取并收集少量SO2 |
您最近一年使用:0次

 溶液中加入少量
溶液中加入少量 固体,溶液红色变浅
固体,溶液红色变浅 的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快
的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快 溶液中滴2滴
溶液中滴2滴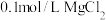 溶液,产生白色沉淀后再滴加2滴
溶液,产生白色沉淀后再滴加2滴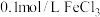 ,又生成红褐色沉淀
,又生成红褐色沉淀