 广泛用于冶金、化工等行业,主要用于冶炼钒铁。以钒矿石为原料制备
广泛用于冶金、化工等行业,主要用于冶炼钒铁。以钒矿石为原料制备 的工艺流程如下:
的工艺流程如下: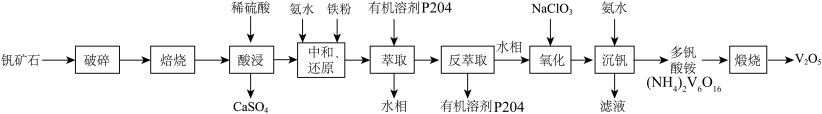
已知:ⅰ.“焙烧”后,固体中主要含有
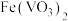 、
、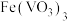 、
、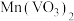 、
、 ;“酸浸”后钒以
;“酸浸”后钒以 形式存在,“中和、还原”后钒以
形式存在,“中和、还原”后钒以 形式存在。
形式存在。ⅱ.有机溶剂P204对四价钒
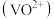 具有高选择性,且萃取
具有高选择性,且萃取 而不萃取
而不萃取 。
。ⅲ.多钒酸铵微溶于冷水,易溶于热水。
ⅳ.该工艺条件下,溶液中金属离子(浓度均为
 )开始沉淀和完全沉淀的pH如下表所示:
)开始沉淀和完全沉淀的pH如下表所示:| 金属离子 |  |  |  |  |
| 开始沉淀pH | 1.9 | 7.0 | 11.9 | 8.1 |
| 完全沉淀pH | 3.2 | 9.0 | 13.9 | 10.1 |
(1)“破碎”的目的是
(2)“中和、还原”时,
 参与反应的离子方程式为
参与反应的离子方程式为(3)钒的浸出率与焙烧温度、硫酸加入量的关系如图1、2所示,适宜的工艺条件为
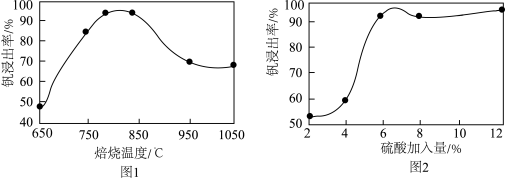
(4)“氧化”时,每消耗
 (本身被还原为
(本身被还原为 ),可得到
),可得到
(5)流程中可循环使用的物质有
(6)“萃取”分离后,所得“水相”中含有丰富的金属资源,经三道工序可回收
 溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂:
溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂: 溶液、
溶液、 、
、 溶液、
溶液、 溶液)
溶液)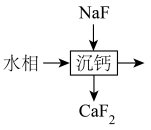
更新时间:2024-01-29 10:42:27
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】一种以NH4Cl酸性蚀铜废液[含NH4Cl,Cu(NH3)4Cl2、CuCl、CuSO4及盐酸等]为原料制备CuCl并回收Cu(OH)2的工艺流程如图:

已知:CuCl溶于浓盐酸,难溶于水,不溶于乙醇。
回答下列问题:
(1)“反应1”中,NaCl、Cu与CuSO4反应的离子方程式为__ ;生产中常将“过滤1”的滤渣返回到“反应1”中,其目的是__ 。
(2)“水解”步骤中,溶液中的CuCl43-在加入大量水稀释即可析出CuCl,原因是__ (结合离子方程式,从平衡角度分析)。
(3)湿的CuCl在空气中易被氧化为Cu2(OH)3Cl,该反应的化学方程式为__ 。
(4)“反应2”需加入的试剂X是__ ;“吹脱”出来的NH3可用于生产碳铵化肥,主要反应的化学方程式为__ 。
(5)测定产品中CuCl质量分数的步骤如下:称取ag产品,加入稍过量的FeCl3溶液,待溶解后用邻菲罗啉作指示剂,立刻用cmol·L-1的Ce(SO4)2标准溶液滴定到终点,消耗标准溶液VmL。则产品中CuCl的质量分数为__ (已知滴定反应为Ce4++Fe2+=Ce3++Fe3+,列出计算式)。

已知:CuCl溶于浓盐酸,难溶于水,不溶于乙醇。
回答下列问题:
(1)“反应1”中,NaCl、Cu与CuSO4反应的离子方程式为
(2)“水解”步骤中,溶液中的CuCl43-在加入大量水稀释即可析出CuCl,原因是
(3)湿的CuCl在空气中易被氧化为Cu2(OH)3Cl,该反应的化学方程式为
(4)“反应2”需加入的试剂X是
(5)测定产品中CuCl质量分数的步骤如下:称取ag产品,加入稍过量的FeCl3溶液,待溶解后用邻菲罗啉作指示剂,立刻用cmol·L-1的Ce(SO4)2标准溶液滴定到终点,消耗标准溶液VmL。则产品中CuCl的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】燃煤烟气中主要成分是空气,SO2和NO的含量小于1%。一种用CO(NH2)2(尿素)和H2O2在固体催化剂作用下脱硫、脱硝。其流程如下:

(1)CO(NH2)2可以水解生成(NH4)2CO3,CO(NH2)2、(NH4)2CO3与烟气中的NO不反应。脱硫后所得吸收液中含CO(NH2)2、(NH4)2SO3、(NH4)2SO4。其他条件一定,反应相同时间,测得SO2的脱除率与温度的关系如图1所示。30~70℃时,SO2的脱除率随温度升高先增大后减小的原因是___________ 。

(2)烟气中的NO与O2反应缓慢。雾化后的H2O2在催化剂中Fe元素作用下可以产生具有极强氧化活性的·OH(羟基自由基),·OH能将NO快速氧化为NO2、HNO3等物质。H2O2在一种固体催化剂表面转化的过程如图2所示:

①脱硝时,NO2与吸收液中(NH4)2SO3反应生成(NH4)2SO4,同时排放出的气体不会污染空气。写出脱硝时NO2与(NH4)2SO3反应的化学方程式:___________ 。
②化学式为LaFeO2.6的催化剂中,Fe3+和Fe2+的物质的量之比为___________ 。
(3)如不使用固体催化剂,用含Fe3+的溶液也能催化H2O2发生类似的转化生成·OH,且相同条件下速率更快。与使用含Fe3+的溶液相比,使用固体催化剂的优点是___________ 。

(1)CO(NH2)2可以水解生成(NH4)2CO3,CO(NH2)2、(NH4)2CO3与烟气中的NO不反应。脱硫后所得吸收液中含CO(NH2)2、(NH4)2SO3、(NH4)2SO4。其他条件一定,反应相同时间,测得SO2的脱除率与温度的关系如图1所示。30~70℃时,SO2的脱除率随温度升高先增大后减小的原因是

(2)烟气中的NO与O2反应缓慢。雾化后的H2O2在催化剂中Fe元素作用下可以产生具有极强氧化活性的·OH(羟基自由基),·OH能将NO快速氧化为NO2、HNO3等物质。H2O2在一种固体催化剂表面转化的过程如图2所示:

①脱硝时,NO2与吸收液中(NH4)2SO3反应生成(NH4)2SO4,同时排放出的气体不会污染空气。写出脱硝时NO2与(NH4)2SO3反应的化学方程式:
②化学式为LaFeO2.6的催化剂中,Fe3+和Fe2+的物质的量之比为
(3)如不使用固体催化剂,用含Fe3+的溶液也能催化H2O2发生类似的转化生成·OH,且相同条件下速率更快。与使用含Fe3+的溶液相比,使用固体催化剂的优点是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】Ⅰ. 、
、 、
、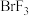 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈 、
、 两种价态,则这种化合物的化学式是
两种价态,则这种化合物的化学式是__________ 。
(2)溴化碘( )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为________ ;
(3)①已知某些离子的还原性强弱顺序为 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______ ;
②下列物质中,也可以使该溶液红色褪去的是_______ ;
A 新制氯水 B 碘水 C D 盐酸
D 盐酸
(4) 为剧毒物质,处理含有
为剧毒物质,处理含有 的废水常用的方法是:在碱性条件下用
的废水常用的方法是:在碱性条件下用 溶液将
溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为
和一种单质气体,该反应的离子方程式为_________ ;
(5)已知 的电离平衡常数
的电离平衡常数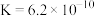 ,
, 的电离平衡常数
的电离平衡常数 ,
, ,则下列离子方程式能发生的是
,则下列离子方程式能发生的是____________ 。
A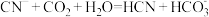 B
B 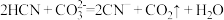
C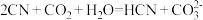 D
D 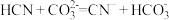
Ⅱ.如下图转化关系: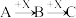
(6)若B为白色胶状不溶物,则A与C反应的离子方程式为_______ 。
(7)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为______ 。
 、
、 、
、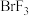 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈
 、
、 两种价态,则这种化合物的化学式是
两种价态,则这种化合物的化学式是(2)溴化碘(
 )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为(3)①已知某些离子的还原性强弱顺序为
 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象②下列物质中,也可以使该溶液红色褪去的是
A 新制氯水 B 碘水 C
 D 盐酸
D 盐酸(4)
 为剧毒物质,处理含有
为剧毒物质,处理含有 的废水常用的方法是:在碱性条件下用
的废水常用的方法是:在碱性条件下用 溶液将
溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为
和一种单质气体,该反应的离子方程式为(5)已知
 的电离平衡常数
的电离平衡常数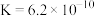 ,
, 的电离平衡常数
的电离平衡常数 ,
, ,则下列离子方程式能发生的是
,则下列离子方程式能发生的是A
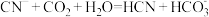 B
B 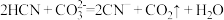
C
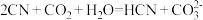 D
D 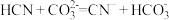
Ⅱ.如下图转化关系:
(6)若B为白色胶状不溶物,则A与C反应的离子方程式为
(7)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】氧化铬(Cr2O3)可用作着色剂、催化剂、印刷纸币的油墨等。以含铬废料(含FeCr2O4、MgO、SiO2、Al2O3等)为原料制备氧化铬的一种流程如图所示。

已知:烧渣的成分为Na2CrO4、NaAlO2、Na2SiO3、Fe2O3、MgO;Ksp[Fe(OH)3]=4×10-38、Ksp[Al(OH)3]=1×10-33、Ksp[Mg(OH)2]=2×10-11,溶液中离子浓度≤10-5mol·L-1时认为该离子沉淀完全。
回答下列问题:
(1)“研磨”的目的为___________ ;“焙烧”过程发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为___________ 。
(2)若滤液1中金属离子的浓度均为0.2mol·L-1,则“调pH”的最小值为___________ 。(保留两位有效数字)。
(3)“除镁”工序控制温度不能过高,且不能在陶瓷容器中进行的原因为___________ 。
(4)“转化”时加入适量H2SO4的作用为___________ 。
(5)部分物质的溶解度曲线如图所示。

①“系列操作”具体指___________ ,将所得滤液降温结晶、过滤、乙醚洗涤。
②降温结晶时控制的适宜温度为___________ (填选项字母)。
A.0~10℃ B.10~20℃ C.50~70℃ D.80℃以上
③用乙醚洗涤而不用乙醇洗涤的原因为___________ 。
(6)“煅烧”反应生成N2和水蒸气,该反应的化学方程式为___________ 。

已知:烧渣的成分为Na2CrO4、NaAlO2、Na2SiO3、Fe2O3、MgO;Ksp[Fe(OH)3]=4×10-38、Ksp[Al(OH)3]=1×10-33、Ksp[Mg(OH)2]=2×10-11,溶液中离子浓度≤10-5mol·L-1时认为该离子沉淀完全。
回答下列问题:
(1)“研磨”的目的为
(2)若滤液1中金属离子的浓度均为0.2mol·L-1,则“调pH”的最小值为
(3)“除镁”工序控制温度不能过高,且不能在陶瓷容器中进行的原因为
(4)“转化”时加入适量H2SO4的作用为
(5)部分物质的溶解度曲线如图所示。

①“系列操作”具体指
②降温结晶时控制的适宜温度为
A.0~10℃ B.10~20℃ C.50~70℃ D.80℃以上
③用乙醚洗涤而不用乙醇洗涤的原因为
(6)“煅烧”反应生成N2和水蒸气,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】铜氨溶液在纤维工业有广泛应用。实验室模拟用废弃辉铜矿渣(主要含Cu2S,还含有少量FeS、SiO2)为原料制备Cu(NH3) 的流程如图:
的流程如图:
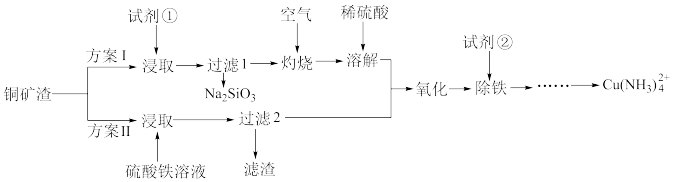
已知:常温下,Ksp[Cu(OH)2]=2×10-20,Cu2++4NH3 Cu(NH3)
Cu(NH3) K=1×1013
K=1×1013
回答下列问题:
(1)实验前将矿渣粉碎的目的是________ ,方案I中试剂①是________ 。
(2)方案II中,“过滤2”所得滤渣的主要成分除S外,还有________ (填化学式)。Cu2S和硫酸铁溶液反应的离子方程式是________ 。
(3)“除铁”前,“氧化”的目的是________ ,试剂②最好选用________ (填化学式)。如何证明铁元素被完全除尽?________ 。
(4)从环保角度看,两种方案更优的是________ 。
(5)常温下,向CuSO4溶液中加入浓氨水,生成Cu(OH)2沉淀,继续加入浓氨水,沉淀溶解生成Cu(NH3) 。沉淀开始溶解时溶液的pH为10,则
。沉淀开始溶解时溶液的pH为10,则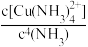 =
=________ 。
 的流程如图:
的流程如图:
已知:常温下,Ksp[Cu(OH)2]=2×10-20,Cu2++4NH3
 Cu(NH3)
Cu(NH3) K=1×1013
K=1×1013回答下列问题:
(1)实验前将矿渣粉碎的目的是
(2)方案II中,“过滤2”所得滤渣的主要成分除S外,还有
(3)“除铁”前,“氧化”的目的是
(4)从环保角度看,两种方案更优的是
(5)常温下,向CuSO4溶液中加入浓氨水,生成Cu(OH)2沉淀,继续加入浓氨水,沉淀溶解生成Cu(NH3)
 。沉淀开始溶解时溶液的pH为10,则
。沉淀开始溶解时溶液的pH为10,则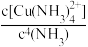 =
=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用作食品添加剂(抗结剂),我国卫生部规定实验中黄血盐的最大使用量为10mg/kg。一种制备黄血盐的工艺如图:

回答下列问题:
(1)步骤Ⅰ制备的Ca2Fe(CN)6易溶于水吗?__ (填“易溶”或“不易溶”)。
(2)步骤Ⅲ的化学方程式为__ 。
(3)步骤Ⅴ所用的试剂X是__ (填化学式)。
(4)工艺中用到剧毒的HCN溶液,含CN-的废水必须处理后才能排放。
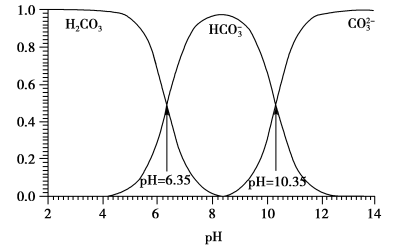
已知:HCN是一种具有苦杏仁味的无色剧毒液体,易挥发,25℃时Ka(HCN)=6.25×10-10;溶液中H2CO3、HCO3-、CO32-的存在与溶液pH的关系如图所示:
①HCN的电子式为__ 。
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5~8.5,用NaClO溶液完全氧化OCN-生成N2和两种盐。第一步控制强碱性的主要目的是__ ,第二步反应的离子方程式为__ 。
(5)已知蓝色染料普鲁士蓝的合成方法如图:

用硫酸亚铁碱性试纸可以检验食品中是否含有CN-,方案如图:

若试纸变蓝则证明食品中含有CN-,基于普鲁士蓝的合成原理,请用离子方程式解释检测时试纸变蓝的原因:__ 。

回答下列问题:
(1)步骤Ⅰ制备的Ca2Fe(CN)6易溶于水吗?
(2)步骤Ⅲ的化学方程式为
(3)步骤Ⅴ所用的试剂X是
(4)工艺中用到剧毒的HCN溶液,含CN-的废水必须处理后才能排放。
已知:HCN是一种具有苦杏仁味的无色剧毒液体,易挥发,25℃时Ka(HCN)=6.25×10-10;溶液中H2CO3、HCO3-、CO32-的存在与溶液pH的关系如图所示:

①HCN的电子式为
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5~8.5,用NaClO溶液完全氧化OCN-生成N2和两种盐。第一步控制强碱性的主要目的是
(5)已知蓝色染料普鲁士蓝的合成方法如图:

用硫酸亚铁碱性试纸可以检验食品中是否含有CN-,方案如图:

若试纸变蓝则证明食品中含有CN-,基于普鲁士蓝的合成原理,请用离子方程式解释检测时试纸变蓝的原因:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】 (乳酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1%
(乳酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1% 、19.5%
、19.5% 和3.4%
和3.4% )为原料制备钒酸铋,并回收
)为原料制备钒酸铋,并回收 制备食品抗氧化剂
制备食品抗氧化剂 的流程如下,回答下列问题:
的流程如下,回答下列问题: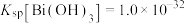 ,
, ;当金属离子浓度
;当金属离子浓度 时,认为该离子已沉淀完全。
时,认为该离子已沉淀完全。
(1)“焙烧”中采用高压空气的目的是_______ , 转化成
转化成 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(2)浸渣的主要成分是_______ (填化学式)。
(3)已知:“酸浸”得到的浸液中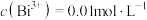 ,则“除铁”调节pH的范围为
,则“除铁”调节pH的范围为_______ 。
(4)“酸溶”需调节pH,避免生成BiOCl(难溶)。产生BiOCl反应的离子方程式为_______ 。
(5)向含少量水的 中通入
中通入 ,得到
,得到 产品。
产品。 易变质生成
易变质生成 ,设计简单实验证明产品是否变质:
,设计简单实验证明产品是否变质:_______ 。
已知: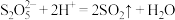 。
。
(6)某工厂用10吨该辉铋矿,最终得到9.234吨 ,则该过程中Bi的损耗率为
,则该过程中Bi的损耗率为_______ %。
 (乳酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1%
(乳酸铋)是一种黄色颜料。某小组以辉铋矿(含77.1% 、19.5%
、19.5% 和3.4%
和3.4% )为原料制备钒酸铋,并回收
)为原料制备钒酸铋,并回收 制备食品抗氧化剂
制备食品抗氧化剂 的流程如下,回答下列问题:
的流程如下,回答下列问题: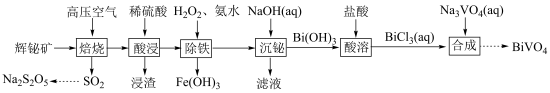
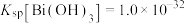 ,
, ;当金属离子浓度
;当金属离子浓度 时,认为该离子已沉淀完全。
时,认为该离子已沉淀完全。(1)“焙烧”中采用高压空气的目的是
 转化成
转化成 发生反应的化学方程式为
发生反应的化学方程式为(2)浸渣的主要成分是
(3)已知:“酸浸”得到的浸液中
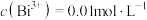 ,则“除铁”调节pH的范围为
,则“除铁”调节pH的范围为(4)“酸溶”需调节pH,避免生成BiOCl(难溶)。产生BiOCl反应的离子方程式为
(5)向含少量水的
 中通入
中通入 ,得到
,得到 产品。
产品。 易变质生成
易变质生成 ,设计简单实验证明产品是否变质:
,设计简单实验证明产品是否变质:已知:
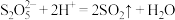 。
。(6)某工厂用10吨该辉铋矿,最终得到9.234吨
 ,则该过程中Bi的损耗率为
,则该过程中Bi的损耗率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】某小组探究 的制备。配制0.1
的制备。配制0.1 的
的 溶液和0.1
溶液和0.1 的
的 溶液备用。
溶液备用。
【查阅资料】
i.FeS、 均为黑色固体,难溶于水。
均为黑色固体,难溶于水。
ii. ,
, 为无色离子。
为无色离子。
iii.硫单质微溶于乙醇,难溶于水。
【设计并实施实验】
(1)实验一中,根据复分解反应规律推测,生产黑色沉淀a的离子方程式为_______ 。
(2)进一步检验浊液X的组成,过程如下。
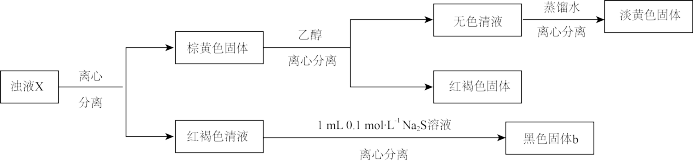
①通过对浊液X组成的检验,推测实验一的黑色沉淀a溶解过程中有氧化还原反应发生,实验证据是_______ 。
②经检测,黑色固体b的主要成分为FeS。甲同学认为,FeS是由红褐色清液中的 与加入的
与加入的 反应产生的。乙同学认为该解释不严谨,理由是
反应产生的。乙同学认为该解释不严谨,理由是_______ 。
(3)实验二制得了 ,但其中含少量
,但其中含少量 。
。
①生成 的离子方程式为
的离子方程式为_______ 。
②从化学反应速率角度推测实验二的棕黑色沉淀中不含S的原因:_______ 。
实验三
小组同学进行如下图所示的改进实验。经检验,黑色沉淀c为纯净的 。
。
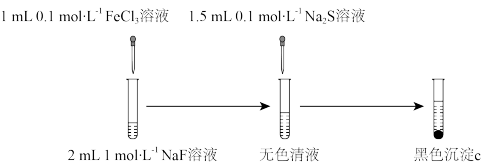
(4)实验三中,由无色清液生成 的离子方程式为
的离子方程式为_______ 。
【反思评价】
(5)对比三个实验,实验三能成功制备 的原因是
的原因是_______ 。
 的制备。配制0.1
的制备。配制0.1 的
的 溶液和0.1
溶液和0.1 的
的 溶液备用。
溶液备用。【查阅资料】
i.FeS、
 均为黑色固体,难溶于水。
均为黑色固体,难溶于水。ii.
 ,
, 为无色离子。
为无色离子。iii.硫单质微溶于乙醇,难溶于水。
【设计并实施实验】
| 编号 | 实验一 | 实验二 |
| 操作 | 1.0mL 0.1  溶液 溶液 | 0.5mL 0.1  溶液 溶液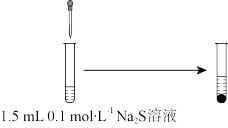 |
| 现象 | 迅速产生黑色沉淀a,振荡后黑色沉淀溶解,并产生臭鸡蛋气味的气体,最终得到棕黄色浊液X | 产生棕黑色沉淀 |
(2)进一步检验浊液X的组成,过程如下。

①通过对浊液X组成的检验,推测实验一的黑色沉淀a溶解过程中有氧化还原反应发生,实验证据是
②经检测,黑色固体b的主要成分为FeS。甲同学认为,FeS是由红褐色清液中的
 与加入的
与加入的 反应产生的。乙同学认为该解释不严谨,理由是
反应产生的。乙同学认为该解释不严谨,理由是(3)实验二制得了
 ,但其中含少量
,但其中含少量 。
。①生成
 的离子方程式为
的离子方程式为②从化学反应速率角度推测实验二的棕黑色沉淀中不含S的原因:
实验三
小组同学进行如下图所示的改进实验。经检验,黑色沉淀c为纯净的
 。
。
(4)实验三中,由无色清液生成
 的离子方程式为
的离子方程式为【反思评价】
(5)对比三个实验,实验三能成功制备
 的原因是
的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】难溶电解质的沉淀溶解平衡及其溶度积在生产、科研等领域有着许多的应用。
(1)25 ℃时,1 L水中约能溶解2.4×10-3 g硫酸钡。
①试计算25 ℃时硫酸钡的溶度积Ksp(BaSO4)=___________ 。
②当人体中钡离子浓度达到2×10-3 mol·L-1时会影响健康,那么硫酸钡可作为“钡餐”的原因是___________ 。
③在25 ℃时,1 L水中约能溶解0.018 g碳酸钡,且胃液是酸性的,碳酸钡不能代替硫酸钡作为“钡餐”的理由是什么?__________ (要运用题中所给数据,经计算回答上述②、③两小题)
(2)锅炉水垢会降低燃料利用率,还会形成安全隐患,因此要定期除去锅炉水垢。水垢中含有CaSO4[Ksp(CaSO4)=7.10×10-5],若用1 mol·L-1碳酸钠溶液处理,使之转化为疏松、易溶于酸的CaCO3[Ksp(CaCO3)=4.96×10-9],试利用Ksp计算反应的平衡常数说明这一转化的原理_______ 。
(1)25 ℃时,1 L水中约能溶解2.4×10-3 g硫酸钡。
①试计算25 ℃时硫酸钡的溶度积Ksp(BaSO4)=
②当人体中钡离子浓度达到2×10-3 mol·L-1时会影响健康,那么硫酸钡可作为“钡餐”的原因是
③在25 ℃时,1 L水中约能溶解0.018 g碳酸钡,且胃液是酸性的,碳酸钡不能代替硫酸钡作为“钡餐”的理由是什么?
(2)锅炉水垢会降低燃料利用率,还会形成安全隐患,因此要定期除去锅炉水垢。水垢中含有CaSO4[Ksp(CaSO4)=7.10×10-5],若用1 mol·L-1碳酸钠溶液处理,使之转化为疏松、易溶于酸的CaCO3[Ksp(CaCO3)=4.96×10-9],试利用Ksp计算反应的平衡常数说明这一转化的原理
您最近一年使用:0次
【推荐1】铍铜合金具有良好的综合性能,广泛应用于制造高级弹性元件。以下是从某旧铍铜元件(含BeO、CuS、少量FeS和SiO2)中回收铍和铜两种金属的工艺流程:
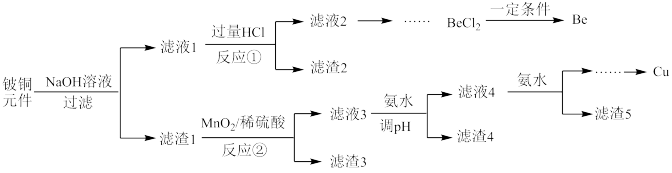
已知:Ⅰ.铍、铝元素的化学性质相似,氧化物具有两性
Ⅱ.常温下部分难溶物的溶度积常数如表:
(1)用NaOH溶液溶解铍铜元件时,能提高浸取率的措施有___ (写出两种)。
(2)滤渣1的成分有___ (填化学式)。
(3)①滤液2中含NaCl、BeCl2和少量HCl,为提纯BeCl2,下列实验步骤合理的顺序为___ (填字母)。
a.加入过量的氨水 b.加入适量的HCl c.洗涤 d.过滤
②从BeCl2溶液中得到BeCl2固体的操作是___ 。
(4)滤渣3中有淡黄色固体,写出反应②中CuS发生反应的离子方程式___ 。
(5)滤液3中含Fe3+,若使Fe3+完全沉淀,溶液pH至少为___ (已知离子物质的量浓度小于10-5mol·L-1时认为完全沉淀,lg2=0.3)。

已知:Ⅰ.铍、铝元素的化学性质相似,氧化物具有两性
Ⅱ.常温下部分难溶物的溶度积常数如表:
| 难溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
| 溶度积常数(Ksp) | 2.2×10-20 | 8.0×10-38 | 2.1×10-13 |
(2)滤渣1的成分有
(3)①滤液2中含NaCl、BeCl2和少量HCl,为提纯BeCl2,下列实验步骤合理的顺序为
a.加入过量的氨水 b.加入适量的HCl c.洗涤 d.过滤
②从BeCl2溶液中得到BeCl2固体的操作是
(4)滤渣3中有淡黄色固体,写出反应②中CuS发生反应的离子方程式
(5)滤液3中含Fe3+,若使Fe3+完全沉淀,溶液pH至少为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】粉煤灰是从煤燃烧后的烟气中收捕下来的细灰,主要成分有 、
、 、FeO和
、FeO和 等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米
等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米 等重要物质。
等重要物质。
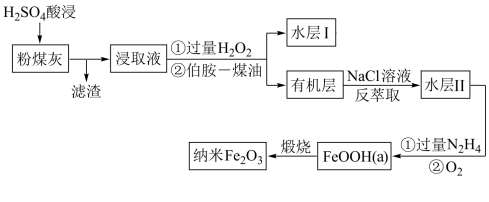
已知:
①伯胺 能与
能与 反应:
反应: ,生成易溶于煤油的产物。
,生成易溶于煤油的产物。
② 在水溶液中能与
在水溶液中能与 反应:
反应: 。
。
(1)“酸浸”过程中FeO发生反应的离子方程式为_______ ;滤渣的成分为_______ 。
(2)加入过量 的作用是
的作用是_______ 。
(3)伯胺-煤油可对浸取液进行分离,该操作的名称是_______ 。
(4)向水层Ⅱ中加入 可使
可使 转化为
转化为 并放出对环境无害的气体,理论上氧化剂与还原剂的物质的量之比为
并放出对环境无害的气体,理论上氧化剂与还原剂的物质的量之比为_______ ;向所得弱酸性溶液中再通入 即可生成FeOOH,其离子方程式为
即可生成FeOOH,其离子方程式为_______ 。
 、
、 、FeO和
、FeO和 等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米
等物质。综合利用粉煤灰不仅能够防止环境污染,还能制得纳米 等重要物质。
等重要物质。
已知:
①伯胺
 能与
能与 反应:
反应: ,生成易溶于煤油的产物。
,生成易溶于煤油的产物。②
 在水溶液中能与
在水溶液中能与 反应:
反应: 。
。(1)“酸浸”过程中FeO发生反应的离子方程式为
(2)加入过量
 的作用是
的作用是(3)伯胺-煤油可对浸取液进行分离,该操作的名称是
(4)向水层Ⅱ中加入
 可使
可使 转化为
转化为 并放出对环境无害的气体,理论上氧化剂与还原剂的物质的量之比为
并放出对环境无害的气体,理论上氧化剂与还原剂的物质的量之比为 即可生成FeOOH,其离子方程式为
即可生成FeOOH,其离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】草酸合铁酸钾晶体Kx[Fe(C2O4)y]·3H2O是一种光敏材料,下面是一种制备草酸合铁酸钾晶体的实验流程。

已知:(NH4)2SO4、FeSO4·7H2O、莫尔盐[(NH4)2SO4·FeSO4·6H2O]的溶解度如表:
(1)废铁屑在进行“溶解1”前,需用在5% Na2CO3溶液中加热数分钟,并洗涤干净。Na2CO3溶液的作用是________ 。
(2)“溶解1”应保证铁屑稍过量,其目的是___________ 。“溶解2”加“几滴H2SO4”的作用是________ 。
(3)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、________ 、过滤、用乙醇洗涤、干燥。用乙醇洗涤的目的是____________ 。
(4)“沉淀”时得到的FeC2O4·2H2O沉淀需用水洗涤干净。检验沉淀是否洗涤干净的方法是_______ 。
(5)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是__________ 。
(6)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤[备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250 mL待测液。
步骤2:用移液管移取25.00 mL待测液于锥形瓶中,加入稀H2SO4酸化,_________ ,C2O42-转化为CO2被除去。
步骤3:向步骤2所得溶液中______________ 。
步骤4:用c mol·L-1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液。

已知:(NH4)2SO4、FeSO4·7H2O、莫尔盐[(NH4)2SO4·FeSO4·6H2O]的溶解度如表:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| (NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
| FeSO4·7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | ― |
| (NH4)2SO4·FeSO4·6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(2)“溶解1”应保证铁屑稍过量,其目的是
(3)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、
(4)“沉淀”时得到的FeC2O4·2H2O沉淀需用水洗涤干净。检验沉淀是否洗涤干净的方法是
(5)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是
(6)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤[备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250 mL待测液。
步骤2:用移液管移取25.00 mL待测液于锥形瓶中,加入稀H2SO4酸化,
步骤3:向步骤2所得溶液中
步骤4:用c mol·L-1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液。
您最近一年使用:0次



