固体电解质以其在电池、传感器等装置中的广泛应用而备受关注,大致分为无机物类及高分子类。
(1)固体电解质中研究得最多的是 和O等的导体。
和O等的导体。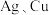 在元素周期表中位于同一族且
在元素周期表中位于同一族且 在
在 的下一周期,具有类似的价层电子排布式,
的下一周期,具有类似的价层电子排布式, 的价层电子排布式为
的价层电子排布式为___________ 。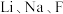 和O的电负性从小到大的顺序为
和O的电负性从小到大的顺序为___________ 。F的第二电离能___________ O的第二电离能(填“>”或“=”或“<”)。
(2) 中阴离子的空间构型为
中阴离子的空间构型为___________ 。
(3)1979年,法国Armand等报道了聚氧化乙烯( )碱金属盐络合物可用作锂离子电池固体聚合物电解质。聚氧化乙烯中O的
)碱金属盐络合物可用作锂离子电池固体聚合物电解质。聚氧化乙烯中O的___________ 杂化轨道与C的 杂化轨道成键;因氢键的形成,聚氧化乙烯是一种水溶性聚合物,若水分子之间形成的氢键可以表示为
杂化轨道成键;因氢键的形成,聚氧化乙烯是一种水溶性聚合物,若水分子之间形成的氢键可以表示为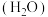
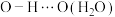 ,请写出使聚氧化乙烯具有水溶性的氢键的表示式
,请写出使聚氧化乙烯具有水溶性的氢键的表示式___________ 。
(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如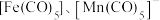 等都满足这个规则。钒配合物
等都满足这个规则。钒配合物 的熔点为
的熔点为 ,其晶体类型为:
,其晶体类型为:___________ ;已知该化合物满足18电子规则,其配体“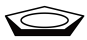 ”中的大
”中的大 键可表示为
键可表示为___________ 。(已知苯中的大 键表示为:
键表示为: )
)
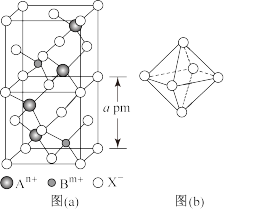
(5)图(a)为一种由阳离子 和阴离子
和阴离子 组成的无机固体电解质的晶胞结构。用A、B、X表示出这种电解质的化学式为
组成的无机固体电解质的晶胞结构。用A、B、X表示出这种电解质的化学式为___________ ,
___________ 。 堆积形成了正八面体和正四面体两种空隙,阳离子占据的空隙类型为
堆积形成了正八面体和正四面体两种空隙,阳离子占据的空隙类型为___________ ,占有率为___________ 。图(b)为 堆积形成的正八面体,其边长为
堆积形成的正八面体,其边长为___________  。(用含a的式子表示)
。(用含a的式子表示)
(1)固体电解质中研究得最多的是
 和O等的导体。
和O等的导体。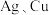 在元素周期表中位于同一族且
在元素周期表中位于同一族且 在
在 的下一周期,具有类似的价层电子排布式,
的下一周期,具有类似的价层电子排布式, 的价层电子排布式为
的价层电子排布式为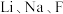 和O的电负性从小到大的顺序为
和O的电负性从小到大的顺序为(2)
 中阴离子的空间构型为
中阴离子的空间构型为(3)1979年,法国Armand等报道了聚氧化乙烯(
 )碱金属盐络合物可用作锂离子电池固体聚合物电解质。聚氧化乙烯中O的
)碱金属盐络合物可用作锂离子电池固体聚合物电解质。聚氧化乙烯中O的 杂化轨道成键;因氢键的形成,聚氧化乙烯是一种水溶性聚合物,若水分子之间形成的氢键可以表示为
杂化轨道成键;因氢键的形成,聚氧化乙烯是一种水溶性聚合物,若水分子之间形成的氢键可以表示为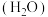
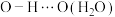 ,请写出使聚氧化乙烯具有水溶性的氢键的表示式
,请写出使聚氧化乙烯具有水溶性的氢键的表示式(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如
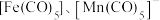 等都满足这个规则。钒配合物
等都满足这个规则。钒配合物 的熔点为
的熔点为 ,其晶体类型为:
,其晶体类型为: ”中的大
”中的大 键可表示为
键可表示为 键表示为:
键表示为: )
)(5)图(a)为一种由阳离子
 和阴离子
和阴离子 组成的无机固体电解质的晶胞结构。用A、B、X表示出这种电解质的化学式为
组成的无机固体电解质的晶胞结构。用A、B、X表示出这种电解质的化学式为
 堆积形成了正八面体和正四面体两种空隙,阳离子占据的空隙类型为
堆积形成了正八面体和正四面体两种空隙,阳离子占据的空隙类型为 堆积形成的正八面体,其边长为
堆积形成的正八面体,其边长为 。(用含a的式子表示)
。(用含a的式子表示)
更新时间:2024-01-23 20:10:08
|
相似题推荐
【推荐1】碳族化合物在研究和生产中有许多重要用途,请回答下列问题:
(1)已知 中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为
中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为_______ 。
(2)基态锗原子(Ge)价层电子的轨道表示式为_______ 。
(3)邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点低;请解释其原因_______ 。
(4)氮化硅( )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N_______ Si—N—Si(填“>”“<”“=”)。
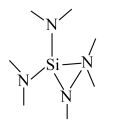
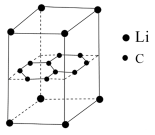
(5)某锂电池的负极材料是将锂原子嵌入到两层石墨烯层中间,其晶体结构如图。已知该晶体中最近的两个碳原子核间距离为a nm,石墨烯层间距离为b nm,则该晶体的密度为_______  (用
(用 表示阿伏加德罗常数,列式即可)。
表示阿伏加德罗常数,列式即可)。
(1)已知
 中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为
中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为(2)基态锗原子(Ge)价层电子的轨道表示式为
(3)邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点低;请解释其原因
(4)氮化硅(
 )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
(5)某锂电池的负极材料是将锂原子嵌入到两层石墨烯层中间,其晶体结构如图。已知该晶体中最近的两个碳原子核间距离为a nm,石墨烯层间距离为b nm,则该晶体的密度为
 (用
(用 表示阿伏加德罗常数,列式即可)。
表示阿伏加德罗常数,列式即可)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】磷、硫、氯、砷等是农药中的重要组成元素。回答下列问题:
(1)基态砷原子的核外价电子排布式为___________ 。
(2)生产农药的原料PSCl3中P、S、Cl的第一电离能由大到小的顺序为_______ ,电负性由大到小的顺序为_______
(3)COS(羰基硫)可用作粮食的熏蒸剂,其中碳原子的杂化轨道类型为_______ ,所含共价键的类型为_____ ,写出一种与COS 键合方式相同且空间构型也相同的微粒:_______ 。
(4)H2O 与H2S为同族元素的氢化物,H2O可以形成H9O4+以或H3O+,而H2S几乎不能形成类似的H9S4+或H3S+,其原因是__________
(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃ ,其晶胞结构如图所示。
① 磷化铝的晶体类型为________ 。
② A、B点的原子坐标如图所示,则C点的原子坐标为_________ 。
③ 磷化铝的晶胞参数a=546.35pm,其密度为________ (列出计算式即可,用从表示阿伏伽德罗常数的数值)g/cm3。
(1)基态砷原子的核外价电子排布式为
(2)生产农药的原料PSCl3中P、S、Cl的第一电离能由大到小的顺序为
(3)COS(羰基硫)可用作粮食的熏蒸剂,其中碳原子的杂化轨道类型为
(4)H2O 与H2S为同族元素的氢化物,H2O可以形成H9O4+以或H3O+,而H2S几乎不能形成类似的H9S4+或H3S+,其原因是
(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃ ,其晶胞结构如图所示。

① 磷化铝的晶体类型为
② A、B点的原子坐标如图所示,则C点的原子坐标为
③ 磷化铝的晶胞参数a=546.35pm,其密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】金属及其化合物在生产生活中有着广泛应用。回答下列问题:
(1)①基态铜原子中,其占据最高能层的符号是___ 。
②锰、锝、铼位于同一副族且原子序数依次增大。类比锰,写出基态锝原子价层电子排布式___ 。
(2)下列状态的铁中,电离最外层的一个电子所需能量最大的是___ (填编号)。
A. B.
B. C.
C. D.
D.
(3)NH3在高温条件下能还原CuO,2NH3+3CuO 3Cu+N2+3H2O,反应中所涉及的所有元素的电负性由大到小的顺序为
3Cu+N2+3H2O,反应中所涉及的所有元素的电负性由大到小的顺序为___ (填元素符号);S元素与多种金属非金属元素形成化合物,SiS2的结构与CS2类似,则SiS2分子的空间构型为___ 。
(4)一种含Cu、S元素的有机物的结构简式如图1所示,N原子的杂化方式为___ 。

(5)超硬材料氮化铂的一种晶胞如图2所示,与N等距最近Pt的原子个数是___ ,若该晶胞参数为apm,密度为ρg·cm-3,则阿伏加德罗常数(NA)为___ mol-1(用含a、ρ的式子表示,并化成最简)
(6)Cl2可氧化KSCN溶液。查阅资料可知SCN-中氮元素转化为NO 。如图3所示,取A中溶液于试管中,加入用HCl酸化的BaCl2溶液,产生白色沉淀。写出SCN-与Cl2反应的离子方程式为
。如图3所示,取A中溶液于试管中,加入用HCl酸化的BaCl2溶液,产生白色沉淀。写出SCN-与Cl2反应的离子方程式为___ 。
(1)①基态铜原子中,其占据最高能层的符号是
②锰、锝、铼位于同一副族且原子序数依次增大。类比锰,写出基态锝原子价层电子排布式
(2)下列状态的铁中,电离最外层的一个电子所需能量最大的是
A.
 B.
B. C.
C. D.
D.
(3)NH3在高温条件下能还原CuO,2NH3+3CuO
 3Cu+N2+3H2O,反应中所涉及的所有元素的电负性由大到小的顺序为
3Cu+N2+3H2O,反应中所涉及的所有元素的电负性由大到小的顺序为(4)一种含Cu、S元素的有机物的结构简式如图1所示,N原子的杂化方式为

(5)超硬材料氮化铂的一种晶胞如图2所示,与N等距最近Pt的原子个数是
(6)Cl2可氧化KSCN溶液。查阅资料可知SCN-中氮元素转化为NO
 。如图3所示,取A中溶液于试管中,加入用HCl酸化的BaCl2溶液,产生白色沉淀。写出SCN-与Cl2反应的离子方程式为
。如图3所示,取A中溶液于试管中,加入用HCl酸化的BaCl2溶液,产生白色沉淀。写出SCN-与Cl2反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
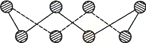
(1) S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是______ ;
(2) 原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为________________ ;
(3) Se原子序数为______ ,其核外M层电子的排布式为______ ;
(4) H2Se的酸性比H2S__________ (填“强”或“弱”)。气态SeO3分子的立体构型为______ ,SO32-离子的立体构型为______ ;
(5) H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,
K2为1.2×10-2,请根据结构与性质的关系解释:
① H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:__________ ;
② H2SeO4比H2SeO3酸性强的原因:______ ;
(6)电镀厂排放的废水中常含有剧毒的CN-离子,可在X的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。
① H、C、N、O四种元素的电负性由小到大的顺序为_______________________ 。
② 与CNO-互为等电子体微粒的化学式为_________________ (写出一种即可)。
③ 氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式________________ 。
(7)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++xR-H―→Rx[CrCln(H2O)6-n]+xH+交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。
将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,可知该配离子的化学式为___
(1) S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是
(2) 原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为
(3) Se原子序数为
(4) H2Se的酸性比H2S
(5) H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,
K2为1.2×10-2,请根据结构与性质的关系解释:
① H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:
② H2SeO4比H2SeO3酸性强的原因:
(6)电镀厂排放的废水中常含有剧毒的CN-离子,可在X的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。
① H、C、N、O四种元素的电负性由小到大的顺序为
② 与CNO-互为等电子体微粒的化学式为
③ 氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式
(7)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++xR-H―→Rx[CrCln(H2O)6-n]+xH+交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。
将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,可知该配离子的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度等特性,被美誉为“未来钢铁”“战略金属”。
 基态钛原子核外电子有
基态钛原子核外电子有________ 种不同的空间运动状态,基态钛原子简化的电子排布式为________ ,区分晶态 和非晶态
和非晶态 最可靠的科学方法是对固体进行
最可靠的科学方法是对固体进行________ 。
 钙钛矿
钙钛矿 可应用于发光二极管。与钙元素同周期且最外层电子数相同的元素有种,氧元素可以与氯元素形成化合物
可应用于发光二极管。与钙元素同周期且最外层电子数相同的元素有种,氧元素可以与氯元素形成化合物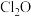 ,其中氧原子的杂化方式为
,其中氧原子的杂化方式为________ ,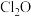 的空间构型为
的空间构型为________ 。
 在浓的
在浓的 的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为
的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为 的绿色晶体,该晶体中两种配体的物质的量之比为
的绿色晶体,该晶体中两种配体的物质的量之比为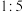 ,则该配离子的化学式为
,则该配离子的化学式为________ 。
 钛在较高温度下可与氧或氮元素及其化合物发生反应,O、N元素形成的简单氢化物的键角前者小于后者的原因是
钛在较高温度下可与氧或氮元素及其化合物发生反应,O、N元素形成的简单氢化物的键角前者小于后者的原因是________ 。

 钛酸钙的晶胞结构如图所示,晶胞中两个最近的氧原子之间的距离为apm,晶胞中钛的氧配位数为
钛酸钙的晶胞结构如图所示,晶胞中两个最近的氧原子之间的距离为apm,晶胞中钛的氧配位数为________ ,晶胞的密度为________  。
。
 基态钛原子核外电子有
基态钛原子核外电子有 和非晶态
和非晶态 最可靠的科学方法是对固体进行
最可靠的科学方法是对固体进行 钙钛矿
钙钛矿 可应用于发光二极管。与钙元素同周期且最外层电子数相同的元素有种,氧元素可以与氯元素形成化合物
可应用于发光二极管。与钙元素同周期且最外层电子数相同的元素有种,氧元素可以与氯元素形成化合物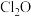 ,其中氧原子的杂化方式为
,其中氧原子的杂化方式为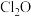 的空间构型为
的空间构型为 在浓的
在浓的 的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为
的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为 的绿色晶体,该晶体中两种配体的物质的量之比为
的绿色晶体,该晶体中两种配体的物质的量之比为 ,则该配离子的化学式为
,则该配离子的化学式为 钛在较高温度下可与氧或氮元素及其化合物发生反应,O、N元素形成的简单氢化物的键角前者小于后者的原因是
钛在较高温度下可与氧或氮元素及其化合物发生反应,O、N元素形成的简单氢化物的键角前者小于后者的原因是
 钛酸钙的晶胞结构如图所示,晶胞中两个最近的氧原子之间的距离为apm,晶胞中钛的氧配位数为
钛酸钙的晶胞结构如图所示,晶胞中两个最近的氧原子之间的距离为apm,晶胞中钛的氧配位数为 。
。
您最近一年使用:0次
【推荐3】氟及其化合物用途非常广泛。回答下列问题:
(1)基态F原子价层电子的轨道表达式为____ ,其核外电子中占据能量最高的能级的电子云轮廓图为____ 。
(2)[H2F]+[SbF6]-(氟酸锑)是一种超强酸,其中[H2F]+离子的空间构型为____ ,写出一种与[H2F]+具有相同空间构型和键合形式的微粒____ 。
(3)H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序____ (填元素符号),BF 中B原子的杂化方式为
中B原子的杂化方式为____ 。
(4)SF6被广泛用作高压电气设备绝缘介质。SF6是一种共价化合物,可通过类似于Born—Haber循环能量构建能量图(见图a)计算相联系的键能。则S—F的键能为____ kJ·mol-1。

(5)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。
①CuF比CuCl熔点高的原因是____ 。
②已知NA为阿伏加德罗常数。CuF的晶胞结构如“图b”。则CuF的晶胞参数a=____ nm(列出计算式)。

(1)基态F原子价层电子的轨道表达式为
(2)[H2F]+[SbF6]-(氟酸锑)是一种超强酸,其中[H2F]+离子的空间构型为
(3)H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序
 中B原子的杂化方式为
中B原子的杂化方式为(4)SF6被广泛用作高压电气设备绝缘介质。SF6是一种共价化合物,可通过类似于Born—Haber循环能量构建能量图(见图a)计算相联系的键能。则S—F的键能为

(5)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。
①CuF比CuCl熔点高的原因是
②已知NA为阿伏加德罗常数。CuF的晶胞结构如“图b”。则CuF的晶胞参数a=

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】钛被誉为“21世纪的金属”,可呈现多种化合价。其中以+4价的Ti最为稳定。回答下列问题:
(1)基态Ti原子的价电子排布式为___________ ,核外不同空间运动状态的电子数为___________ 种。
(2)已知电离能:I2(Ti)=1310kJ·mol-1,I2(K)=3051kJ·mol-1.I2(Ti)<I2(K),其原因为___________ 。
(3)钛某配合物可用于催化环烯烃聚合,其结构如下图所示:

①钛的配位数为___________ ,碳原子的杂化类型有___________ 种。
②该配合物中存在的化学键有___________ (填字母)。
a.离子键b.配位键c.金属键d.共价键e.氢键
(4)钛与卤素形成的化合物熔、沸点如下表所示:
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是___________ 。
(5)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为___________ ,阴离子的立体构型为___________ 。

(6)已知TiN晶体的晶胞结构如下图所示,若该晶胞的密度为ρg·cm-3,阿伏加德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为___________ pm。(用含ρ、NA的代数式表示)

(1)基态Ti原子的价电子排布式为
(2)已知电离能:I2(Ti)=1310kJ·mol-1,I2(K)=3051kJ·mol-1.I2(Ti)<I2(K),其原因为
(3)钛某配合物可用于催化环烯烃聚合,其结构如下图所示:

①钛的配位数为
②该配合物中存在的化学键有
a.离子键b.配位键c.金属键d.共价键e.氢键
(4)钛与卤素形成的化合物熔、沸点如下表所示:
| TiCl4 | TiBr4 | TiI4 | |
| 熔点/℃ | -24.1 | 38.3 | 155 |
| 沸点/℃ | 136.5 | 233.5 | 377 |
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是
(5)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为

(6)已知TiN晶体的晶胞结构如下图所示,若该晶胞的密度为ρg·cm-3,阿伏加德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】储氯合金能有效解决氢气的贮在和输运问题,对大规模使用氢能具有重要的意义。
(1)镍氢电池放电时的总反应为NiOOH+MH = Ni (OH)₂+ M,M表示储氢合金。Ni3+的价层电子排布式为___________ 。
(2)用KF/HF溶液对储氢合金表面进行氟化处理,能改善合金的表面活性。
①HF与水能按任何比例互溶,原因是__________ 。
②已知 ,KHF2晶体中的作用力类型有
,KHF2晶体中的作用力类型有__________ 。
(3)用KBH4和NaH2PO4处理储氢合金电极。KBH4中阴离子的空间构型是_________ 。NaH2PO4中阴离子中心原子的杂化类型是_________ 。
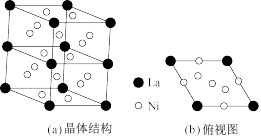
(4)某储氢合金的结构属六方晶系,晶体结构(底面夹角为60度)及俯视图分别如下图(a). (b)所示,该储氢合金的化学式是_____ ( 填最简式)。已知该储氢合金晶胞底边长为a=0.5017nm,高为c=0.3977nm,设阿伏加德罗常数的值为NA,该晶体的密度为____ g·cmˉ³(列出计算式)。
(1)镍氢电池放电时的总反应为NiOOH+MH = Ni (OH)₂+ M,M表示储氢合金。Ni3+的价层电子排布式为
(2)用KF/HF溶液对储氢合金表面进行氟化处理,能改善合金的表面活性。
①HF与水能按任何比例互溶,原因是
②已知
 ,KHF2晶体中的作用力类型有
,KHF2晶体中的作用力类型有(3)用KBH4和NaH2PO4处理储氢合金电极。KBH4中阴离子的空间构型是
(4)某储氢合金的结构属六方晶系,晶体结构(底面夹角为60度)及俯视图分别如下图(a). (b)所示,该储氢合金的化学式是

您最近一年使用:0次
【推荐3】 及其化合物在化工、医药、材料等方面应用十分广泛.回答下列有关问题:
及其化合物在化工、医药、材料等方面应用十分广泛.回答下列有关问题:
(1)N基态原子核外电子的空间运动状态有_______ 种,与 同周期且基态原子核外未成对电子数与
同周期且基态原子核外未成对电子数与 相同的元素还有
相同的元素还有_______ 种。
(2)碳元素的单质有多种形式,如图所示,依次是 、石墨和金刚石的结构图:
、石墨和金刚石的结构图:

 属于
属于_______ 晶体,石墨晶体中,层内 键的键长小于金刚石中
键的键长小于金刚石中 键的键长,其原因是金刚石中只存在
键的键长,其原因是金刚石中只存在 间的
间的_______ 共价键,而石墨层内的 间不仅存在该键,还有
间不仅存在该键,还有_______ 键。
(3)比较下列卤化物的熔点和沸点,分析其变化规律及原因_______ .
(4)磷、硼形成的一种化合物为立方晶系晶体,沿体对角线投影如图所示:

该晶胞中原子的分数坐标为:

则该晶胞中,与B原子紧邻的P原子有_______ 个,若阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为 ,则
,则 键键长为
键键长为_______ pm(列出计算式)
 及其化合物在化工、医药、材料等方面应用十分广泛.回答下列有关问题:
及其化合物在化工、医药、材料等方面应用十分广泛.回答下列有关问题:(1)N基态原子核外电子的空间运动状态有
 同周期且基态原子核外未成对电子数与
同周期且基态原子核外未成对电子数与 相同的元素还有
相同的元素还有(2)碳元素的单质有多种形式,如图所示,依次是
 、石墨和金刚石的结构图:
、石墨和金刚石的结构图:
 属于
属于 键的键长小于金刚石中
键的键长小于金刚石中 键的键长,其原因是金刚石中只存在
键的键长,其原因是金刚石中只存在 间的
间的 间不仅存在该键,还有
间不仅存在该键,还有(3)比较下列卤化物的熔点和沸点,分析其变化规律及原因
 |  |  |  |  | |
| 熔点/℃ |  | 26 | 146 | 993 | 1248 |
| 沸点/℃ | 83.1 | 186 | 约400 | 1704 | 2260 |
(4)磷、硼形成的一种化合物为立方晶系晶体,沿体对角线投影如图所示:

该晶胞中原子的分数坐标为:


则该晶胞中,与B原子紧邻的P原子有
 ,该晶体的密度为
,该晶体的密度为 ,则
,则 键键长为
键键长为
您最近一年使用:0次



