碳族化合物在研究和生产中有许多重要用途,请回答下列问题:
(1)已知 中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为
中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为_______ 。
(2)基态锗原子(Ge)价层电子的轨道表示式为_______ 。
(3)邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点低;请解释其原因_______ 。
(4)氮化硅( )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N_______ Si—N—Si(填“>”“<”“=”)。
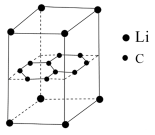
(5)某锂电池的负极材料是将锂原子嵌入到两层石墨烯层中间,其晶体结构如图。已知该晶体中最近的两个碳原子核间距离为a nm,石墨烯层间距离为b nm,则该晶体的密度为_______  (用
(用 表示阿伏加德罗常数,列式即可)。
表示阿伏加德罗常数,列式即可)。
(1)已知
 中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为
中硅元素为+4价,则H、Si、O、C的电负性由大到小的顺序为(2)基态锗原子(Ge)价层电子的轨道表示式为
(3)邻羟基苯甲酸的沸点比对羟基苯甲酸的沸点低;请解释其原因
(4)氮化硅(
 )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且均达到8电子稳定结构,请比较晶体结构中键角大小:N—Si—N
(5)某锂电池的负极材料是将锂原子嵌入到两层石墨烯层中间,其晶体结构如图。已知该晶体中最近的两个碳原子核间距离为a nm,石墨烯层间距离为b nm,则该晶体的密度为
 (用
(用 表示阿伏加德罗常数,列式即可)。
表示阿伏加德罗常数,列式即可)。
22-23高三上·浙江·开学考试 查看更多[3]
浙江省名校协作体2022-2023学年高三上学期开学考试化学试题(已下线)2023年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷B(已下线)专题02 物质结构专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
更新时间:2022-09-02 20:19:00
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】我国已经形成对全球稀土产业链的统治力,在稀土开采技术方面,我国遥遥领先,无论是美国的芒廷帕斯还是澳大利亚的稀土矿山,均为在我国技术的参与下才实现产出。我国科学家最早研究的是稀土—钴化合物的结构。请回答下列问题:
(1)钴原子的价层电子排布图为_________ ,其M层上共有______ 个不同运动状态的电子。
(2)已知:配合物中,配位体中含有一个配位原子的配体称为单齿配体;一个配体中有两个或两个以上配位原子的配体称为多齿配体。[Co(NO3)4]2-中Co2+的配位数为4,该配离子中各元素第一电离能由大到小的顺序_______ (填元素符号),1mol该离子中含σ键数目为_________ 。
(3)①Co的某配合物化学式为CoCl3·3NH3,为八面体结构,其中极性分子有___ 种。
②该配合物在热NaOH溶液中发生反应产生沉淀,并释放出气体,该反应的化学方程式_________ 。
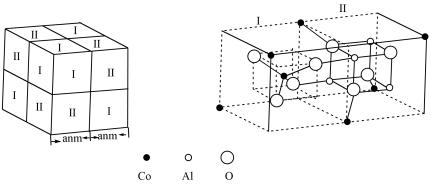
(4)钴蓝晶体结构如下图,该立方晶胞由I型和II型小立方体各4个构成,其化学式为_____ ,晶体中Al3+占据O2-形成的_____ (填“四面体”或者“八面体”)空隙,NA为阿伏加德罗常数的值,设化学式对应的摩尔质量为Mg/mol,则钴蓝晶体的密度计算式为_________ g/cm3。
(1)钴原子的价层电子排布图为
(2)已知:配合物中,配位体中含有一个配位原子的配体称为单齿配体;一个配体中有两个或两个以上配位原子的配体称为多齿配体。[Co(NO3)4]2-中Co2+的配位数为4,该配离子中各元素第一电离能由大到小的顺序
(3)①Co的某配合物化学式为CoCl3·3NH3,为八面体结构,其中极性分子有
②该配合物在热NaOH溶液中发生反应产生沉淀,并释放出气体,该反应的化学方程式
(4)钴蓝晶体结构如下图,该立方晶胞由I型和II型小立方体各4个构成,其化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C、D、E五种元素的原子序数依次增大,A原子无中子,B的单质在空气中含量最多,C、D元素同主族且原子序数D为C的二倍,E元素的价电子排布式为(n-l)dn+6ns1。回答下列问题:
(1)元素B在周期表中的位置是__________________ ;E元素的元素符号为______ ,它能形成E+的原因为___________________________________________________ 。
(2)D元素基态原子的核外电子轨道排布图为______________  。
。
(3)A元素与C元素形成两种常见的化合物,其原子个数比分别为2:1和1:1,两种化合物可以任意比互溶,原因是____________________ ;其中一种化合物可在酸性条件下将KMnO4还原为Mn2+,相关反应的离子方程式为___________________ 。
(1)元素B在周期表中的位置是
(2)D元素基态原子的核外电子轨道排布图为
 。
。(3)A元素与C元素形成两种常见的化合物,其原子个数比分别为2:1和1:1,两种化合物可以任意比互溶,原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】FeSe、MgB2、Nb3Al等超导材料具有广泛应用前景。
(1)Fe2+基态价电子的轨道表示式(价电子排布图)__ ,Se、Mg、B三种元素的电负性大小顺序是__ 。
(2)蒸气状态下以二聚分子存在的A1Cl3的结构式是___ ,其中A1原子的杂化方式是___ ,分子中八个原子___ (选填“是”或“不是”)在同一平面上,该分子是____ (选填“极性“或“非极性“)分子。
(3)制备FeSe基超导材料Li0.6(NH2)0.2(NH3)0.8Fe2Se2过程中需将金属锂溶于液氨,从而制得具有很高反应活性的金属电子溶液,反应为:Li+(m+n)NH3—X+e-(NH3)n。
①X的化学式为____ ;
②NH3的价层电子对互斥模型是____ 。
(4)MgB2晶体结构中的B原子层具有类似石墨的层状结构,且被六方密排的Mg原子层隔开,B原子位于Mg原子组成的三棱柱的中心。已知:平面中Mg原子间的最近核间距为acm,平面间Mg原子间的最近核间距为bcm,阿伏加 德罗常数为NA。

①B原子层六元环中处于对位的B原子核间距为____ cm。
②MgB2晶体的密度是____ g·cm-3。
(1)Fe2+基态价电子的轨道表示式(价电子排布图)
(2)蒸气状态下以二聚分子存在的A1Cl3的结构式是
(3)制备FeSe基超导材料Li0.6(NH2)0.2(NH3)0.8Fe2Se2过程中需将金属锂溶于液氨,从而制得具有很高反应活性的金属电子溶液,反应为:Li+(m+n)NH3—X+e-(NH3)n。
①X的化学式为
②NH3的价层电子对互斥模型是
(4)MgB2晶体结构中的B原子层具有类似石墨的层状结构,且被六方密排的Mg原子层隔开,B原子位于Mg原子组成的三棱柱的中心。已知:平面中Mg原子间的最近核间距为acm,平面间Mg原子间的最近核间距为bcm,阿伏加 德罗常数为NA。

①B原子层六元环中处于对位的B原子核间距为
②MgB2晶体的密度是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】下表为长式周期表的一部分其中的编号代表对应的元素。
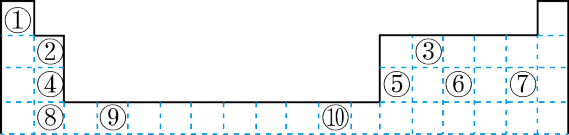
请回答下列问题:
(1)表中属于 ds 区的元素是___________ (填元素符号)它的基态原子的价电子排布式为___________ 。
(2)表中元素①的 6 个原子与元素③的 6 个原子形成的某种平面环状分子其分子式为___________ ,其中元素③的基态原子的电子排布图为_______ ;①和⑥形成的一种常见四原子分子的化学式为_______ ,该分子的立体构型为______ 。
(3)某元素原子的价电子排布式为 nsnnpn+1,该元素原子的电子层上未成对电子数为___________ ;该元素与元素①形成的最简单分子 X 的电子式为___________ 。
(4)元素⑤的电负性___________ ④元素的电负性(选填>、=、<下同);元素⑥的第一电离能___________ 原子序数为 16 的元素的第一电离能。
(5)用电子式表示元素④和⑦组成的化合物的形成过程___________ 。

请回答下列问题:
(1)表中属于 ds 区的元素是
(2)表中元素①的 6 个原子与元素③的 6 个原子形成的某种平面环状分子其分子式为
(3)某元素原子的价电子排布式为 nsnnpn+1,该元素原子的电子层上未成对电子数为
(4)元素⑤的电负性
(5)用电子式表示元素④和⑦组成的化合物的形成过程
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】新型铜锌锡硫化合物(CuxZnySnzSn)薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:
(1)Si、P、S三种元素中第一电离能最小的是___________ ,电负性最大的元素是___________ 。
(2)比较SO 和SO
和SO 中键角大小,并解释原因
中键角大小,并解释原因___________ 。
(3)某单质晶体的晶胞如下图,已知a微粒的原子坐标为(1,1,1)b微粒的原子坐标为___________ 。其晶胞俯视图为(II中选择)___________ ,
(I)
(II)A、 B、
B、 C、
C、 D、
D、
(4)Na3OCl晶体属于立方晶系,其晶胞结构如图所示。
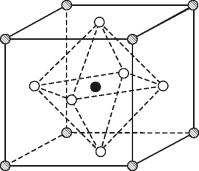
已知:晶胞参数(边长)为anm,密度为dg·cm-3
①Na3OCl晶胞中,Cl位于各顶点位置,Na位于___________ 位置,两个Na之间的最短距离为___________ nm。
②用a、d表示阿伏加德罗常数的值
___________ (列计算式)。
(1)Si、P、S三种元素中第一电离能最小的是
(2)比较SO
 和SO
和SO 中键角大小,并解释原因
中键角大小,并解释原因(3)某单质晶体的晶胞如下图,已知a微粒的原子坐标为(1,1,1)b微粒的原子坐标为
(I)

(II)A、
 B、
B、 C、
C、 D、
D、
(4)Na3OCl晶体属于立方晶系,其晶胞结构如图所示。

已知:晶胞参数(边长)为anm,密度为dg·cm-3
①Na3OCl晶胞中,Cl位于各顶点位置,Na位于
②用a、d表示阿伏加德罗常数的值

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为____ 。
(2)基态Ge原子核外电子排布式为____ ;SiO2、GeO2具有类似的晶体结构,其中熔点较高的是___ ,原因是____ 。
(3)如图1为H3BO3晶体的片层结构,其中B的杂化方式为____ ;硼酸在热水中比在冷水中溶解度显著增大的主要原因是____ 。

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形),晶胞参数为apm、bpm和cpm。如图2为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为___ ;CsSiB3O7的摩尔质量为Mg•mol-1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为___ g•cm-3(用代数式表示)。

(1)C、O、Si三种元素电负性由大到小的顺序为
(2)基态Ge原子核外电子排布式为
(3)如图1为H3BO3晶体的片层结构,其中B的杂化方式为

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形),晶胞参数为apm、bpm和cpm。如图2为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】高技术领域常使用高纯试剂。纯磷酸(熔点为 ,易吸潮)可通过市售85%磷酸溶液减压蒸馏除水、结晶除杂得到,纯化过程需要严格控制温度和水分,温度低于
,易吸潮)可通过市售85%磷酸溶液减压蒸馏除水、结晶除杂得到,纯化过程需要严格控制温度和水分,温度低于 易形成
易形成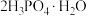 (熔点为
(熔点为 ),高于
),高于 则发生分子间脱水生成焦磷酸等。某兴趣小组为制备磷酸晶体设计的实验装置如下(夹持装置略):
则发生分子间脱水生成焦磷酸等。某兴趣小组为制备磷酸晶体设计的实验装置如下(夹持装置略):

回答下列问题:
(1)A的名称是___________ 。B的进水口为___________ (填“a”或“b”)。
(2) 的作用是
的作用是___________ 。
(3)空气流入毛细管的主要作用是防止___________ ,还具有搅拌和加速水逸出的作用。
(4)升高温度能提高除水速度,实验选用水浴加热的目的是___________ 。
(5)磷酸易形成过饱和溶液,难以结晶,可向过饱和溶液中加入___________ 促进其结晶。
(6)过滤磷酸晶体时,除了需要干燥的环境外,还需要控制温度为___________ (填标号)。
A. B.
B. C.
C.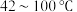
(7)磷酸中少量的水极难除去的原因是___________ 。
 ,易吸潮)可通过市售85%磷酸溶液减压蒸馏除水、结晶除杂得到,纯化过程需要严格控制温度和水分,温度低于
,易吸潮)可通过市售85%磷酸溶液减压蒸馏除水、结晶除杂得到,纯化过程需要严格控制温度和水分,温度低于 易形成
易形成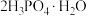 (熔点为
(熔点为 ),高于
),高于 则发生分子间脱水生成焦磷酸等。某兴趣小组为制备磷酸晶体设计的实验装置如下(夹持装置略):
则发生分子间脱水生成焦磷酸等。某兴趣小组为制备磷酸晶体设计的实验装置如下(夹持装置略):
回答下列问题:
(1)A的名称是
(2)
 的作用是
的作用是(3)空气流入毛细管的主要作用是防止
(4)升高温度能提高除水速度,实验选用水浴加热的目的是
(5)磷酸易形成过饱和溶液,难以结晶,可向过饱和溶液中加入
(6)过滤磷酸晶体时,除了需要干燥的环境外,还需要控制温度为
A.
 B.
B. C.
C.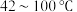
(7)磷酸中少量的水极难除去的原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
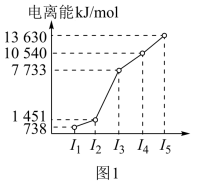
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素原子核外有______ 种不同运动状态的电子。
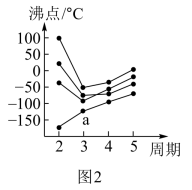
(2)如图2所示,每条折线表示周期表第ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是______ 。
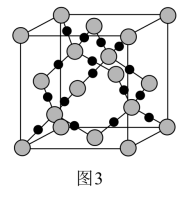
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于______ 晶体。
(4)第一电离能介于Al、P之间的第三周期元素有_______ 种。
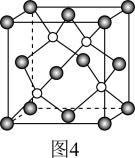
(5)图4是碳化硅的晶胞结构。若碳化硅晶胞边长为apm,阿伏加德罗常数的值为NA,则碳化硅晶体的密度为_______ g/cm3(列出计算式即可)。
(6)浓磷酸在200~300℃时脱水生成焦磷酸(化学式:H4P2O7),焦磷酸的结构式为______ 。
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素原子核外有

(2)如图2所示,每条折线表示周期表第ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于

(4)第一电离能介于Al、P之间的第三周期元素有
(5)图4是碳化硅的晶胞结构。若碳化硅晶胞边长为apm,阿伏加德罗常数的值为NA,则碳化硅晶体的密度为

(6)浓磷酸在200~300℃时脱水生成焦磷酸(化学式:H4P2O7),焦磷酸的结构式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】以Cu2O、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
(1)基态O原子的电子排布式_____ 。
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_____ 。
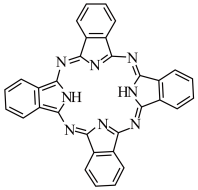
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取_____ 杂化。邻苯二甲酸酐(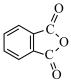 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是_____ 。
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_____ 。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn—N键中离子键成分的百分数小于Zn—O键,原因是_____ 。
(6)AlCl3可用作有机反应的催化剂。在AlCl3催化下,乙酰氯的部分反应历程如图:

①乙酰氯分子中C—C键与C—Cl键的夹角_____ 120°(填“大于”、“等于”或“小于”)。
②请写出一种与AlCl 互为等电子体的分子
互为等电子体的分子_____ 。
(1)基态O原子的电子排布式
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取
 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn—N键中离子键成分的百分数小于Zn—O键,原因是
(6)AlCl3可用作有机反应的催化剂。在AlCl3催化下,乙酰氯的部分反应历程如图:

①乙酰氯分子中C—C键与C—Cl键的夹角
②请写出一种与AlCl
 互为等电子体的分子
互为等电子体的分子
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】按照要求回答下列问题。
(1)高温下,Cu2O比CuO稳定,原因是___________ 。
(2)过渡元素的原子或者离子很容易形成配合物,Fe(CO)5就是其一,它相当活泼,在一定条件下可生成Fe(CO)3(CH3OH)。1.5 mol Fe(CO)5中所含配位键的个数为___________ ,Fe(CO)3(CH3OH)的配位原子为___________ 。(填元素符号)
(3)第四周期第一电离能数值介于Ga和As之间的主族元素有:___________ 。(填名称)
(4)金属钛重量轻、强度高,航空发动机用的高温钛合金和机体用的结构钛合金是钛合金的主要发展方向。钛原子的外围电子排布图为___________ 。已知金属Be的堆积方式与金属钛相同,则堆积方式为___________ ,Be与NaOH溶液反应的离子方程式为___________ 。
(5)Sr晶体堆积方式与Cu相似,设Sr的原子直径为a,则Sr晶体的空间利用率为___________ 。(请用含有a的表达式表示,不要化简)
(1)高温下,Cu2O比CuO稳定,原因是
(2)过渡元素的原子或者离子很容易形成配合物,Fe(CO)5就是其一,它相当活泼,在一定条件下可生成Fe(CO)3(CH3OH)。1.5 mol Fe(CO)5中所含配位键的个数为
(3)第四周期第一电离能数值介于Ga和As之间的主族元素有:
(4)金属钛重量轻、强度高,航空发动机用的高温钛合金和机体用的结构钛合金是钛合金的主要发展方向。钛原子的外围电子排布图为
(5)Sr晶体堆积方式与Cu相似,设Sr的原子直径为a,则Sr晶体的空间利用率为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】Ⅰ.MnS 纳米粒子被广泛应用于除去重金属离子中的隔离子。
(1)锰的价层电子排布式为_______ 。
(2)磁性氧化铁纳米粒子除隔效率不如 MnS 纳米粒子,试比较两种纳米材料中的阴离子的半径大小O2-_______ S2-(填>、<或=)。H3O+中H-O-H的键角比H2O中的_______ (填大或小)
(3)Mn 可以形成多种配合物,[Mn(CO)(H2O)2(NH3)3]Cl2·H2O中第二周期元素第一电离能由大到小关系为_______ ,配体H2O中心原子杂化类型为_______ 配体NH3的空间构型为_______ (用文字描述)。
II.(1)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为_______ 。

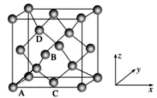
(2)图为金刚石晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______ 。已知金刚石的晶胞参数为a pm,则其密度为_______ g·cm-3(列出计算式)。
(1)锰的价层电子排布式为
(2)磁性氧化铁纳米粒子除隔效率不如 MnS 纳米粒子,试比较两种纳米材料中的阴离子的半径大小O2-
(3)Mn 可以形成多种配合物,[Mn(CO)(H2O)2(NH3)3]Cl2·H2O中第二周期元素第一电离能由大到小关系为
II.(1)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为

(2)图为金刚石晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)属于氟原子激发态的电子排布式有_______ (填字母)。
a. b.
b. c.
c. d.
d.
(2)第三周期部分主族元素的氟化物的熔点(见表):
 比
比 熔点低的原因是
熔点低的原因是_______ 。
(3) 中心原子为
中心原子为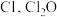 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大π键
中存在大π键 。
。 中
中 原子的轨道杂化方式为
原子的轨道杂化方式为_______ ;比较 与
与 中
中 键的键长并说明原因
键的键长并说明原因_______ 。
(4) 与其他卤素单质反应可以形成卤素互化物,例如
与其他卤素单质反应可以形成卤素互化物,例如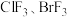 等。已知
等。已知 的键能为
的键能为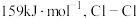 的键能为
的键能为 的键能为
的键能为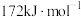 ,写出
,写出 和
和 生成
生成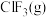 的热化学方程式
的热化学方程式_______ 。
(5)有机卤化铅晶体具有独特的光电性能,下图为其晶胞结构示意图。
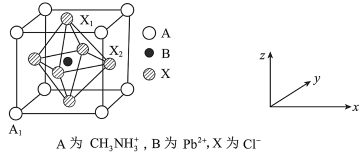
①原子坐标参数 为
为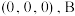 为
为 ,则
,则 为
为_______ 。
②在该晶胞的另一种表达方式中,若图中 处于顶点位置,则
处于顶点位置,则 处于
处于_______ 位置。
(6)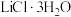 属于正交晶系(长方体形),晶胞参数为
属于正交晶系(长方体形),晶胞参数为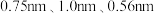 。下图为沿z轴投影的晶胞中所有氯原子的分布图和原子分数坐标。
。下图为沿z轴投影的晶胞中所有氯原子的分布图和原子分数坐标。
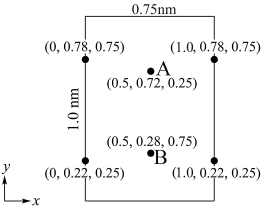
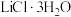 的摩尔质量为
的摩尔质量为 ,晶胞密度为
,晶胞密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为_______  (列出计算式)。
(列出计算式)。
(1)属于氟原子激发态的电子排布式有
a.
 b.
b. c.
c. d.
d.
(2)第三周期部分主族元素的氟化物的熔点(见表):
| 化合物 |  |  |  |  |
| 熔点/℃ | 993 | 1040 | 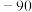 | 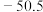 |
 比
比 熔点低的原因是
熔点低的原因是(3)
 中心原子为
中心原子为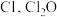 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大π键
中存在大π键 。
。 中
中 原子的轨道杂化方式为
原子的轨道杂化方式为 与
与 中
中 键的键长并说明原因
键的键长并说明原因(4)
 与其他卤素单质反应可以形成卤素互化物,例如
与其他卤素单质反应可以形成卤素互化物,例如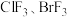 等。已知
等。已知 的键能为
的键能为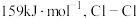 的键能为
的键能为 的键能为
的键能为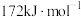 ,写出
,写出 和
和 生成
生成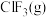 的热化学方程式
的热化学方程式(5)有机卤化铅晶体具有独特的光电性能,下图为其晶胞结构示意图。

①原子坐标参数
 为
为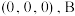 为
为 ,则
,则 为
为②在该晶胞的另一种表达方式中,若图中
 处于顶点位置,则
处于顶点位置,则 处于
处于(6)
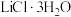 属于正交晶系(长方体形),晶胞参数为
属于正交晶系(长方体形),晶胞参数为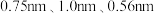 。下图为沿z轴投影的晶胞中所有氯原子的分布图和原子分数坐标。
。下图为沿z轴投影的晶胞中所有氯原子的分布图和原子分数坐标。
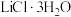 的摩尔质量为
的摩尔质量为 ,晶胞密度为
,晶胞密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次



