下表为长式周期表的一部分其中的编号代表对应的元素。
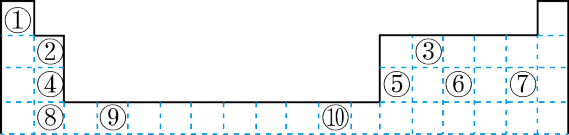
请回答下列问题:
(1)表中属于 ds 区的元素是___________ (填元素符号)它的基态原子的价电子排布式为___________ 。
(2)表中元素①的 6 个原子与元素③的 6 个原子形成的某种平面环状分子其分子式为___________ ,其中元素③的基态原子的电子排布图为_______ ;①和⑥形成的一种常见四原子分子的化学式为_______ ,该分子的立体构型为______ 。
(3)某元素原子的价电子排布式为 nsnnpn+1,该元素原子的电子层上未成对电子数为___________ ;该元素与元素①形成的最简单分子 X 的电子式为___________ 。
(4)元素⑤的电负性___________ ④元素的电负性(选填>、=、<下同);元素⑥的第一电离能___________ 原子序数为 16 的元素的第一电离能。
(5)用电子式表示元素④和⑦组成的化合物的形成过程___________ 。

请回答下列问题:
(1)表中属于 ds 区的元素是
(2)表中元素①的 6 个原子与元素③的 6 个原子形成的某种平面环状分子其分子式为
(3)某元素原子的价电子排布式为 nsnnpn+1,该元素原子的电子层上未成对电子数为
(4)元素⑤的电负性
(5)用电子式表示元素④和⑦组成的化合物的形成过程
更新时间:2021-02-22 16:35:25
|
相似题推荐
【推荐1】铁及其化合物有重要且广泛的应用
(1)基态Fe2+的价层电子排布图为_____________ 。
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______ 。
(3)部分电离能数据如下表:
根据表中数据可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是___________________________ 。
(4)已知Fe单质有如图所示的两种常见堆积方式:

其中属于体心立方密堆积的是______  填“a”或“b”
填“a”或“b” ;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为
;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为_________ 。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为___________ g·cm−3。
(1)基态Fe2+的价层电子排布图为
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子
(3)部分电离能数据如下表:
| 元素 | Mn | Fe | |
电离能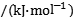 | 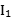 | 717 | 759 |
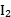 | 1 509 | 1 561 | |
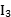 | 3 248 | 2 957 | |
根据表中数据可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是
(4)已知Fe单质有如图所示的两种常见堆积方式:

其中属于体心立方密堆积的是
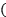 填“a”或“b”
填“a”或“b” ;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为
;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为______ 、______ ;
(2)XZ2与YZ2分子的立体结构分别是______ 和______ ,在水中溶解度较大的是______ (填化学式);
(3)Q元素的电子排布式为______ ,在形成化合物时它的最高化合价为______ ;
(4)Z与E形成的化合物中,各原子最外层都达到8电子结构,该化合物中心原子采用的轨道杂化方式是______ 。
下表为元素周期表中第四周期的部分元素(从左到右按原子序数递增排列),根据要求回答下列问题:
(5)以上元素的基态原子的电子排布中,4s轨道上只有1个电子的元素有______ (填元素名称)。
(6)以上元素中,属于s区的元素有______ 种,属于d区的元素有______ 种。
(7)第一电离能I1(Cr)______ I1(Co)(填“>”“<”或“=”,下同)。
(1)X、Y的元素符号依次为
(2)XZ2与YZ2分子的立体结构分别是
(3)Q元素的电子排布式为
(4)Z与E形成的化合物中,各原子最外层都达到8电子结构,该化合物中心原子采用的轨道杂化方式是
下表为元素周期表中第四周期的部分元素(从左到右按原子序数递增排列),根据要求回答下列问题:
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(5)以上元素的基态原子的电子排布中,4s轨道上只有1个电子的元素有
(6)以上元素中,属于s区的元素有
(7)第一电离能I1(Cr)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
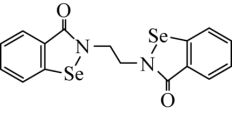
①基态Se原子的价电子排布图为_______ ;
②该新药分子中有_______ 种不同化学环境的C原子;
③比较键角大小:气态SeO3分子_______ 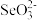 离子(填填“>”、“<”或“=”),原因是
离子(填填“>”、“<”或“=”),原因是_______ 。
(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:
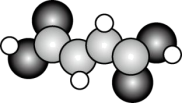
①富马酸分子中σ键与π键的数目比为_______ ;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______ 。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为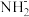 ,反应过程如图所示:
,反应过程如图所示:
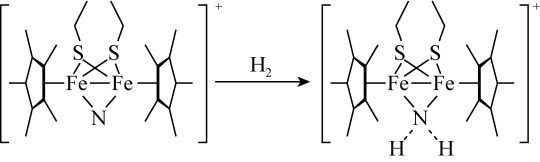
①产物中N原子的杂化轨道类型为_______ ;
②与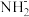 互为等电子体的一种分子为
互为等电子体的一种分子为_______ (填化学式)。
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
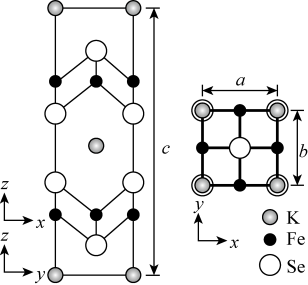
①该超导材料的最简化学式为_______ ;
②Fe原子的配位数为_______ ;
③该晶胞参数a=b=0.4nm、c=1.4nm。阿伏加德罗常数的值为NA,则该晶体的密度为_______ g·cm-1(列出计算式)。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①基态Se原子的价电子排布图为
②该新药分子中有
③比较键角大小:气态SeO3分子
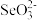 离子(填填“>”、“<”或“=”),原因是
离子(填填“>”、“<”或“=”),原因是(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:

①富马酸分子中σ键与π键的数目比为
②富马酸亚铁中各元素的电负性由大到小的顺序为
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为
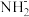 ,反应过程如图所示:
,反应过程如图所示:
①产物中N原子的杂化轨道类型为
②与
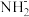 互为等电子体的一种分子为
互为等电子体的一种分子为(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:

①该超导材料的最简化学式为
②Fe原子的配位数为
③该晶胞参数a=b=0.4nm、c=1.4nm。阿伏加德罗常数的值为NA,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】中国是最早发现并使用青铜器的国家。司母戊鼎是迄今为止出土的世界上最大、最重的青铜礼器,享有“镇国之宝”的美誉(如图1)。
(1)Cu原子的外围电子排布式为_____ 。
(2)图2所示为第四周期某主族元素的第一至五电离能数据,该元素是____ ,I3远大于I2的原因是______ 。
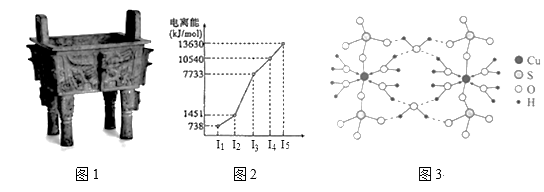
(3)图3是某含铜配合物的晶体结构示意图。
①晶体中H2O和SO42-的中心原子的杂化类型为_____ ,试判断H2O和SO42-的键角大小关系并说明原因_____ 。
②图3中的氢键有(H2O)O—H···O(H2O)和_______ 。
③写出该配合物的化学式_______ 。
(4)一种铜的氯化物晶胞结构如图所示。
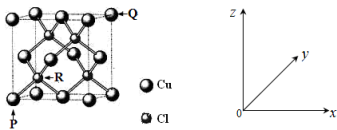
该化合物的化学式为______ ,已知P、Q、R的原子坐标分别(0,0,0)、(1,1,1)、( ,
, ,
, ),若Cu原子与最近的Cl原子的核间距为apm,则该晶体的密度计算表达式为
),若Cu原子与最近的Cl原子的核间距为apm,则该晶体的密度计算表达式为______ 。
(1)Cu原子的外围电子排布式为
(2)图2所示为第四周期某主族元素的第一至五电离能数据,该元素是

(3)图3是某含铜配合物的晶体结构示意图。
①晶体中H2O和SO42-的中心原子的杂化类型为
②图3中的氢键有(H2O)O—H···O(H2O)和
③写出该配合物的化学式
(4)一种铜的氯化物晶胞结构如图所示。

该化合物的化学式为
 ,
, ,
, ),若Cu原子与最近的Cl原子的核间距为apm,则该晶体的密度计算表达式为
),若Cu原子与最近的Cl原子的核间距为apm,则该晶体的密度计算表达式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】2020年,自修复材料、自适应材料、新型传感材料等智能材料技术将大量涌现,为生物医疗、国防军事以及航空航天等领域发展提供支撑。
(1)我国科研工作者基于丁二酮肟氨酯基团的多重反应性,研制了一种强韧、自愈的超级防护材料,
其中的分子机制如图所示。
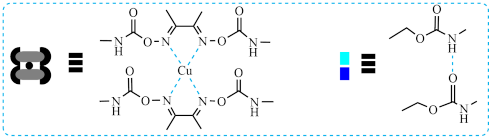
Cu在元素周期表中位于_____ 区,M层中核外电子能量最高的电子云在空间有_____ 个伸展方向。C、N、O第一电离能由大到小的顺序为_____________
(2)氧化石墨烯基水凝胶是一类新型复合材料,对氧化石墨烯进行还原可得到还原氧化石墨烯,二者的结构如图所示:
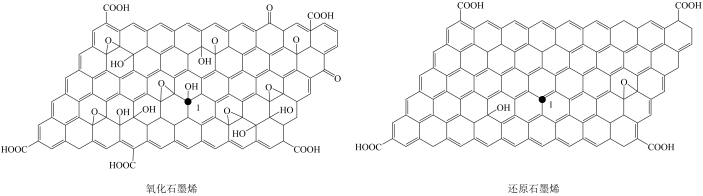
还原石墨烯中碳原子的杂化形式是______ ,上图中氧化石墨烯转化为还原石墨烯时,1号C与其相邻 C原子间键能的变化是_____________ (填“变大”、“变小”或“不变”),二者当中在水溶液中溶解度更大的是____________ (填物质名称),原因为__________________
(3)砷化硼是近期受到广泛关注一种III—V半导体材料。砷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);( ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, );……
);……
As:( ,
, ,
, );(
);( ,
, ,
,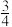 );(
);(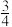 ,
, ,
,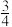 );(
);(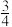 ,
, ,
, )
)
请在图中画出砷化硼晶胞的俯视图 ___________ ,已知晶体密度为dg/cm3,As半径为a pm,假设As、B原子相切,则B原子的半径为_________ pm(写计算表达式)。
(1)我国科研工作者基于丁二酮肟氨酯基团的多重反应性,研制了一种强韧、自愈的超级防护材料,
其中的分子机制如图所示。

Cu在元素周期表中位于
(2)氧化石墨烯基水凝胶是一类新型复合材料,对氧化石墨烯进行还原可得到还原氧化石墨烯,二者的结构如图所示:

还原石墨烯中碳原子的杂化形式是
(3)砷化硼是近期受到广泛关注一种III—V半导体材料。砷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);(
 ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, );……
);……As:(
 ,
, ,
, );(
);( ,
, ,
, );(
);(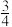 ,
, ,
,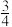 );(
);(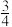 ,
,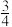 ,
, )
)请在图中

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】X、Y、Z、M、Q、R是元素周期表中前四周期元素,且原子序数依次增大,其相关信息如表所示:
回答下列问题。
(1)X与Q的电负性大小顺序为___________ (用元素符号表示)。
(2)Y元素基态原子的简化电子排布式为___________ ;R元素基态原子的价层电子轨道表示式为___________ 。
(3)R元素可形成 和
和 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(4)Y、Z的电负性较大的是___________ (填元素符号)。
(5)与M元素成对角线规则关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物对应的水化物反应的离子方程式:___________ 。
| 元素 | 相关信息 |
| X | 原子核外有6种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 原子半径在同周期主族元素中最大 |
| M | 逐级电离能(单位: )依次为578、1817、2745、11575、14830、18376、23293 )依次为578、1817、2745、11575、14830、18376、23293 |
| Q | 基态原子的核外电子占据5个能级,且最外层p轨道上有2个电子的自旋方向与其他电子的自旋方向相反 |
| R | 基态原子3d能级上有6个电子 |
(1)X与Q的电负性大小顺序为
(2)Y元素基态原子的简化电子排布式为
(3)R元素可形成
 和
和 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(4)Y、Z的电负性较大的是
(5)与M元素成对角线规则关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】二甲基亚砜(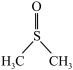 )是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
)是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
(1)铬和锰基态原子核外未成对电子数之比为_______ 。
(2)已知:二甲基亚砜能够与水和丙酮(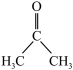 )分别以任意比互溶。
)分别以任意比互溶。
①二甲基亚砜分子中硫原子的杂化类型为_______ 。
②丙酮分子中各原子电负性由大到小的顺序为_______ 。
③二甲基亚砜易溶于水,原因可能为_______ 。
(3)CrCl3·6H2O的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3:2:1,对应的颜色分别为紫色、浅绿色和蓝绿色,其中浅绿色的结构中配离子的化学式为_______ 。
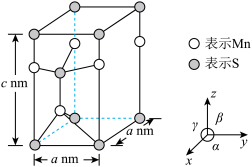
(4)已知硫化锰(MnS)晶胞如图所示,该晶胞参数α=120°,β=γ=90°。
①该晶体中,锰原子周围的硫原子数目为_______ 。
②空间利用率指的是构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分比。已知锰和硫的原子半径分别r1 nm和r2 nm,该晶体中原子的空间利用率为_______ (列出计算式即可)。
 )是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
)是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:(1)铬和锰基态原子核外未成对电子数之比为
(2)已知:二甲基亚砜能够与水和丙酮(
 )分别以任意比互溶。
)分别以任意比互溶。①二甲基亚砜分子中硫原子的杂化类型为
②丙酮分子中各原子电负性由大到小的顺序为
③二甲基亚砜易溶于水,原因可能为
(3)CrCl3·6H2O的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3:2:1,对应的颜色分别为紫色、浅绿色和蓝绿色,其中浅绿色的结构中配离子的化学式为
(4)已知硫化锰(MnS)晶胞如图所示,该晶胞参数α=120°,β=γ=90°。
①该晶体中,锰原子周围的硫原子数目为
②空间利用率指的是构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分比。已知锰和硫的原子半径分别r1 nm和r2 nm,该晶体中原子的空间利用率为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】氰化钾(KCN)是一种有剧毒的物质,贮存和使用时必须注意安全。已知:KCN+H2O2=KOCN+H2O。回答下列问题:
(1)OCN-中所含三种元素的第一电离能从大到小的顺序为_________ (用元素符号表示,下同),电负性从大到小的顺序为________ ;基态氮原子外围电子排布式为__________ 。
(2)H2O2中的共价键类型为_______ (填“σ键”或“π键”) ,其中氧原子的杂化轨道类型为_________ ;分子中4个原子______ (填“在”或“不在”)同一条直线上;H2O2易溶于水除它们都是极性分子外,还因为____________________ 。
(3)与OCN-键合方式相同且互为等电子体的分子为________ (任举一例);在与OCN-互为等电子体的微粒中,由一种元素组成的阴离子是____________ 。
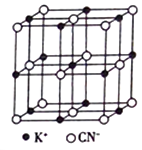
(4)KCN的晶胞结构如图所示。晶体中K+的配位数为_______ ,若其晶胞参数a=0.648nm,则KCN 晶体的密度为_______ g/cm3(列出计算式)。
(1)OCN-中所含三种元素的第一电离能从大到小的顺序为
(2)H2O2中的共价键类型为
(3)与OCN-键合方式相同且互为等电子体的分子为
(4)KCN的晶胞结构如图所示。晶体中K+的配位数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
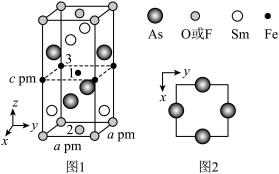
【推荐3】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe—Sm—As—F—O组成的化合物。回答下列问题:
(1)AsH3的沸点比NH3的________ (填“高”或“低”),其判断理由是______ 。
(2)Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为________ 。
(3)一种四方结构的超导化合物的晶胞如图1所示。晶胞中Sm和As原子的投影位置如图2所示。图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表示为____________ ;通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=______________ g·cm-3。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为( ,
,  ,
,  ),则位于底面中心的原子2和铁原子3的坐标分别为
),则位于底面中心的原子2和铁原子3的坐标分别为___________ 、__________ 。

(1)AsH3的沸点比NH3的
(2)Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为
(3)一种四方结构的超导化合物的晶胞如图1所示。晶胞中Sm和As原子的投影位置如图2所示。图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表示为
 ,
,  ,
,  ),则位于底面中心的原子2和铁原子3的坐标分别为
),则位于底面中心的原子2和铁原子3的坐标分别为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】过渡元素中,Ti被誉为“未来金属”、“战略金属”,其具有稳定的化学性质。回答下列问题:
(1)基态钛原子的电子排布式为_______ 。
(2)Ti可形成多种配合物。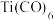 、
、 、
、 的配体所含原子中电负性由大到小的顺序是
的配体所含原子中电负性由大到小的顺序是_______ (写元素符号);CO作配体时,配位原子是C而不是O,其原因是_______ ; 中
中
_______ (填“大于”、“小于”或“等于”)单个水分子中 。
。
(3) 是氧化法制取钛的中间产物。
是氧化法制取钛的中间产物。 的分子结构与
的分子结构与 相同,二者在常温下都是液体。
相同,二者在常温下都是液体。 分子的空间构型是
分子的空间构型是_______ ,其中Ti原子采取_______ 杂化。
(4)如图为四方晶系的 晶体结构:
晶体结构:
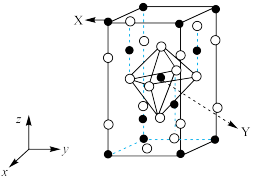
●表示_______ 原子(填元素符号),晶胞参数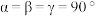 ,底面边长为
,底面边长为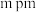 ,高为
,高为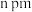 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,
, 的密度为
的密度为 ,则m的表达式为
,则m的表达式为_______ pm(列出计算式)。
(1)基态钛原子的电子排布式为
(2)Ti可形成多种配合物。
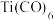 、
、 、
、 的配体所含原子中电负性由大到小的顺序是
的配体所含原子中电负性由大到小的顺序是 中
中
 。
。(3)
 是氧化法制取钛的中间产物。
是氧化法制取钛的中间产物。 的分子结构与
的分子结构与 相同,二者在常温下都是液体。
相同,二者在常温下都是液体。 分子的空间构型是
分子的空间构型是(4)如图为四方晶系的
 晶体结构:
晶体结构:
●表示
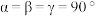 ,底面边长为
,底面边长为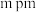 ,高为
,高为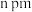 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,
, 的密度为
的密度为 ,则m的表达式为
,则m的表达式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】第四周期的元素镓(Ga)、锗(Ge).、砷(As)、硒(Se)都在高科技尖端科学特别是信息领域有着广泛的用途。试回答下列问题:
(1)基态锗原子的价电子排布式为______________________ 。
(2)沸点:NH3_______ AsH3(填“>”、“<”或“=”),原因是_____________________ 。
(3)某砷的氧化物俗称“砒霜”,其分子结构如图甲所示,该化合物的分子式为___________________ ,As原子采取_____________ 杂化。
(4)H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3酸性强的原因________________________________________ 。
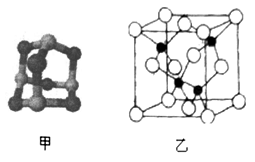
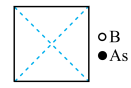
(5)砷化镓可由(CH3)2Ga和AsH3在700℃下反应制得,反应的方程式为__________________________ ;砷化镓的晶胞结构如图乙所示,其晶胞边长为apm,则每立方厘米该晶体中所含砷元素的质量为_____ g(用NA表示阿伏伽德罗常数的值)。
(1)基态锗原子的价电子排布式为
(2)沸点:NH3
(3)某砷的氧化物俗称“砒霜”,其分子结构如图甲所示,该化合物的分子式为
(4)H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3酸性强的原因

(5)砷化镓可由(CH3)2Ga和AsH3在700℃下反应制得,反应的方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】硫、锌及其化合物用途非常广泛。回答下列问题:
(1)基态锌原子核外能量不同的电子有___________ 种;锌的第二电离能I2(Zn)小于铜的第二电离能I2(Cu),其原因是___________ 。
(2)O和S处于同一主族。在H2O和H2S分子中,中心原子的杂化方式相同,但H2O分子中的键角∠HOH比H2S分子中的键角∠HSH大,其原因是___________ 。
(3)单质硫与热的NaOH浓溶液反应的产物之一为Na2S3。S 的空间构型为
的空间构型为___________ ,中心原子的杂化方式为___________ 。
(4)噻吩(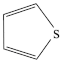 )广泛应用于合成医药、农药、染料工业。
)广泛应用于合成医药、农药、染料工业。
①噻吩分子中含有___________ 个σ键,分子中的大π键可用符号∏ 表示,其中m代表参与形成大键的原子数,n代表参与形成大键的电子数如苯分子中的大π键可表示为∏
表示,其中m代表参与形成大键的原子数,n代表参与形成大键的电子数如苯分子中的大π键可表示为∏ ,则噻吩分子中的大π键应表示为
,则噻吩分子中的大π键应表示为___________ 。
②噻吩的沸点为84℃,吡咯(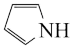 )的沸点在129~131℃之间,后者沸点较高,其原因是
)的沸点在129~131℃之间,后者沸点较高,其原因是___________ 。
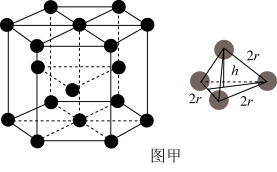
(5)晶体中Mg的原子堆积方式如图甲所示,这种堆积方式称为___________ 。已知镁原子半径为r,晶体中四个相邻的镁原子紧密堆积成正四面体,两层镁原子形成的正四面体高 ,晶胞的空间利用率为
,晶胞的空间利用率为___________ %(只写出化简式,不需计算结果)。
(1)基态锌原子核外能量不同的电子有
(2)O和S处于同一主族。在H2O和H2S分子中,中心原子的杂化方式相同,但H2O分子中的键角∠HOH比H2S分子中的键角∠HSH大,其原因是
(3)单质硫与热的NaOH浓溶液反应的产物之一为Na2S3。S
 的空间构型为
的空间构型为(4)噻吩(
 )广泛应用于合成医药、农药、染料工业。
)广泛应用于合成医药、农药、染料工业。①噻吩分子中含有
 表示,其中m代表参与形成大键的原子数,n代表参与形成大键的电子数如苯分子中的大π键可表示为∏
表示,其中m代表参与形成大键的原子数,n代表参与形成大键的电子数如苯分子中的大π键可表示为∏ ,则噻吩分子中的大π键应表示为
,则噻吩分子中的大π键应表示为②噻吩的沸点为84℃,吡咯(
 )的沸点在129~131℃之间,后者沸点较高,其原因是
)的沸点在129~131℃之间,后者沸点较高,其原因是(5)晶体中Mg的原子堆积方式如图甲所示,这种堆积方式称为
 ,晶胞的空间利用率为
,晶胞的空间利用率为
您最近一年使用:0次



