A、B、D、E、F五种元素的原子序数依次增大,且均为元素周期表前四周期元素,其中基态A原子的最外层电子数是最内层电子数的2倍;基态B原子的2p轨道上有3个未成对电子;基态D原子的s能级和p能级的电子总数相等;E和D可形成淡黄色固体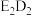 ;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:
;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:
(1)写出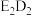 的电子式:
的电子式:___________ 。
(2)B的简单氢化物分子的空间结构是___________ ,其中心原子采取___________ 杂化。
(3)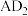 分子的
分子的 模型为
模型为___________ ,它的键角为___________ 。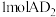 含有
含有 键的数目为
键的数目为___________ 。
(4)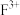 比
比 稳定,请用原子结构知识解释其原因:
稳定,请用原子结构知识解释其原因:___________ 。
(5)A、B、D简单氢化物稳定性由弱到强的顺序为___________ (用化学式表示),原因是___________ (从原子结构与键参数角度解释原因)。
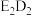 ;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:
;基态F原子的3d轨道的电子数是4s轨道电子数的3倍。回答下列问题:(1)写出
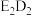 的电子式:
的电子式:(2)B的简单氢化物分子的空间结构是
(3)
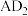 分子的
分子的 模型为
模型为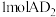 含有
含有 键的数目为
键的数目为(4)
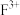 比
比 稳定,请用原子结构知识解释其原因:
稳定,请用原子结构知识解释其原因:(5)A、B、D简单氢化物稳定性由弱到强的顺序为
更新时间:2024-02-01 11:27:07
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:

其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;试写出:
(1)写出下列粒子的电子式:
①c__________ ;②d__________ ;③e__________ ;④a__________ 。
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:__________ >__________ (用化学式表示)。
(3)用电子式表示b元素与氧形成的化合物b2O的形成过程:________________ 。

其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;试写出:
(1)写出下列粒子的电子式:
①c
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:
(3)用电子式表示b元素与氧形成的化合物b2O的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如右图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。请回答下列问题:
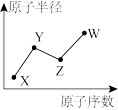
(1)写出四种元素的元素符号:X____ Y____ Z____ W____
(2)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确___ ,说明理由__________________________________ 。
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,其化学式为________ ;化合物乙是一种常见的强酸,会因保存不当而变成黄色液体,其原因是_______________________________ 。把红热的木炭投入黄色液体,剧烈反应,方程式为_____________________ ,将产生的气体通过澄清石灰水时气体变为无色,但未见有浑浊现象,原因是______________ 。(写出有关反应的化学方程式)

(1)写出四种元素的元素符号:X
(2)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,其化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有A、B、C、D、E、F、G、H八种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(A、C等为字母代号,请将字母代号用元素符号表示,下同)
(1)C2A4的结构式为_______ ,E2D2的电子式为_______ ,B、C、D原子第一电离能由大到小的顺序是_______ 。
(2)B元素的原子核外共有_______ 种不同运动状态的电子。F原子电子所占原子轨道数为_______ 个。
(3)用氢键表示式写出A2D存在的氢键_______ 。写出C元素基态原子的外围电子排布图为:_______ 。
(4)D、E、F三种元素的简单离子半径由大到小的顺序是_______ 。(用离子符号表示)
(5)H位于元素周期表中_______ 区(按电子排布分区),其基态H2+的价电子排布式为_______ ,实验室用一种溶液检验H3+时产生红色溶液,该反应的离子方程式为_______ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素是形成化合物种类最多的元素 |
| C元素基态原子的核外p电子数比s电子数少1 |
| D元素基态原子的核外p轨道中有两个未成对电子 |
| E是短周期中(除稀有气体外)原子半径最大的元素 |
| F元素的主族序数与周期数的差为4 |
| G元素是前四周期中电负性最小的元素 |
| H元素位于元素周期表中的第八列 |
(1)C2A4的结构式为
(2)B元素的原子核外共有
(3)用氢键表示式写出A2D存在的氢键
(4)D、E、F三种元素的简单离子半径由大到小的顺序是
(5)H位于元素周期表中
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】自然界中不存在氟的单质,得到单质氟的过程中,不少科学家为此献出了宝费的生命。1886年,法国化学家莫瓦桑发明了莫氏电炉,用电解法成功地制取了单质氟,因此荣获1906年诺贝尔化学奖,氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(1)氟磷灰石可用于制取磷肥,基态P原子有_______ 个未成对电子, 的中心P原子的杂化方式为
的中心P原子的杂化方式为_______ 。
(2)氟气可以用于制取情性强于N2的保护气SF6,也可以用于制取聚合反应的催化剂PF3,PF3可以作为工业制取硅单质的中间物质(SiF4)的原料。
①SiF4分子的空间结构为_______ 。
②S、P、Si的第一电离能由大到小的顺序为_______ 。
(3)氟气可以用于制取高化学稳定性材料聚四氟乙烯的原料四氟乙烯(C2F4),50g四氟乙烯含σ键的数目为_______ 。
(4)工业上电解Al2O3制取单质铝,常利用冰晶石Na3AlF6降低Al2O3的熔点。Na、Al、F的电负性由小到大的顺序为_______ ,工业上不用电解AlCl3制取铝的原因为_______ 。
(1)氟磷灰石可用于制取磷肥,基态P原子有
 的中心P原子的杂化方式为
的中心P原子的杂化方式为(2)氟气可以用于制取情性强于N2的保护气SF6,也可以用于制取聚合反应的催化剂PF3,PF3可以作为工业制取硅单质的中间物质(SiF4)的原料。
①SiF4分子的空间结构为
②S、P、Si的第一电离能由大到小的顺序为
(3)氟气可以用于制取高化学稳定性材料聚四氟乙烯的原料四氟乙烯(C2F4),50g四氟乙烯含σ键的数目为
(4)工业上电解Al2O3制取单质铝,常利用冰晶石Na3AlF6降低Al2O3的熔点。Na、Al、F的电负性由小到大的顺序为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】决定物质性质的重要因素是物质结构。请回答下列问题。
(1)CH 、·CH3、CH
、·CH3、CH 都是重要的有机反应中间体,有关它们的说法正确的是_____
都是重要的有机反应中间体,有关它们的说法正确的是_____
(2)在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
①HCl、CS2、H2S、SO2四种分子中μ=0的是____________________ ;
②实验测得:μPF3=1.03、μBCl3=0。由此可知,PF3分子是_____ 构型,BCl3分子是_____ 构型。
(3)对物质的磁性研究表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是__________________ 。
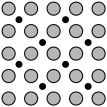
(4)利用光电子能谱证实:在洁净铁(可用于合成氨反应的催化剂)的表面上存在氮原子,右图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则在单层晶面上N/Fe原子数之比为________________ 。
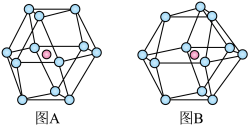
(5)金属晶体的结构可用等径圆球的密堆积来描述,在等径圆球的最密堆积的各种形式中,立方最密堆积和六方最密堆积最为重要,请指出下图中哪个为立方最密堆积______ (填“A”或“B”)
(1)CH
 、·CH3、CH
、·CH3、CH 都是重要的有机反应中间体,有关它们的说法正确的是_____
都是重要的有机反应中间体,有关它们的说法正确的是_____| A.它们均由甲烷去掉一个氢原子所得 |
| B.它们的空间构型相同,碳原子均可以采取sp2杂化 |
C.CH 与NH3、H3O+互为等电子体,几何构型均为三角锥形 与NH3、H3O+互为等电子体,几何构型均为三角锥形 |
D.CH 中的碳原子采取sp3杂化,所有原子均共面 中的碳原子采取sp3杂化,所有原子均共面 |
①HCl、CS2、H2S、SO2四种分子中μ=0的是
②实验测得:μPF3=1.03、μBCl3=0。由此可知,PF3分子是
(3)对物质的磁性研究表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是
(4)利用光电子能谱证实:在洁净铁(可用于合成氨反应的催化剂)的表面上存在氮原子,右图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则在单层晶面上N/Fe原子数之比为

(5)金属晶体的结构可用等径圆球的密堆积来描述,在等径圆球的最密堆积的各种形式中,立方最密堆积和六方最密堆积最为重要,请指出下图中哪个为立方最密堆积

您最近一年使用:0次
【推荐3】氮是重要的非金属元素,可以形成多种化合物。回答以下问题:
(1)基态氮原子的电子排布式是________________ 。C、N、O三种元素第一电离能从大到小的顺序是____________________ 。
(2)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是________________________ ;N2H4分子中氮原子轨道的杂化类型是____________________ 。
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(1)+2N2H4(1)===3N2(g)+4H2O(g) △H=-1038.7kJ·mol-1
若该反应中有4molN-H键断裂,则形成的π键有_________ mol。
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在__________ (填标号)
a.离子键 b.共价键 c.配位键 d.范德华力
(3)(CH3)3NH+和AlCl4-形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂___________ (填“大”或“小”),可用作____________ (填代号)。
a.助燃剂 b.“绿色”溶剂
c.复合材料 d.绝热材料
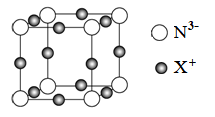
(4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是___________ ,与同一个N3-相连的X+有_________ 个。
(1)基态氮原子的电子排布式是
(2)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(1)+2N2H4(1)===3N2(g)+4H2O(g) △H=-1038.7kJ·mol-1
若该反应中有4molN-H键断裂,则形成的π键有
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在
a.离子键 b.共价键 c.配位键 d.范德华力
(3)(CH3)3NH+和AlCl4-形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂
a.助燃剂 b.“绿色”溶剂
c.复合材料 d.绝热材料
(4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】A、 B、 C、 D、 E、 F 为前四周期元素且原子序数依次增大,其中基态 A 原子的电子分布在 3 个能级,且每个能级所含的电子数相同; C 的原子核外最外层有 6 个运动状态不同的电子; D 是短周期元素中电负性最小的元素; E 的最高价氧化物的水化物酸性最强; 基态 F 原子核外最外层只有一个电子, 其余能层均充满电子。 G 元素与 D 元素同主族,且相差 3 个周期。
(1)元素 A、 B、 C 的第一电离能由小到大的是____________________ (用元素符号表示)。
(2)E的最高价含氧酸中 E 原子的杂化方式为_____________ 。 基态 E 原子中,核外电子占据最高能级的电子云轮廓形状为____________________________ 。
(3)F原子的外围电子排布式为_______________________ , F 单质晶体中原子的堆积方式是下图中的_______ (填写“甲”、 “乙”或“丙”) ,该晶体的空间利用率为_____________ 。(保留两位有效数字)

(4)已知元素 A、B形成的(AB)2分子中所有原子都满足 8电子稳定结构,则其分子中 σ键与 π键数目之比为__________ 。
(5)通常情况下, D 单质的熔沸点比 G 单质高,原因是_________________________ 。
(6)已知 DE 晶体的晶胞如下图所示:

若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示 A的一种晶体的晶胞(已知 A—A 键的键长为 a cm, NA表示阿伏伽德罗常数),则该晶胞中含有_________ 个 A 原子,该晶体的密度是______________ g·cm-3(列式表示) 。
(1)元素 A、 B、 C 的第一电离能由小到大的是
(2)E的最高价含氧酸中 E 原子的杂化方式为
(3)F原子的外围电子排布式为

(4)已知元素 A、B形成的(AB)2分子中所有原子都满足 8电子稳定结构,则其分子中 σ键与 π键数目之比为
(5)通常情况下, D 单质的熔沸点比 G 单质高,原因是
(6)已知 DE 晶体的晶胞如下图所示:

若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示 A的一种晶体的晶胞(已知 A—A 键的键长为 a cm, NA表示阿伏伽德罗常数),则该晶胞中含有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铜的相关化合物在生产生活中具有重要的作用。回答下列问题:
(1)铜元素在周期表中的位置是______ ,基态铜原子中,核外电子占据最高能层的符号是______ ,占据该最高能层的电子数为__________ 。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于__________ (填“晶体”或“非晶体”)。
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为_____________ 。硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是异硫氰酸(H-N=C=S)。理论上前者沸点低于后者,其原因是____________________________ 。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为________ 。
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为____  用含a、NA的代数式表示)g•cm-3。
用含a、NA的代数式表示)g•cm-3。
(1)铜元素在周期表中的位置是
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为
 用含a、NA的代数式表示)g•cm-3。
用含a、NA的代数式表示)g•cm-3。 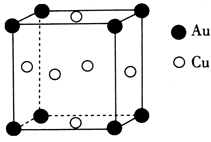
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
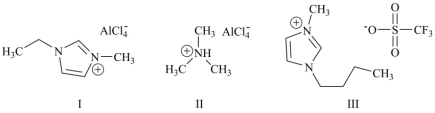
【推荐3】铝离子电池能量密度高、成本低且安全性高,是有前景的下一代储能电池。铝离子电池一般采用离子液体作为电解质,几种离子液体的结构如下。
(1)基态铝原子的核外电子排布式为___________ 。
(2)基态氮原子的价层电子排布图为___________(填编号)。
(3)化合物Ⅰ中碳原子的杂化轨道类型为___________ 。
(4)化合物Ⅲ中O、F、S电负性由大到小的顺序为___________ 。
(5)铝离子电池的其中一种正极材料为AlMn2O4,其晶胞中铝原子的骨架如图所示。___________ 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,如图中原子1的坐标为(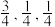 ),原子2的坐标为(
),原子2的坐标为( ),则原子3的坐标为
),则原子3的坐标为___________ 。
③已知该晶体属于立方晶系,晶胞参数为apm,阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为___________ g·cm-3(列出计算式)。
(1)基态铝原子的核外电子排布式为
(2)基态氮原子的价层电子排布图为___________(填编号)。
A.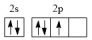 | B.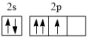 | C.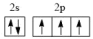 | D.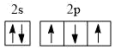 |
(4)化合物Ⅲ中O、F、S电负性由大到小的顺序为
(5)铝离子电池的其中一种正极材料为AlMn2O4,其晶胞中铝原子的骨架如图所示。
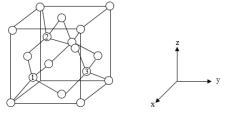
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,如图中原子1的坐标为(
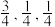 ),原子2的坐标为(
),原子2的坐标为(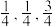 ),则原子3的坐标为
),则原子3的坐标为③已知该晶体属于立方晶系,晶胞参数为apm,阿伏加德罗常数的值为
 ,则晶体的密度为
,则晶体的密度为
您最近一年使用:0次



