自然界中不存在氟的单质,得到单质氟的过程中,不少科学家为此献出了宝费的生命。1886年,法国化学家莫瓦桑发明了莫氏电炉,用电解法成功地制取了单质氟,因此荣获1906年诺贝尔化学奖,氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(1)氟磷灰石可用于制取磷肥,基态P原子有_______ 个未成对电子, 的中心P原子的杂化方式为
的中心P原子的杂化方式为_______ 。
(2)氟气可以用于制取情性强于N2的保护气SF6,也可以用于制取聚合反应的催化剂PF3,PF3可以作为工业制取硅单质的中间物质(SiF4)的原料。
①SiF4分子的空间结构为_______ 。
②S、P、Si的第一电离能由大到小的顺序为_______ 。
(3)氟气可以用于制取高化学稳定性材料聚四氟乙烯的原料四氟乙烯(C2F4),50g四氟乙烯含σ键的数目为_______ 。
(4)工业上电解Al2O3制取单质铝,常利用冰晶石Na3AlF6降低Al2O3的熔点。Na、Al、F的电负性由小到大的顺序为_______ ,工业上不用电解AlCl3制取铝的原因为_______ 。
(1)氟磷灰石可用于制取磷肥,基态P原子有
 的中心P原子的杂化方式为
的中心P原子的杂化方式为(2)氟气可以用于制取情性强于N2的保护气SF6,也可以用于制取聚合反应的催化剂PF3,PF3可以作为工业制取硅单质的中间物质(SiF4)的原料。
①SiF4分子的空间结构为
②S、P、Si的第一电离能由大到小的顺序为
(3)氟气可以用于制取高化学稳定性材料聚四氟乙烯的原料四氟乙烯(C2F4),50g四氟乙烯含σ键的数目为
(4)工业上电解Al2O3制取单质铝,常利用冰晶石Na3AlF6降低Al2O3的熔点。Na、Al、F的电负性由小到大的顺序为
更新时间:2024-01-11 14:27:38
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】完成下列问题。
(1) 是一种强氧化剂,在酸性条件下与乙醇发生反应:
是一种强氧化剂,在酸性条件下与乙醇发生反应: 。
。
①Cr基态核外电子排布式为_______ 。
②K、S、O三种元素的第一电离能由大到小的顺序为_______ 。
③乙醇的沸点比二甲醚 的高,主要原因是
的高,主要原因是_______ 。
④某铬铝合金是一种高温材料,其晶胞结构如图所示,该晶体中
_______ 。

(2)Cu3Au的晶胞如图所示,Cu3Au晶体中每个铜原子周围距离最近的铜原子数目为_______ 。

(1)
 是一种强氧化剂,在酸性条件下与乙醇发生反应:
是一种强氧化剂,在酸性条件下与乙醇发生反应: 。
。①Cr基态核外电子排布式为
②K、S、O三种元素的第一电离能由大到小的顺序为
③乙醇的沸点比二甲醚
 的高,主要原因是
的高,主要原因是④某铬铝合金是一种高温材料,其晶胞结构如图所示,该晶体中


(2)Cu3Au的晶胞如图所示,Cu3Au晶体中每个铜原子周围距离最近的铜原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】CuO在化学链(如气相烃类)燃烧和催化CO氧化过程中均展现出良好的性能,同时具有成本低廉的优势,有望成为贵金属催化剂的替代品。中国科学院工程热物理研究所的科研人员初步揭示了CO在CuO表面的催化机理,并深入研究了CO在铜基氧化物表面的反应机制,并提出了对应的反应动力学模型。
(1)基态铜原子的价电子排布式为_______ ,其核外电子的空间运动状态有_______ 种。
(2)N与C、O同周期,H、C、N三种元素的电负性从小到大的顺序为_______ ;C、N、O 的第一电离能从大到小的顺序为_______ 。
(3)NH3具有还原性,能被CuO氧化,NH3分子中N原子的杂化方式为_______ ,NH3的沸点高于PH3的原因是_______ 。
(4)已知Cu2O的熔点高于Cu2S的熔点,其原因是_______ 。
(5)铜的某种氧化物的晶胞结构如图所示,若该晶胞中Cu原子与O原子之间的最近距离为apm,设阿伏加德罗常数的值为NA,则该晶胞的密度为_______ g· cm-3(填含a、NA的代数式)。
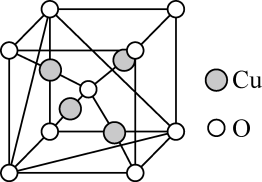
(1)基态铜原子的价电子排布式为
(2)N与C、O同周期,H、C、N三种元素的电负性从小到大的顺序为
(3)NH3具有还原性,能被CuO氧化,NH3分子中N原子的杂化方式为
(4)已知Cu2O的熔点高于Cu2S的熔点,其原因是
(5)铜的某种氧化物的晶胞结构如图所示,若该晶胞中Cu原子与O原子之间的最近距离为apm,设阿伏加德罗常数的值为NA,则该晶胞的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是__________ ,Na、Mg、Al第一电离能I1从小到大的排列顺序是____________ 。
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示。

①实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是_________________ 。
②SO42-中S原子的杂化类型是_____ ,与其互为等电子体的分子有________ (任写一种)。
③Cu2+还能与NH3、Cl-等形成配位数为4的配合物,[Cu(NH3)4]2+中存在的化学键类型有__ (填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
④写出基态Cu原子的外围电子排布式________ ;金属铜采用面心立方堆积方式,已知Cu原子的半径为r pm,相对原子质量为M,NA表示阿伏加德罗常数,则金属铜的密度是_____ g/cm3(列出计算式)。
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ•mol-1) | 786 | 715 | 3401 |
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示。

①实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是
②SO42-中S原子的杂化类型是
③Cu2+还能与NH3、Cl-等形成配位数为4的配合物,[Cu(NH3)4]2+中存在的化学键类型有
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
④写出基态Cu原子的外围电子排布式
您最近一年使用:0次
【推荐1】X、Y、Z、W、Q、R均为前4周期元素,且原子序数依次增大。其相关信息如下表所示:
请回答下列问题:
(1)Y元素的基态原子的电子排布式为________________ ;R元素的价电子排布式为___________ 。
(2)元素X、Y、Z电负性由大到小的顺序为_________ (填元素符号);X、Y、Z中第一电离能最大的是__________ (填元素名称)。
(3)W在周期表中的位置是__________ ;X的最简单氢化物分子中键角为__________ ;化合物Q2Z2中所含化学键类型为_____________ 。
(4)YZ2与水反应的离子方程式为___________________ 。
| X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
| Y原子的2p轨道中有3个未成对电子 |
| Z元素的族序数是其周期数的3倍 |
| W原子的第一至第六电离能分别为:I1=578kJ/mol;I2=1817kJ/mol;I3=2745kJ/mol;I4=11575kJ/mol;I5=14830kJ/mol;I6=18376kJ/mol |
| Q为前4周期中电负性最小的元素 |
| 元素R位于周期表的第11列 |
(1)Y元素的基态原子的电子排布式为
(2)元素X、Y、Z电负性由大到小的顺序为
(3)W在周期表中的位置是
(4)YZ2与水反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】1932年美国化学家鲍林首先提出了电负性(用x表示)的概念。表中是某些短周期元素的x值:
(1)表格元素中,第一电离能最小的元素的基态原子电子排布式为____ 。
(2)通过分析x值变化规律,确定N元素x值范围:____<x(N)<____。____
(3)第一电离能大小:Mg____ Al(填“大于”“小于”)。
(4)S元素和Cl元素基态原子核外未成对电子数之比为____ 。
(5)某有机化合物结构中含S-N键,其共用电子对偏向____ (写原子名称)。
(6)经验规律告诉我们:当成键的两原子相应元素的x差值△x>1.7时,一般为离子键,当△x<1.7时,一般为共价键。试推断AlBr3中化学键类型是____ 。
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| x值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(2)通过分析x值变化规律,确定N元素x值范围:____<x(N)<____。
(3)第一电离能大小:Mg
(4)S元素和Cl元素基态原子核外未成对电子数之比为
(5)某有机化合物结构中含S-N键,其共用电子对偏向
(6)经验规律告诉我们:当成键的两原子相应元素的x差值△x>1.7时,一般为离子键,当△x<1.7时,一般为共价键。试推断AlBr3中化学键类型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】硼和过渡金属在新能源和新材料的研究、合成和利用中有着重要地位和作用。回答下列问题:
(1)图中状态的硼中,能量最低的是_______ (填选项字母)。

(2)BF3属于_______ (填“极性分子”或“非极性分子”),理由为_______ 。
(3)氮化硼和碳化硼均属于原子晶体,氮化硼的熔点高于碳化硼的原因为_______ ;B、C、N的第一电离能由大到小的顺序为_______ 。
(4)NaBH4是一种重要的还原剂和储氢材料,其阴离子的立体构型为_______ ,B原子的杂化方式为_______ ;1 mol 阴离子中含有配位键的数目为_______ ;Na、B、H的电负性由大到小的顺序为_______ 。
(5)过渡金属Q与镧(La)形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为nd2n+2(n+1)sn-4;该合金的晶胞结构和x轴方向的投影图如图所示。

①Q的元素符号为_______ 。
②若阿伏加德罗常数的值为NA,Q的相对原子质量为M,则该合金的密度ρ=_______ g·cm-3(用含a、c、NA、M的代数式表示)。
(1)图中状态的硼中,能量最低的是

(2)BF3属于
(3)氮化硼和碳化硼均属于原子晶体,氮化硼的熔点高于碳化硼的原因为
(4)NaBH4是一种重要的还原剂和储氢材料,其阴离子的立体构型为
(5)过渡金属Q与镧(La)形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为nd2n+2(n+1)sn-4;该合金的晶胞结构和x轴方向的投影图如图所示。

①Q的元素符号为
②若阿伏加德罗常数的值为NA,Q的相对原子质量为M,则该合金的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】工业中可利用生产钛白的副产物 和硫铁矿
和硫铁矿 联合制备铁精粉(
联合制备铁精粉( )和硫酸,实现能源及资源的有效利用。
)和硫酸,实现能源及资源的有效利用。
(1) 结构示意图如图。
结构示意图如图。

①铁元素常见的化合价有+2和+3价, 比
比 稳定的因:
稳定的因:________ 。
②下列粒子的中心原子杂化方式与 中S的杂化方式相同的是:
中S的杂化方式相同的是:
A.HCN B. C.
C. D.
D.
③ 中Fe(Ⅱ)的配位数是
中Fe(Ⅱ)的配位数是_______ , 与
与 的作用力类型是
的作用力类型是_________ 。
(2) 晶体的晶胞形状为立方体,结构如图。
晶体的晶胞形状为立方体,结构如图。
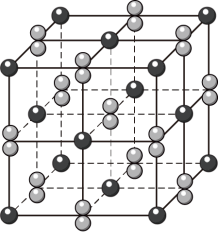
①距离 最近的阳离子有
最近的阳离子有___________ 个, 位于
位于 所形成的
所形成的___________ (填“正四面体”或“正八面体”)空隙。
② 晶体的晶胞参数为a nm,密度为
晶体的晶胞参数为a nm,密度为 ,
, 的摩尔质量为M
的摩尔质量为M  ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
___________ (用含a、ρ、M的代数式表示)。
(3) 加热脱水后生成
加热脱水后生成 ,再与
,再与 在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收
在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收 制得发烟硫酸(化学组成可表示为
制得发烟硫酸(化学组成可表示为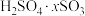 ),可生产
),可生产 质量分数为40%的发烟硫酸
质量分数为40%的发烟硫酸___________ 吨。
 和硫铁矿
和硫铁矿 联合制备铁精粉(
联合制备铁精粉( )和硫酸,实现能源及资源的有效利用。
)和硫酸,实现能源及资源的有效利用。(1)
 结构示意图如图。
结构示意图如图。
①铁元素常见的化合价有+2和+3价,
 比
比 稳定的因:
稳定的因:②下列粒子的中心原子杂化方式与
 中S的杂化方式相同的是:
中S的杂化方式相同的是:A.HCN B.
 C.
C. D.
D.
③
 中Fe(Ⅱ)的配位数是
中Fe(Ⅱ)的配位数是 与
与 的作用力类型是
的作用力类型是(2)
 晶体的晶胞形状为立方体,结构如图。
晶体的晶胞形状为立方体,结构如图。
①距离
 最近的阳离子有
最近的阳离子有 位于
位于 所形成的
所形成的②
 晶体的晶胞参数为a nm,密度为
晶体的晶胞参数为a nm,密度为 ,
, 的摩尔质量为M
的摩尔质量为M  ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
(3)
 加热脱水后生成
加热脱水后生成 ,再与
,再与 在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收
在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收 制得发烟硫酸(化学组成可表示为
制得发烟硫酸(化学组成可表示为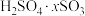 ),可生产
),可生产 质量分数为40%的发烟硫酸
质量分数为40%的发烟硫酸
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的DF-31A洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了Fe、Cr、Ni、Cu、C等多种元素。回答下列问题:
(1)基态铁原子的价电子排布式为___________ 。
(2)与Cr同周期且基态原子最外层电子数相同的元素有___________ (填元素符号),其位于周期表中的___________ 区。
(3)实验室常用KSCN溶液、苯酚( )检验Fe3+,苯酚中碳原子的杂化轨道类型为
)检验Fe3+,苯酚中碳原子的杂化轨道类型为___________ ,苯酚中所有原子可能共面吗?___________ (填“能”或“不能”)。
(4)铁元素能与CO形成羰基铁[Fe(CO)5],羰基铁[Fe(CO)5]可作催化剂、汽油抗爆剂等。1molFe(CO)5分子中含___________ molσ键,配体CO中σ键与π键数目之比为___________ 。
(5)+3价铬的一种配离子为[Cr(H2O)6]3+,则配体中中心原子的杂化方式为___________ ,杂化轨道的空间构型为___________ ,该配离子中不存在下列哪种作用力___________ 。
A.共价键 B.离子键 C.配位键 D.σ键 E.π键
(6)已知铜的第一、第二电离能分别为745.5kJ/mol、1957.9kJ/mol,则铜的第二电离能远大于第一电离能的理由是___________ 。
(7)在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色的溶液。写出蓝色沉淀溶解的离子方程式___________ 。
(1)基态铁原子的价电子排布式为
(2)与Cr同周期且基态原子最外层电子数相同的元素有
(3)实验室常用KSCN溶液、苯酚(
 )检验Fe3+,苯酚中碳原子的杂化轨道类型为
)检验Fe3+,苯酚中碳原子的杂化轨道类型为(4)铁元素能与CO形成羰基铁[Fe(CO)5],羰基铁[Fe(CO)5]可作催化剂、汽油抗爆剂等。1molFe(CO)5分子中含
(5)+3价铬的一种配离子为[Cr(H2O)6]3+,则配体中中心原子的杂化方式为
A.共价键 B.离子键 C.配位键 D.σ键 E.π键
(6)已知铜的第一、第二电离能分别为745.5kJ/mol、1957.9kJ/mol,则铜的第二电离能远大于第一电离能的理由是
(7)在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色的溶液。写出蓝色沉淀溶解的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】Ⅰ.回答下列问题:
(1)利用价层电子对互斥模型推测分子或离子的空间结构。
 ;
;___________ ; (共价分子):
(共价分子):___________ 。
(2)有两种活性反应中间体,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给出的这两种粒子的结构,写出相应的化学式。
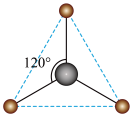
___________ ;
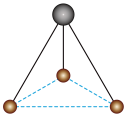
___________ 。
(3)按要求写出由第二周期非金属元素的原子构成的中性分子的化学式。
平面三角形分子:_______ ,三角锥形分子:________ ,正四面体形分子________ 。
Ⅱ.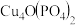 是锂—磷酸氧铜电池正极的活性物质,它可通过下列反应制备:
是锂—磷酸氧铜电池正极的活性物质,它可通过下列反应制备: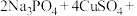
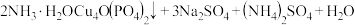 。
。
(4)写出基态 的电子排布式:
的电子排布式:___________ 。
(5) 的空间结构是
的空间结构是___________ 。
(6)P、S、N元素第一电离能由大到小的顺序为___________ 。
(7)氨基乙酸铜分子结构如下,其中碳原子的杂化方式为___________ ,基态碳原子核外电子有___________ 种运动状态。

(1)利用价层电子对互斥模型推测分子或离子的空间结构。
 ;
; (共价分子):
(共价分子):(2)有两种活性反应中间体,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给出的这两种粒子的结构,写出相应的化学式。


(3)按要求写出由第二周期非金属元素的原子构成的中性分子的化学式。
平面三角形分子:
Ⅱ.
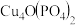 是锂—磷酸氧铜电池正极的活性物质,它可通过下列反应制备:
是锂—磷酸氧铜电池正极的活性物质,它可通过下列反应制备: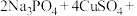
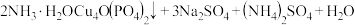 。
。(4)写出基态
 的电子排布式:
的电子排布式:(5)
 的空间结构是
的空间结构是(6)P、S、N元素第一电离能由大到小的顺序为
(7)氨基乙酸铜分子结构如下,其中碳原子的杂化方式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】金属锂有“白色石油”之称,是新时代重要的资源,“盐湖提锂”越来越受到重视。
(1) 与
与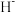 具有相同的电子构型,
具有相同的电子构型,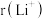 小于
小于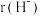 ,原因是
,原因是_______ 。 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 离子的空间结构是
离子的空间结构是_______ ,其中心原子的杂化轨道类型为_______ 。

(2) 晶胞如图所示,已知晶胞参数为
晶胞如图所示,已知晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为_______  (列出计算式)。
(列出计算式)。
(3)某兴趣小组取盐湖水进行浓缩和初步除杂后,得到浓缩卤水(含有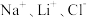 和少量
和少量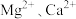 ),并设计了以下列过程通过制备碳酸锂来提取锂。
),并设计了以下列过程通过制备碳酸锂来提取锂。

 时相关物质的参数如下:①
时相关物质的参数如下:① 的溶解度:
的溶解度:
②:

回答下列问题:
①“沉淀1”为_______ 。
②向“滤液1”中加入适量固体 发生反应:
发生反应: 。通过计算解释
。通过计算解释 可用于转化的原因:
可用于转化的原因:_______ 。
③为提高 ,的析出量和纯度,“操作A”依次为
,的析出量和纯度,“操作A”依次为_______ 、_______ 、洗涤。
④有同学建议用“侯氏制碱法”的原理制备 。查阅资料后,发现文献对常温下的
。查阅资料后,发现文献对常温下的 有不同的描述:i.是白色固体:ii.尚未从溶液中分离出来。为探究
有不同的描述:i.是白色固体:ii.尚未从溶液中分离出来。为探究 的性质,将饱和
的性质,将饱和 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
_______ (填“稳定”或“不稳定”),有关反应的离子方程式为_______ 。
(1)
 与
与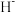 具有相同的电子构型,
具有相同的电子构型,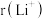 小于
小于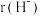 ,原因是
,原因是 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 离子的空间结构是
离子的空间结构是
(2)
 晶胞如图所示,已知晶胞参数为
晶胞如图所示,已知晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式)。
(列出计算式)。(3)某兴趣小组取盐湖水进行浓缩和初步除杂后,得到浓缩卤水(含有
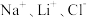 和少量
和少量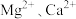 ),并设计了以下列过程通过制备碳酸锂来提取锂。
),并设计了以下列过程通过制备碳酸锂来提取锂。
 时相关物质的参数如下:①
时相关物质的参数如下:① 的溶解度:
的溶解度:
②:

| 化合物 |  |
 | 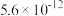 |
 |  |
 |  |
 |  |
①“沉淀1”为
②向“滤液1”中加入适量固体
 发生反应:
发生反应: 。通过计算解释
。通过计算解释 可用于转化的原因:
可用于转化的原因:③为提高
 ,的析出量和纯度,“操作A”依次为
,的析出量和纯度,“操作A”依次为④有同学建议用“侯氏制碱法”的原理制备
 。查阅资料后,发现文献对常温下的
。查阅资料后,发现文献对常温下的 有不同的描述:i.是白色固体:ii.尚未从溶液中分离出来。为探究
有不同的描述:i.是白色固体:ii.尚未从溶液中分离出来。为探究 的性质,将饱和
的性质,将饱和 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铬云母是一些玉石、彩石的重要组成和着色矿物。理想的组分是含Al的八面体片,化学式为KAl2[Si3AlO10](OH,F)2,其中的Al也可少量地被Fe、Mg、Mn、Cr、V等替换。
(1)基态Cr原子的核外电子排布式为__ 。
(2)基态锰原子核外电子排布中能量最高的能级符号为___ 。
(3)O、F、Si三种元素的第一电离能由大到小的顺序为___ 。
(4)O、F、Si与H形成的氢化物有H2O2、H2O、HF、SiH4、Si2H6等。
①SiH4中Si原子的杂化方式为__ 。
②H2O、HF、SiH4三种物质中沸点最高的是__ 。
③等物质的量的H2O2与Si2H6所含σ键数目之比为__ 。
(1)基态Cr原子的核外电子排布式为
(2)基态锰原子核外电子排布中能量最高的能级符号为
(3)O、F、Si三种元素的第一电离能由大到小的顺序为
(4)O、F、Si与H形成的氢化物有H2O2、H2O、HF、SiH4、Si2H6等。
①SiH4中Si原子的杂化方式为
②H2O、HF、SiH4三种物质中沸点最高的是
③等物质的量的H2O2与Si2H6所含σ键数目之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】镍是一种用途广泛的金属,常用于电镀工业和制造电池。镍易形成Ni(CO)4、[Ni(NH3)6]SO4等配合物。
(1)Ni2+的核外电子排布式为___________ 。
(2)Ni2+可用丁二酮肟检验。丁二酮肟的结构如图所示,其分子中碳原子轨道的杂化类型为___________ 。

(3)1mol [Ni(NH3)6]SO4中σ键的数目为___________ NA。氨的沸点高于膦(PH3),原因是___________ 。
(4)镧镍合金是较好的储氢材料。储氢后所得晶体的化学式为LaNi5H6,晶胞结构如图所示,X、Y、Z表示储氢后的三种微粒,则图中Z表示的微粒为___________ (填化学式)。

(1)Ni2+的核外电子排布式为
(2)Ni2+可用丁二酮肟检验。丁二酮肟的结构如图所示,其分子中碳原子轨道的杂化类型为

(3)1mol [Ni(NH3)6]SO4中σ键的数目为
(4)镧镍合金是较好的储氢材料。储氢后所得晶体的化学式为LaNi5H6,晶胞结构如图所示,X、Y、Z表示储氢后的三种微粒,则图中Z表示的微粒为

您最近一年使用:0次



