利用某金属废屑(含Cu、Al、Fe及其少量氧化物)制备胆矾的工艺流程如图所示.
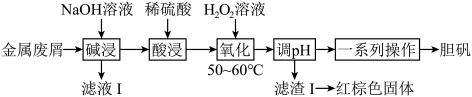
回答下列问题:
(1)“碱浸”工序Al发生反应的离子方程式为____________ .
(2)相关离子在溶液中的去除率随pH的变化如图所示.
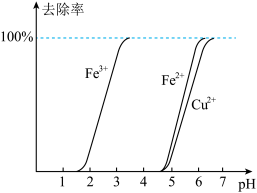
①“氧化”工序中 的作用是
的作用是__________ 、______________ (用离子方程式表示);“氧化”工序采取的加热方式为____________ ,温度不宜过高的原因是___________ .
②“调pH”时,应控制溶液pH的适宜范围为__________ (填标号).
A.2.0~3.0 B.3.0~4.0 C.4.0~5.0
(3)红棕色固体的用途有___________ (任写一种).“一系列操作”中包含__________ 、__________ 、过滤、洗涤、干燥.

回答下列问题:
(1)“碱浸”工序Al发生反应的离子方程式为
(2)相关离子在溶液中的去除率随pH的变化如图所示.

①“氧化”工序中
 的作用是
的作用是②“调pH”时,应控制溶液pH的适宜范围为
A.2.0~3.0 B.3.0~4.0 C.4.0~5.0
(3)红棕色固体的用途有
更新时间:2024-02-05 15:37:36
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某工厂废金属屑的主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的金属废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
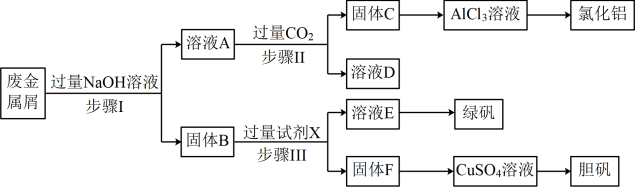
完成下列填空:
(1)写出步骤Ⅰ反应的离子方程式:___ 。
(2)试剂X是___ ,溶液D是___ 。
(3)在步骤Ⅱ中,用如图装置制取CO2并通入溶液A中。一段时间后,仍观察不到烧杯中产生白色沉淀。为了固体C的生成,在药品和装置上可采取的改进措施是___ 。

(4)溶液E中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因:___ 。
(5)将固体F继续加入热的稀硫酸,同时不断鼓入空气,固体溶解得CuSO4溶液,写出反应的化学方程式:___ 。

完成下列填空:
(1)写出步骤Ⅰ反应的离子方程式:
(2)试剂X是
(3)在步骤Ⅱ中,用如图装置制取CO2并通入溶液A中。一段时间后,仍观察不到烧杯中产生白色沉淀。为了固体C的生成,在药品和装置上可采取的改进措施是

(4)溶液E中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因:
(5)将固体F继续加入热的稀硫酸,同时不断鼓入空气,固体溶解得CuSO4溶液,写出反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】七水合硫酸亚铁( )是一种重要的食品或饲料添加剂,颜料及电子工业的原材料。某同学设计了利用工业烧渣并采用如图流程来制备七水合硫酸亚铁:
)是一种重要的食品或饲料添加剂,颜料及电子工业的原材料。某同学设计了利用工业烧渣并采用如图流程来制备七水合硫酸亚铁:
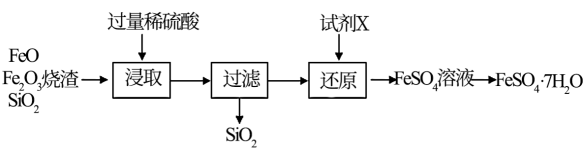
回答下列问题:
(1)工业烧渣与稀硫酸反应的离子反应有: ,
,_______ 。
(2)加入的试剂X是:_______ ,写出发生的反应离子方程式_______ 。
A. B.
B.  C.
C.  D.
D. 
(3)若需检验还原后的 溶液中是否存在有
溶液中是否存在有 ,可选择的方法是取2~3mL试液,在其中滴加
,可选择的方法是取2~3mL试液,在其中滴加_______ 溶液(填名称),当_______ 时(填实验现象),说明溶液中存在 。
。
(4)从 溶液中得到产品
溶液中得到产品 ,应进行的操作依次是
,应进行的操作依次是_______ 、过滤、洗涤、干燥。
(5)利用工业烧渣还可以制得一种重要的净水剂 ,其基本原理是先由烧渣制得氢氧化铁,再将氢氧化铁与
,其基本原理是先由烧渣制得氢氧化铁,再将氢氧化铁与 、烧碱在40℃反应,即可制备
、烧碱在40℃反应,即可制备 ,其中
,其中 被还原成
被还原成 ,此方法称为“湿法”。请写出湿法制备
,此方法称为“湿法”。请写出湿法制备 的化学方程式
的化学方程式_______ 。
 )是一种重要的食品或饲料添加剂,颜料及电子工业的原材料。某同学设计了利用工业烧渣并采用如图流程来制备七水合硫酸亚铁:
)是一种重要的食品或饲料添加剂,颜料及电子工业的原材料。某同学设计了利用工业烧渣并采用如图流程来制备七水合硫酸亚铁:
回答下列问题:
(1)工业烧渣与稀硫酸反应的离子反应有:
 ,
,(2)加入的试剂X是:
A.
 B.
B.  C.
C.  D.
D. 
(3)若需检验还原后的
 溶液中是否存在有
溶液中是否存在有 ,可选择的方法是取2~3mL试液,在其中滴加
,可选择的方法是取2~3mL试液,在其中滴加 。
。(4)从
 溶液中得到产品
溶液中得到产品 ,应进行的操作依次是
,应进行的操作依次是(5)利用工业烧渣还可以制得一种重要的净水剂
 ,其基本原理是先由烧渣制得氢氧化铁,再将氢氧化铁与
,其基本原理是先由烧渣制得氢氧化铁,再将氢氧化铁与 、烧碱在40℃反应,即可制备
、烧碱在40℃反应,即可制备 ,其中
,其中 被还原成
被还原成 ,此方法称为“湿法”。请写出湿法制备
,此方法称为“湿法”。请写出湿法制备 的化学方程式
的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】 和
和 都是光电转化的重要材料。某探究小组利用钛铁矿(主要成分为钛酸亚铁
都是光电转化的重要材料。某探究小组利用钛铁矿(主要成分为钛酸亚铁 ,还含有少量
,还含有少量 等杂质)来制备
等杂质)来制备 和
和 ,并利用黄钾铁矾
,并利用黄钾铁矾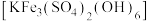 回收铁的工艺流程如下图所示:
回收铁的工艺流程如下图所示:
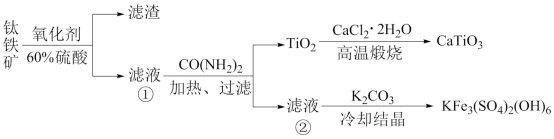
已知:a.“氧化酸解”后滤液①中钛元素以 形式存在于溶液中;
形式存在于溶液中;
b.黄钾铁矾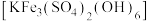 可存在于碱性溶液中。
可存在于碱性溶液中。
回答下列问题:
(1) 中钛元素的化合价为
中钛元素的化合价为___________ ;盛放 溶液的试剂瓶不能用玻璃塞的原因是
溶液的试剂瓶不能用玻璃塞的原因是___________ (用化学方程式表示)。
(2)“氧化酸解”时,控制反应温度为150℃,不同氧化剂对钛铁矿酸解率的影响如下图所示。50min时,要求酸解率大于85%,则所选氧化剂应为___________ ;采用 作氧化剂时,其效率低的原因可能是
作氧化剂时,其效率低的原因可能是___________ 。
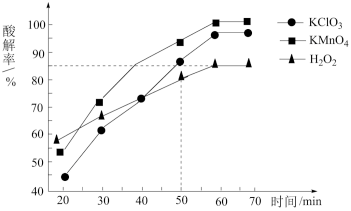
不同氧化剂对钛铁矿酸解率的影响
(3)根据工艺流程图,写出生成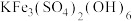 的离子方程式:
的离子方程式:___________ 。
(4)写出“高温煅烧”中由 制备
制备 的化学方程式:
的化学方程式:___________ 。
(5) ℃时,
℃时, 恰好沉淀完全【此时溶液中
恰好沉淀完全【此时溶液中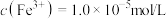 】,已知
】,已知 ℃时,
℃时, 的
的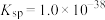 ,水的离子积
,水的离子积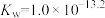 。请通过计算求此时溶液的
。请通过计算求此时溶液的 (写出计算过程)
(写出计算过程)___________ 。
 和
和 都是光电转化的重要材料。某探究小组利用钛铁矿(主要成分为钛酸亚铁
都是光电转化的重要材料。某探究小组利用钛铁矿(主要成分为钛酸亚铁 ,还含有少量
,还含有少量 等杂质)来制备
等杂质)来制备 和
和 ,并利用黄钾铁矾
,并利用黄钾铁矾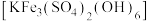 回收铁的工艺流程如下图所示:
回收铁的工艺流程如下图所示:
已知:a.“氧化酸解”后滤液①中钛元素以
 形式存在于溶液中;
形式存在于溶液中;b.黄钾铁矾
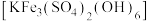 可存在于碱性溶液中。
可存在于碱性溶液中。回答下列问题:
(1)
 中钛元素的化合价为
中钛元素的化合价为 溶液的试剂瓶不能用玻璃塞的原因是
溶液的试剂瓶不能用玻璃塞的原因是(2)“氧化酸解”时,控制反应温度为150℃,不同氧化剂对钛铁矿酸解率的影响如下图所示。50min时,要求酸解率大于85%,则所选氧化剂应为
 作氧化剂时,其效率低的原因可能是
作氧化剂时,其效率低的原因可能是
不同氧化剂对钛铁矿酸解率的影响
(3)根据工艺流程图,写出生成
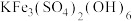 的离子方程式:
的离子方程式:(4)写出“高温煅烧”中由
 制备
制备 的化学方程式:
的化学方程式:(5)
 ℃时,
℃时, 恰好沉淀完全【此时溶液中
恰好沉淀完全【此时溶液中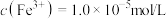 】,已知
】,已知 ℃时,
℃时, 的
的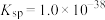 ,水的离子积
,水的离子积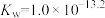 。请通过计算求此时溶液的
。请通过计算求此时溶液的 (写出计算过程)
(写出计算过程)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】镍、钴及其化合物在工业上有广泛的应用。以含镍废料(主要成分为NiO,含少量FeO、Fe2O3、CoO、BaO和SiO2)为原料制备NixOy,和碳酸钴(CoCO3)的工艺流程如图。
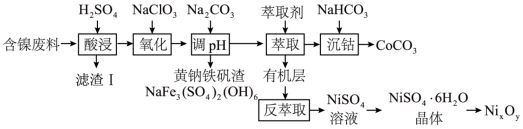
已知:Ksp[Co(OH)2]=2×10-15,请回答以下问题:
(1)“滤渣I”主要成分是___________ 。
(2)“氧化”时反应的离子方程式是___________ ,为证明添加NaClO3已足量,可用___________ (写化学式)溶液进行检验。
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为___________ 。
(4)“萃取”和“反萃取”可简单表示为:2HX+Ni2+ NiX2+2H+。在萃取过程中加入适量氨水,其作用是
NiX2+2H+。在萃取过程中加入适量氨水,其作用是___________ 。“反萃取”需要往有机层中加___________ (填试剂)。
(5)若起始时c(Co2+)=0.02mol∙L-1,“沉钴”过程中应控制pH___________ (填范围)。
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
由NiSO4溶液获得稳定的NiSO4•6H2O晶体的操作依次是蒸发浓缩、___________ 、过滤、洗涤、干燥。

已知:Ksp[Co(OH)2]=2×10-15,请回答以下问题:
(1)“滤渣I”主要成分是
(2)“氧化”时反应的离子方程式是
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为
(4)“萃取”和“反萃取”可简单表示为:2HX+Ni2+
 NiX2+2H+。在萃取过程中加入适量氨水,其作用是
NiX2+2H+。在萃取过程中加入适量氨水,其作用是(5)若起始时c(Co2+)=0.02mol∙L-1,“沉钴”过程中应控制pH
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
| 温度 | 低于30.8°C | 30.8°C~53.8°C | 53.8°C~280°C | 高于280°C |
| 晶体形态 | NiSO4•7H2O | NiSO4•6H2O | 多种结晶水合物 | NiSO4 |
您最近一年使用:0次
【推荐2】某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:
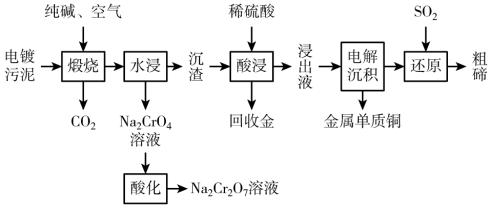
已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2 2CuO+TeO2。
2CuO+TeO2。
(1)煅烧时,Cr2O3发生反应的化学方程式为___________ 。
(2)为提高酸浸速率,可采用的措施是___________ (任写一条)。
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有___________ (写化学式)。
(4)在实际的含铬废水处理中,还可采用直接沉淀的方法,处理成本较低。
①已知含铬酸性废水中存在着Cr2O 和CrO
和CrO 相互转化的平衡,请用离子方程式表示它们之间的转化反应
相互转化的平衡,请用离子方程式表示它们之间的转化反应___________ 。
②在实际工业生产中,加入沉淀剂BaCl2溶液之前还要加入一定量的NaOH,这样有利于沉淀的生成,则生成的沉淀为___________ 。(写化学式)。
(5)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50g配成250mL溶液,用移液管取出25.00mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O 被还原为Cr3+)
被还原为Cr3+)
①氧化还原滴定过程中的离子方程式为___________ 。
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL,则所得产品中K2Cr2O7的纯度为___________ %。[已知M(K2Cr2O7)=294g·mol-1,计算结果保留三位有效数字]
(6)上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?___________ (填“是”或“否”)。{已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31}

已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2
 2CuO+TeO2。
2CuO+TeO2。(1)煅烧时,Cr2O3发生反应的化学方程式为
(2)为提高酸浸速率,可采用的措施是
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有
(4)在实际的含铬废水处理中,还可采用直接沉淀的方法,处理成本较低。
①已知含铬酸性废水中存在着Cr2O
 和CrO
和CrO 相互转化的平衡,请用离子方程式表示它们之间的转化反应
相互转化的平衡,请用离子方程式表示它们之间的转化反应②在实际工业生产中,加入沉淀剂BaCl2溶液之前还要加入一定量的NaOH,这样有利于沉淀的生成,则生成的沉淀为
(5)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50g配成250mL溶液,用移液管取出25.00mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O
 被还原为Cr3+)
被还原为Cr3+)①氧化还原滴定过程中的离子方程式为
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL,则所得产品中K2Cr2O7的纯度为
(6)上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?
您最近一年使用:0次
【推荐3】某科研小组以平板液晶显示屏生产过程中产生的废玻璃粉末(含CeO2、SiO2、Fe2O3等)为原料回收Ce的流程如图所示。
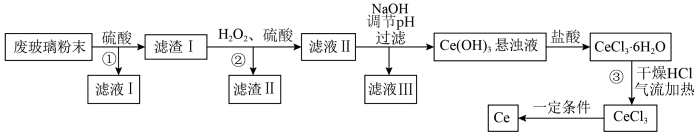
已知:Ce的常见化合价为+3和+4,CeO2具有强氧化性,一般不与常见的无机酸反应。回答下列问题:
(1)为了加快废玻璃粉末的酸浸速率,通常采用的方法有_______ (写两种)。
(2)加入H2O2只作还原剂,该反应的离子方程式为_______ 。操作③在加热的条件下通入干燥HCl气流的作用是_______ 。
(3)25℃当加入NaOH调节溶液pH=9时,Ce(OH)3悬浊液中c(Ce3+)=_______ mol/L。[已知:25℃时,Ce(OH)3的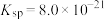 ]
]
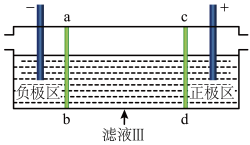
(4)三室式电渗析法处理滤液Ⅲ的原理如下图所示,采用惰性电极,ab、cd均为离子交换膜。充分电解后,可以得到循环至该流程使用的物质有_______ 。
(5)测定CeCl3样品纯度的方法如下:准确称量样品12.50 g配成200 mL溶液,取50.00 mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵[(NH4)2S2O8]溶液使Ce3+被氧化为Ce4+,然后用萃取剂萃取Ce4+,再用1.000 mol/L的FeSO4标准液滴定至终点,重复2~3次,平均消耗10.00mL标准液。
①滴定过程中发生反应的离子方程式为_______ 。
②CeCl3样品的纯度为_______ 。[已知M(CeCl3)=246.5 g/mol,结果保留2位小数]。

已知:Ce的常见化合价为+3和+4,CeO2具有强氧化性,一般不与常见的无机酸反应。回答下列问题:
(1)为了加快废玻璃粉末的酸浸速率,通常采用的方法有
(2)加入H2O2只作还原剂,该反应的离子方程式为
(3)25℃当加入NaOH调节溶液pH=9时,Ce(OH)3悬浊液中c(Ce3+)=
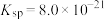 ]
](4)三室式电渗析法处理滤液Ⅲ的原理如下图所示,采用惰性电极,ab、cd均为离子交换膜。充分电解后,可以得到循环至该流程使用的物质有

(5)测定CeCl3样品纯度的方法如下:准确称量样品12.50 g配成200 mL溶液,取50.00 mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵[(NH4)2S2O8]溶液使Ce3+被氧化为Ce4+,然后用萃取剂萃取Ce4+,再用1.000 mol/L的FeSO4标准液滴定至终点,重复2~3次,平均消耗10.00mL标准液。
①滴定过程中发生反应的离子方程式为
②CeCl3样品的纯度为
您最近一年使用:0次
【推荐1】镍氢电池有着广泛的应用,旧电池的回收和再利用同样的重要。废旧镍氢电池中常含有NiOOH、 、及少量
、及少量 、FeO等,以下为金属分离以及镍的回收流程,按要求回答下列问题:
、FeO等,以下为金属分离以及镍的回收流程,按要求回答下列问题:
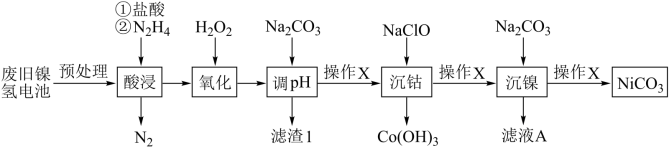
(1)“酸浸”中,加入 的主要作用是
的主要作用是_______ 。
(2)“氧化”过程中与 有关的离子方程式是
有关的离子方程式是_______ 。滤渣1主要成分是弱碱,其化学式是_______ 。
(3)滤液A的主要溶质是_______ ;操作X是_______ 。
(4)丁二酮肟(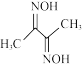 )是检验
)是检验 的灵敏试剂,在稀氨水介质中,
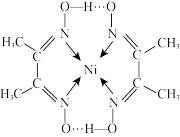
的灵敏试剂,在稀氨水介质中, 与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
回答下列问题:
①基态Ni中最外层电子所占据的原子轨道有_______ 种伸展方向。
② 丁二酮肟分子含有
丁二酮肟分子含有 键数目为
键数目为_______ ( 是阿伏加德罗常数的值)
是阿伏加德罗常数的值)
③丁二酮肟镍分子内不存在的作用力有_______ (填序号)
A.金属键 B.氢键 C. 键 D.配位键
键 D.配位键
 、及少量
、及少量 、FeO等,以下为金属分离以及镍的回收流程,按要求回答下列问题:
、FeO等,以下为金属分离以及镍的回收流程,按要求回答下列问题:
(1)“酸浸”中,加入
 的主要作用是
的主要作用是(2)“氧化”过程中与
 有关的离子方程式是
有关的离子方程式是(3)滤液A的主要溶质是
(4)丁二酮肟(
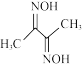 )是检验
)是检验 的灵敏试剂,在稀氨水介质中,
的灵敏试剂,在稀氨水介质中, 与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
回答下列问题:
①基态Ni中最外层电子所占据的原子轨道有
②
 丁二酮肟分子含有
丁二酮肟分子含有 键数目为
键数目为 是阿伏加德罗常数的值)
是阿伏加德罗常数的值)③丁二酮肟镍分子内不存在的作用力有
A.金属键 B.氢键 C.
 键 D.配位键
键 D.配位键
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】铝元素在自然界中主要存在于铝土矿(主要成分为A ,还含有F
,还含有F 、FeO、Si
、FeO、Si )中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
)中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
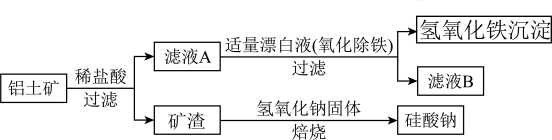
(1)在滤液A中加入漂白液,目的是氧化除铁,便于后期形成Fe(OH 沉淀,所得滤液B显酸性。
沉淀,所得滤液B显酸性。
①检验滤液A中含有F 的试剂为
的试剂为_____
②检验滤液B中不含有F 的实验操作方法为
的实验操作方法为_____ 。
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为_____ (填选项编号)。
a.氢氧化钠溶液 b.硫酸溶液 c.二氧化碳 d.氨水
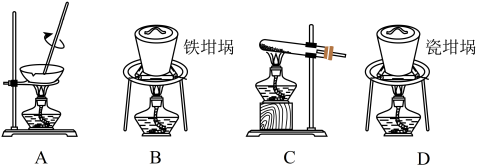
(2)矿渣中一定含有的物质是_____ (填化学式)。焙烧制备硅酸钠,可采用的装置为_____ (填选项编号)。
 ,还含有F
,还含有F 、FeO、Si
、FeO、Si )中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
)中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
(1)在滤液A中加入漂白液,目的是氧化除铁,便于后期形成Fe(OH
 沉淀,所得滤液B显酸性。
沉淀,所得滤液B显酸性。①检验滤液A中含有F
 的试剂为
的试剂为②检验滤液B中不含有F
 的实验操作方法为
的实验操作方法为③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
a.氢氧化钠溶液 b.硫酸溶液 c.二氧化碳 d.氨水
(2)矿渣中一定含有的物质是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】钛合金密度较小,常温下特别稳定,耐酸碱腐蚀,韧性好,高温下海绵状钛能与氧气反应,是航空、军工、电力等领域的必须金属材料。
I.由钛铁矿(主要成分是钛酸亚铁: ,还含有少量
,还含有少量 、
、 等杂质)制备
等杂质)制备 的一种工艺流程示意如下:
的一种工艺流程示意如下:

回答下列问题:
(1)为提高酸浸效率,可采取的措施有_______ (任写二种即可)。
(2) 中Ti的化合价为
中Ti的化合价为_______ ,“酸浸”中, 反应的离子方程式为
反应的离子方程式为_______ 。
(3)加入铁屑的作用是_______ 。
(4)①实验室完成“操作I”需用到的玻璃仪器有烧杯、_______ ,废渣的主要成分是_______ 。
②实验室完成“操作II”包含的具体操作有蒸发浓缩,_______ ,过滤,洗涤,干燥。
II.以 为原料,采用亨特(Hunter)法生产钛的流程如下:
为原料,采用亨特(Hunter)法生产钛的流程如下:

(5)沸腾氯化炉中反应的化学方程式为_______ 。
(6)制备海绵钛中Ar的作用是_______ 。
I.由钛铁矿(主要成分是钛酸亚铁:
 ,还含有少量
,还含有少量 、
、 等杂质)制备
等杂质)制备 的一种工艺流程示意如下:
的一种工艺流程示意如下:
回答下列问题:
(1)为提高酸浸效率,可采取的措施有
(2)
 中Ti的化合价为
中Ti的化合价为 反应的离子方程式为
反应的离子方程式为(3)加入铁屑的作用是
(4)①实验室完成“操作I”需用到的玻璃仪器有烧杯、
②实验室完成“操作II”包含的具体操作有蒸发浓缩,
II.以
 为原料,采用亨特(Hunter)法生产钛的流程如下:
为原料,采用亨特(Hunter)法生产钛的流程如下:
(5)沸腾氯化炉中反应的化学方程式为
(6)制备海绵钛中Ar的作用是
您最近一年使用:0次



