硫酸亚铁晶体( )俗称绿矾,可用来制药,受热易分解失去结晶水。某兴趣小组从实验室收集到一桶含有
)俗称绿矾,可用来制药,受热易分解失去结晶水。某兴趣小组从实验室收集到一桶含有 、
、 的废液,想从中回收金属铜和硫酸亚铁晶体,设计的实验方案如下图,结合实验方案回答下列问题:
的废液,想从中回收金属铜和硫酸亚铁晶体,设计的实验方案如下图,结合实验方案回答下列问题:
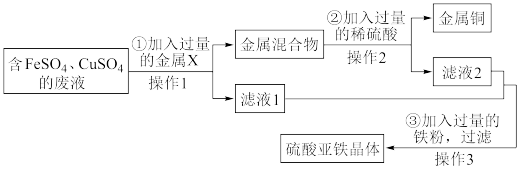
(1)步骤①中:
Ⅰ.金属X是__________ 。(填化学式)
Ⅱ.操作1的名称是__________ ,此操作中玻璃棒的作用是__________ 。
(2)步骤②中:
Ⅰ.加入过量稀硫酸的目的是__________ 。所得滤液2中含有的溶质是__________ 。(填化学式)
Ⅱ.洗涤金属铜的操作是__________ 。
Ⅲ.检验铜洗净的操作是_______________ 。
(3)操作3为蒸发浓缩、__________ 、过滤。
(4)若废液的体积为 ,废液中
,废液中 的浓度为
的浓度为 、
、 的浓度为
的浓度为 。
。
Ⅰ.理论上废液回收得到的金属铜的质量为__________ 。
Ⅱ.若整个过程中参与反应的铁共 ,
,__________ (填“能”或“不能”)计算出得到 的质量。若不能,写出原因;若能,写出计算过程和结果。
的质量。若不能,写出原因;若能,写出计算过程和结果。__________
 )俗称绿矾,可用来制药,受热易分解失去结晶水。某兴趣小组从实验室收集到一桶含有
)俗称绿矾,可用来制药,受热易分解失去结晶水。某兴趣小组从实验室收集到一桶含有 、
、 的废液,想从中回收金属铜和硫酸亚铁晶体,设计的实验方案如下图,结合实验方案回答下列问题:
的废液,想从中回收金属铜和硫酸亚铁晶体,设计的实验方案如下图,结合实验方案回答下列问题:
(1)步骤①中:
Ⅰ.金属X是
Ⅱ.操作1的名称是
(2)步骤②中:
Ⅰ.加入过量稀硫酸的目的是
Ⅱ.洗涤金属铜的操作是
Ⅲ.检验铜洗净的操作是
(3)操作3为蒸发浓缩、
(4)若废液的体积为
 ,废液中
,废液中 的浓度为
的浓度为 、
、 的浓度为
的浓度为 。
。Ⅰ.理论上废液回收得到的金属铜的质量为
Ⅱ.若整个过程中参与反应的铁共
 ,
, 的质量。若不能,写出原因;若能,写出计算过程和结果。
的质量。若不能,写出原因;若能,写出计算过程和结果。
更新时间:2024-02-16 11:27:43
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】以硫铁矿(主要成分为 ,还有少量CuS、
,还有少量CuS、 等杂质)为原料制备绿矾晶体
等杂质)为原料制备绿矾晶体 的工艺流程如下:
的工艺流程如下:

(1)硫铁矿的主要成分 中铁元素化合价为
中铁元素化合价为_______ 。
(2)“酸浸”过程,矿渣中的 与稀
与稀 反应的离子方程式
反应的离子方程式_______ 。
(3)烟气中的 会污染环境,可用足量氨水吸收,写出该反应的离子方程式
会污染环境,可用足量氨水吸收,写出该反应的离子方程式_______ 。
(4)写出检验滤液中阴离子的方法_______ 。
(5)铁粉还原过滤,滤渣主要成分是_______ (写化学式)。
(6)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到 溶液。其过程如图所示:
溶液。其过程如图所示:

已知总反应为: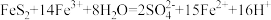 。写出过程II反应的离子方程式
。写出过程II反应的离子方程式______ 。
 ,还有少量CuS、
,还有少量CuS、 等杂质)为原料制备绿矾晶体
等杂质)为原料制备绿矾晶体 的工艺流程如下:
的工艺流程如下:
(1)硫铁矿的主要成分
 中铁元素化合价为
中铁元素化合价为(2)“酸浸”过程,矿渣中的
 与稀
与稀 反应的离子方程式
反应的离子方程式(3)烟气中的
 会污染环境,可用足量氨水吸收,写出该反应的离子方程式
会污染环境,可用足量氨水吸收,写出该反应的离子方程式(4)写出检验滤液中阴离子的方法
(5)铁粉还原过滤,滤渣主要成分是
(6)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到
 溶液。其过程如图所示:
溶液。其过程如图所示:
已知总反应为:
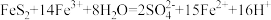 。写出过程II反应的离子方程式
。写出过程II反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某待测液中可能含有Ba2+、Fe3+、K+、Fe2+、CO32-、Cl-等离子,进行如下实验:
①取适量待测液于试管中,加入稀H2SO4,有白色沉淀生成;
②过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现;
③在步骤②中的溶液中,继续滴加氯水,溶液立即变红。
根据实验现象回答:
(1)待测液中一定含有的离子是___________ ,一定不含有的离子是_______________ ;
(2)还有一种离子不能确定是否存在,要确认这种离子的实验方法和现象是_________________ 。
①取适量待测液于试管中,加入稀H2SO4,有白色沉淀生成;
②过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现;
③在步骤②中的溶液中,继续滴加氯水,溶液立即变红。
根据实验现象回答:
(1)待测液中一定含有的离子是
(2)还有一种离子不能确定是否存在,要确认这种离子的实验方法和现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】Na2S2O4俗称保险粉,常用作纺织工业的漂白剂、脱色剂等。某科研小组制备并探究其性质。制备Na2S2O4 (夹持、加热装置略去)的装置如图所示。
资料:Na2S2O4易溶于水,具有极强的还原性,易被空气中的氧气氧化,在碱性介质中稳定。
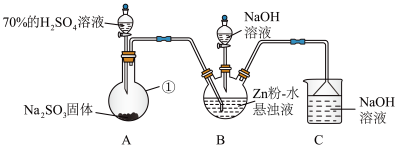
(1)仪器①的名称是__________ 。
(2)B装置用于制备Na2S2O4。第一步反应: Zn+2SO2 ZnS2O4;第二步,加入NaOH溶液,在28~35℃下反应生成Na2S2O4,该步反应的化学方程式为
ZnS2O4;第二步,加入NaOH溶液,在28~35℃下反应生成Na2S2O4,该步反应的化学方程式为_______________________________ 。
(3)B装置反应前,先进行的实验操作是__________ 。
(4)隔绝空气加热Na2S2O4固体,完全分解后得到固体产物Na2SO3、Na2S2O3 (与酸反应可生成S和SO2)和气体产物SO2,但科研小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是_______________________________ 。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液、KMnO4溶液)
(5)制备纳米级银粉:用NaOH溶液溶解Na2S2O4,加入一定量的AgNO3溶液,生成纳米级银粉。在制备银粉的反应中,氧化剂和还原剂的物质的量之比为2:1,且生成的含硫物质只有一种,写出该反应的离子方程式:_______________________________ 。
资料:Na2S2O4易溶于水,具有极强的还原性,易被空气中的氧气氧化,在碱性介质中稳定。

(1)仪器①的名称是
(2)B装置用于制备Na2S2O4。第一步反应: Zn+2SO2
 ZnS2O4;第二步,加入NaOH溶液,在28~35℃下反应生成Na2S2O4,该步反应的化学方程式为
ZnS2O4;第二步,加入NaOH溶液,在28~35℃下反应生成Na2S2O4,该步反应的化学方程式为(3)B装置反应前,先进行的实验操作是
(4)隔绝空气加热Na2S2O4固体,完全分解后得到固体产物Na2SO3、Na2S2O3 (与酸反应可生成S和SO2)和气体产物SO2,但科研小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是
(5)制备纳米级银粉:用NaOH溶液溶解Na2S2O4,加入一定量的AgNO3溶液,生成纳米级银粉。在制备银粉的反应中,氧化剂和还原剂的物质的量之比为2:1,且生成的含硫物质只有一种,写出该反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
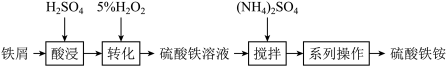
【推荐1】硫酸铁铵[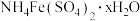 ]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用铁屑来制备硫酸铁铵,流程如下:
]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用铁屑来制备硫酸铁铵,流程如下:
已知:相同温度下, 在水中的溶解度比
在水中的溶解度比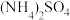 、
、 的溶解度小。
的溶解度小。
回答下列问题:
(1)“酸浸”铁单质与硫酸反应的离子方程式为_______ 。
(2)“转化”中加入足量的 ,目的是
,目的是_______ ,写出该反应的离子方程式为_______ 。
(3)“系列操作”的过程为_______ ,经干燥得到硫酸铁铵晶体样品。
(4)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为_______ 。
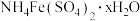 ]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用铁屑来制备硫酸铁铵,流程如下:
]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用铁屑来制备硫酸铁铵,流程如下:
已知:相同温度下,
 在水中的溶解度比
在水中的溶解度比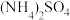 、
、 的溶解度小。
的溶解度小。回答下列问题:
(1)“酸浸”铁单质与硫酸反应的离子方程式为
(2)“转化”中加入足量的
 ,目的是
,目的是(3)“系列操作”的过程为
(4)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铝是一种重要金属,从铝土矿(主要成分为 、
、 、
、 等)中冶炼Al的工业生产流程如图:
等)中冶炼Al的工业生产流程如图:
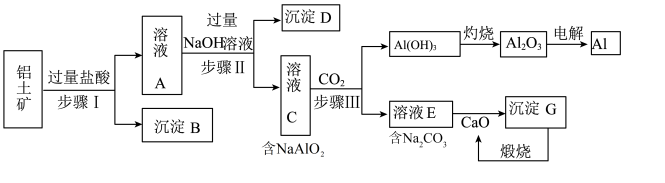
已知: 是酸性氧化物,不溶于盐酸
是酸性氧化物,不溶于盐酸
(1)步骤Ⅰ、Ⅱ、Ⅲ都要用到的分离方法是过滤。在实验室模拟该操作,要用到的玻璃仪器有:烧杯、_______ 、________ 。
(2)溶液A含有的金属阳离子为_______ 。沉淀D的化学式为________ 。
(3)步骤Ⅲ生成 沉淀的化学方程式为
沉淀的化学方程式为_______ 。
(4)生产过程中,可循环使用的物质有 、
、________ 、_________ (填化学式)。
 、
、 、
、 等)中冶炼Al的工业生产流程如图:
等)中冶炼Al的工业生产流程如图:
已知:
 是酸性氧化物,不溶于盐酸
是酸性氧化物,不溶于盐酸(1)步骤Ⅰ、Ⅱ、Ⅲ都要用到的分离方法是过滤。在实验室模拟该操作,要用到的玻璃仪器有:烧杯、
(2)溶液A含有的金属阳离子为
(3)步骤Ⅲ生成
 沉淀的化学方程式为
沉淀的化学方程式为(4)生产过程中,可循环使用的物质有
 、
、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】铁的化合物有广泛的应用,如碳酸亚铁(FeCO3)可以作为补血剂,铁红可以作为颜料。工业上可以利用硫酸厂产生的烧渣(主要成分含Fe2O3、FeO,还有一定量的SiO2)制备碳酸亚铁的工艺流程如图所示:
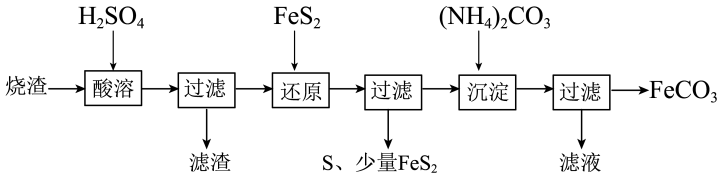
(1)“酸溶”时加快反应速率的方法有___________ (任写一种)。
(2)还原剂FeS2中铁元素的化合价为___________ ,已知“还原”时,FeS2与H2SO4不反应,Fe3+通过两个反应被还原,其中一个反应为FeS2+14Fe3++8H2O=15Fe2++2 +16H+,另一个反应中FeS2中硫元素全部转化为淡黄色沉淀,则相应的离子方程式为
+16H+,另一个反应中FeS2中硫元素全部转化为淡黄色沉淀,则相应的离子方程式为___________ 。
(3)FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色Fe(OH)3,同时释放出CO2,则与FeCO3反应的物质有___________ (填化学式)。
(4)为得到较为纯净的FeCO3需对所得产品进行多次洗涤操作,请简要描述洗涤FeCO3的基本操作___________ 。
(5)取一定质量的FeCO3样品将其溶于适量稀盐酸中制得FeCl2溶液,若想检验在溶解的过程中是有铁元素被氧化,可加入的检验试剂是___________ (填试剂名称),可观察到的现象有___________ 。

(1)“酸溶”时加快反应速率的方法有
(2)还原剂FeS2中铁元素的化合价为
 +16H+,另一个反应中FeS2中硫元素全部转化为淡黄色沉淀,则相应的离子方程式为
+16H+,另一个反应中FeS2中硫元素全部转化为淡黄色沉淀,则相应的离子方程式为(3)FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色Fe(OH)3,同时释放出CO2,则与FeCO3反应的物质有
(4)为得到较为纯净的FeCO3需对所得产品进行多次洗涤操作,请简要描述洗涤FeCO3的基本操作
(5)取一定质量的FeCO3样品将其溶于适量稀盐酸中制得FeCl2溶液,若想检验在溶解的过程中是有铁元素被氧化,可加入的检验试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验小组利用下图装置制备Na2S2O3(夹持装置略去)。
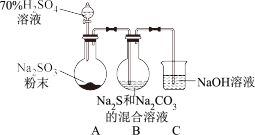
已知: 。
。
回答下列问题:
(1)仪器a的名称为___________ 。
(2)开始时,将分液漏斗中的液体放入仪器a,放液的正确操作是___________ 。
(3)装置A中发生反应的化学方程式是___________ 。
(4)装置C中NaOH溶液的作用是___________ 。
(5)该装置存在缺陷,提出改进措施___________ (答出一点即可)。

已知:
 。
。回答下列问题:
(1)仪器a的名称为
(2)开始时,将分液漏斗中的液体放入仪器a,放液的正确操作是
(3)装置A中发生反应的化学方程式是
(4)装置C中NaOH溶液的作用是
(5)该装置存在缺陷,提出改进措施
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】氯化亚铜是一种白色粉末,难溶于水,溶于浓盐酸生成氯亚铜酸,常用作催化剂、杀菌剂。以辉铜矿(主要成分为 ,含少量
,含少量 、
、 等杂质)和软锰矿(主要成分
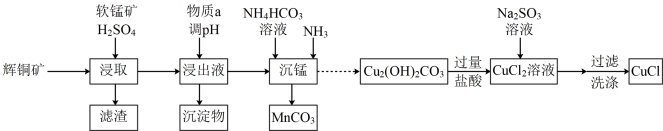
等杂质)和软锰矿(主要成分 )为原料制备碱式碳酸铜,并进一步制取氯化亚铜(CuCl)的工艺流程如下:
)为原料制备碱式碳酸铜,并进一步制取氯化亚铜(CuCl)的工艺流程如下:
已知:① 的沸点为46.2℃
的沸点为46.2℃
②常温下几种物质开始沉淀与完全沉淀时的pH如下表
请回答下列问题:
(1)为加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有___________ (任写一种),浸取过程中得到一种单质,写出主要反应的化学方程式___________ ,该单质可用 提取回收,回收过程中温度应控制在40℃~45℃之间,不宜过高的原因是
提取回收,回收过程中温度应控制在40℃~45℃之间,不宜过高的原因是___________ 。
(2)调节pH的范围为_____ ,物质a可选用_____ (填序号)。
A.CuO B. C.
C. D.
D.
(3)“沉锰”时发生反应的离子方程式_____ 。
(4)得到的CuCl晶体需用水洗,判断晶体是否洗涤干净的操作是___________ 。
 ,含少量
,含少量 、
、 等杂质)和软锰矿(主要成分
等杂质)和软锰矿(主要成分 )为原料制备碱式碳酸铜,并进一步制取氯化亚铜(CuCl)的工艺流程如下:
)为原料制备碱式碳酸铜,并进一步制取氯化亚铜(CuCl)的工艺流程如下:
已知:①
 的沸点为46.2℃
的沸点为46.2℃②常温下几种物质开始沉淀与完全沉淀时的pH如下表
| 金属离子 |  |  |  |  |
| 开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
| 完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
请回答下列问题:
(1)为加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有
 提取回收,回收过程中温度应控制在40℃~45℃之间,不宜过高的原因是
提取回收,回收过程中温度应控制在40℃~45℃之间,不宜过高的原因是(2)调节pH的范围为
A.CuO B.
 C.
C. D.
D.
(3)“沉锰”时发生反应的离子方程式
(4)得到的CuCl晶体需用水洗,判断晶体是否洗涤干净的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在工业生产上中,主要用Na2SO3制造亚硫酸纤维素酯、硫代硫酸钠、有机化学药品、漂白织物等。但Na2SO3在空气中易氧化为Na2SO4而变质。为了求出变质样品中Na2SO3的含量,采用0.2 mol·L-1KMnO4酸性溶液滴定用样品配制的溶液。反应离子方程式是:2MnO4-+5SO32-+6H+=2Mn2++5SO42-+3H2O,称取20 g样品,配成250 mL溶液,量取25 mL进行滴定,记录数据,再重复2次实验。
填空完成问题:
(1)滴定实验不需要下列仪器中的________ 。
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL) C.量筒(10 mL) D.锥形瓶 E.铁架台 F.滴定管夹
G.白纸 H.玻璃棒
(2)已知滴定过程不需要指示剂,理由是_______________________ 。
(3)下列操作中可能使所测Na2SO3溶液的浓度数值偏低的是________ (填字母)。
A.盛放Na2SO3溶液的滴定管没有使用Na2SO3溶液润洗
B.锥形瓶内有水残留,没有烘干,装入待测的Na2SO3溶液滴定
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
(4)滴定完毕,三次实验平均消耗0.2 mol·L-1KMnO4酸性溶液20.00mL,则样品中Na2SO3的百分含量为:_________ 。
填空完成问题:
(1)滴定实验不需要下列仪器中的
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL) C.量筒(10 mL) D.锥形瓶 E.铁架台 F.滴定管夹
G.白纸 H.玻璃棒
(2)已知滴定过程不需要指示剂,理由是
(3)下列操作中可能使所测Na2SO3溶液的浓度数值偏低的是
A.盛放Na2SO3溶液的滴定管没有使用Na2SO3溶液润洗
B.锥形瓶内有水残留,没有烘干,装入待测的Na2SO3溶液滴定
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
(4)滴定完毕,三次实验平均消耗0.2 mol·L-1KMnO4酸性溶液20.00mL,则样品中Na2SO3的百分含量为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
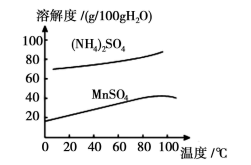
【推荐1】以含锰废料(含有MnO2、CuO、Fe和少量CaO)为原料制备MnSO4的一种流程如下:

已知:I.烧渣中含有MnO、CuO、Cu、Fe、CaO。
II.难溶电解质的溶度积常数如下表所示:
回答下列问题:
(1)“焙烧”过程生成的气体有_______ 。
(2)“酸浸”时所加稀H2SO4稍过量的原因为_______ ,滤渣1的主要成分为_______ (填化学式)。
(3)“氧化”过程中加入的X可以是_______ 。
a.Cl2 b.H2O2 c.MnO2 d.KMnO4
(4)若“溶液”中c(Cu2+)=0.044 mol·L-1,“滤液2”的体积是“溶液”体积的2倍,“调pH”的范围为_______ 。
(5)写出加入(NH4)2S时的离子方程式_______ 。
(6)已知:(NH4)2SO4与MnSO4的溶解度曲线如图所示。“操作”主要包括蒸发浓缩、降温结晶、过滤、_______ 、干燥,需控制温度为_______ (填选项字母)得到产品较多。
a.80℃ b.60℃ c.40℃ d.20℃

已知:I.烧渣中含有MnO、CuO、Cu、Fe、CaO。
II.难溶电解质的溶度积常数如下表所示:
 物质 物质 | Mn(OH)2 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 溶度积常数(Ksp) | 1.9×10-13 | 1.8×10-16 | 2.2×10-20 | 8.0×10-38 |
(1)“焙烧”过程生成的气体有
(2)“酸浸”时所加稀H2SO4稍过量的原因为
(3)“氧化”过程中加入的X可以是
a.Cl2 b.H2O2 c.MnO2 d.KMnO4
(4)若“溶液”中c(Cu2+)=0.044 mol·L-1,“滤液2”的体积是“溶液”体积的2倍,“调pH”的范围为
(5)写出加入(NH4)2S时的离子方程式
(6)已知:(NH4)2SO4与MnSO4的溶解度曲线如图所示。“操作”主要包括蒸发浓缩、降温结晶、过滤、
a.80℃ b.60℃ c.40℃ d.20℃

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海水资源非常丰富。某化学实验小组同学为了从海带中提取碘和海水提溴,进行以下实验:
I.从海带中提取碘单质,实验流程图如下:
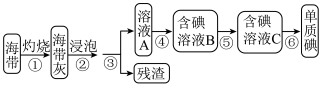
已知:步骤⑥是用反萃取法从碘的四氯化碳溶液中提取碘。
回答下列问题:
(1)在进行步骤①之前,称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入___________ 中灼烧至海带完全成灰烬。
(2)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,未发现明显变化,再加入F后溶液颜色变蓝,此反应的离子方程式是___________ ;乙同学认为使用稀硫酸和H2O2溶液能更有利于提取碘,写出离子方程式___________ 。
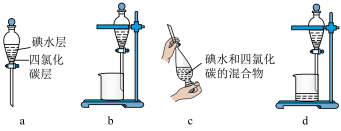
(3)步骤⑤中用分液漏斗得到碘的四氯化碳溶液,其操作顺序是___________ (填字母)。
(4)将得到的单质碘,干燥、称量,其质量为n g,则海带中碘元素的含量为___________ 。
II.模拟用空气吹出法从海水中提取溴的工艺流程,如下图:
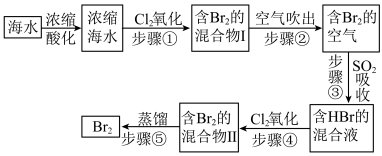
请回答下列问题。
(5)将海水浓缩的方法是___________ 。
(6)步骤②通入热空气吹出Br2,利用了Br2的___________ 性质。
(7)步骤①反应的离子方程式是___________ ,步骤③反应的离子方程式是___________ ,从理论上分析,下列也能吸收溴的是___________ (填字母)。
A.NaOH B.Na2SO3 C.H2O D.FeCl2
(8)已知海水中Br-含量为64mg/L,依据上述流程,若将5m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为___________ L(忽略Cl2的溶解)。
I.从海带中提取碘单质,实验流程图如下:

已知:步骤⑥是用反萃取法从碘的四氯化碳溶液中提取碘。
回答下列问题:
(1)在进行步骤①之前,称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入
(2)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,未发现明显变化,再加入F后溶液颜色变蓝,此反应的离子方程式是
(3)步骤⑤中用分液漏斗得到碘的四氯化碳溶液,其操作顺序是

(4)将得到的单质碘,干燥、称量,其质量为n g,则海带中碘元素的含量为
II.模拟用空气吹出法从海水中提取溴的工艺流程,如下图:

请回答下列问题。
(5)将海水浓缩的方法是
(6)步骤②通入热空气吹出Br2,利用了Br2的
(7)步骤①反应的离子方程式是
A.NaOH B.Na2SO3 C.H2O D.FeCl2
(8)已知海水中Br-含量为64mg/L,依据上述流程,若将5m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】硒是人体不可缺少的微量元素,硒的应用范围非常广泛。以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、 、CuO、ZnO、
、CuO、ZnO、 等)提取硒一种工艺流程如下:
等)提取硒一种工艺流程如下:
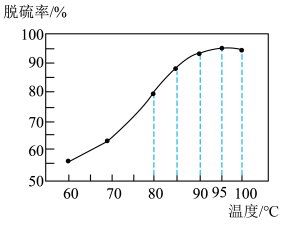
(1)“脱硫”时,脱硫率随温度的变化如图所示,试分析随温度的升高,脱硫率呈上升趋势的原因;_______ ,最佳脱硫温度为_______ 。 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(3)“控电位还原”,是将电位高的物质先还原,电位低的物质保留在溶液中,以达到物质的分离。可采用硫脲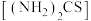 联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。
联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。
控制电位在0.740~1.511V范围内,在氧化酸浸液中添加硫脲,可选择性还原 ,该过程的还原反应(半反应)式为
,该过程的还原反应(半反应)式为_______ ,为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在_______ V以上。
(4)“精制”过程中 先将Se浸出转化成硒代硫酸钠(
先将Se浸出转化成硒代硫酸钠(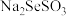 ),
),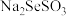 再被
再被 酸化生成硒的离子方程式为
酸化生成硒的离子方程式为_______ 。
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg⋅g ,则精硒中铁的质量分数为
,则精硒中铁的质量分数为_______ %。
 、CuO、ZnO、
、CuO、ZnO、 等)提取硒一种工艺流程如下:
等)提取硒一种工艺流程如下: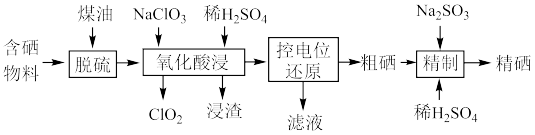
(1)“脱硫”时,脱硫率随温度的变化如图所示,试分析随温度的升高,脱硫率呈上升趋势的原因;
 ,该反应的化学方程式为
,该反应的化学方程式为(3)“控电位还原”,是将电位高的物质先还原,电位低的物质保留在溶液中,以达到物质的分离。可采用硫脲
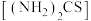 联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。
联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。名称 |
|
|
|
|
|
|
中位/V | 0.345 | -0.760 | -0.440 | 0.770 | 1.511 | 0.740 |
 ,该过程的还原反应(半反应)式为
,该过程的还原反应(半反应)式为(4)“精制”过程中
 先将Se浸出转化成硒代硫酸钠(
先将Se浸出转化成硒代硫酸钠(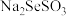 ),
), 再被
再被 酸化生成硒的离子方程式为
酸化生成硒的离子方程式为(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg⋅g
 ,则精硒中铁的质量分数为
,则精硒中铁的质量分数为
您最近一年使用:0次

 /Zn
/Zn


