以硫酸工业生产后的硫铁矿烧渣(主要成分为 、
、 ,还含有少量
,还含有少量 、
、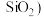 制备铁红颜料(
制备铁红颜料( )的生产流程如下:
)的生产流程如下:
(1)要提高酸浸的效率,可采取的措施为___________ (任写一种)。
(2)“酸浸”过程中 与稀硫酸反应,该反应的化学方程式为
与稀硫酸反应,该反应的化学方程式为___________ 。
(3)“步骤1”的操作名称为___________ ,“滤渣1”的主要成份为___________ 。
(4)加入过量铁粉的目的有以下两点:
①除去过量的硫酸;
②___________ 。检验“滤液X”金属阳离子是否完全转化适宜的试剂为___________ 。
(5)“滤液Y”反应生成 的同时产生无色无味且能使澄清石灰水变浑浊的气体,该反应的离子方程式为
的同时产生无色无味且能使澄清石灰水变浑浊的气体,该反应的离子方程式为___________ ,“滤液Z”中主要成份的用途为___________ (任写一种)。
(6)若经“步骤3”得到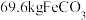 ,使其完全焙烧得到铁红(
,使其完全焙烧得到铁红( ),理论上需要氧气的体积为
),理论上需要氧气的体积为___________ L(标准状况下)。
 、
、 ,还含有少量
,还含有少量 、
、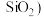 制备铁红颜料(
制备铁红颜料( )的生产流程如下:
)的生产流程如下:
(1)要提高酸浸的效率,可采取的措施为
(2)“酸浸”过程中
 与稀硫酸反应,该反应的化学方程式为
与稀硫酸反应,该反应的化学方程式为(3)“步骤1”的操作名称为
(4)加入过量铁粉的目的有以下两点:
①除去过量的硫酸;
②
(5)“滤液Y”反应生成
 的同时产生无色无味且能使澄清石灰水变浑浊的气体,该反应的离子方程式为
的同时产生无色无味且能使澄清石灰水变浑浊的气体,该反应的离子方程式为(6)若经“步骤3”得到
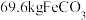 ,使其完全焙烧得到铁红(
,使其完全焙烧得到铁红( ),理论上需要氧气的体积为
),理论上需要氧气的体积为
更新时间:2024-02-04 18:32:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】次氯酸溶液是常用的消毒剂和漂白剂。某学习小组根据需要欲制备某浓度的次氯酸溶液。
资料1: 极易溶于
极易溶于 。
。
资料2:常温常压下, 为棕黄色气体,沸点为
为棕黄色气体,沸点为 ,
, 以上会分解生成
以上会分解生成 和
和 ,
, 易溶于水并与水立即反应生成
易溶于水并与水立即反应生成 。
。
资料3:将氯气和空气(不参与反应)按体积比1:3混合通入潮湿的碳酸钠中,用水吸收 (不含
(不含 )制得次氯酸溶液。
)制得次氯酸溶液。
用如图装置制备次氯酸溶液。

回答下列问题:
(1)各装置的连接顺序为___________→___________→___________→___________→E。___________
(2)实验中控制氯气与空气流速的方法是___________ 。
(3)反应过程中,装置B需放在冷水中,其目的是___________ 。
(4)装置E采用棕色圆底烧瓶是因为___________ 。
(5)将氯气通入潮湿的碳酸钠中,充分反应, 气体生成的同时生成碳酸氢钠以及一种含氯元素的盐。请写出此反应的化学方程式:
气体生成的同时生成碳酸氢钠以及一种含氯元素的盐。请写出此反应的化学方程式:___________ 。每消耗9g水时生成 的物质的量为
的物质的量为___________ mol。
资料1:
 极易溶于
极易溶于 。
。资料2:常温常压下,
 为棕黄色气体,沸点为
为棕黄色气体,沸点为 ,
, 以上会分解生成
以上会分解生成 和
和 ,
, 易溶于水并与水立即反应生成
易溶于水并与水立即反应生成 。
。资料3:将氯气和空气(不参与反应)按体积比1:3混合通入潮湿的碳酸钠中,用水吸收
 (不含
(不含 )制得次氯酸溶液。
)制得次氯酸溶液。用如图装置制备次氯酸溶液。

回答下列问题:
(1)各装置的连接顺序为___________→___________→___________→___________→E。
(2)实验中控制氯气与空气流速的方法是
(3)反应过程中,装置B需放在冷水中,其目的是
(4)装置E采用棕色圆底烧瓶是因为
(5)将氯气通入潮湿的碳酸钠中,充分反应,
 气体生成的同时生成碳酸氢钠以及一种含氯元素的盐。请写出此反应的化学方程式:
气体生成的同时生成碳酸氢钠以及一种含氯元素的盐。请写出此反应的化学方程式: 的物质的量为
的物质的量为
您最近一年使用:0次
【推荐2】某学生为测定某烧碱样品中NaOH的质量分数,进行如下实验(已知该样品中含有少量不与酸作用的杂质):
A.在250 mL 容量瓶中定容,配制成250 mL 烧碱溶液
B.用移液管(或碱式滴定管)量取25.00 mL 烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品20.5 g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为1.00 mol/L 的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度数V1 mL
E.在锥形瓶下垫一张白纸,滴定至溶液变为橙色为止,记录终点耗酸体积V2 mL
回答下列问题:
(1)正确的操作步骤的顺序是(填写字母)______ →______ →________ →______ →______ 。
(2)滴定管读数应注意________________________________ 。
(3)E步骤的操作中在锥形瓶下垫一张白纸的作用是__________________ 。
(4)下列操作中可能使所测NaOH的质量分数偏低的是________ (填字母)。
a.A步操作中未将溶液冷却至室温就转移到容量瓶中定容
b.C步操作中,称量药品时,砝码放在左盘,NaOH放在右盘
c.D步操作中酸式滴定管在装入标准H2SO4溶液前未用标准液润洗
d.读取硫酸体积时,开始时仰视读数,结束时俯视读数
(5)硫酸的初读数和末读数如图所示。末读数为______ mL,初读数为____ mL,用量为________ mL。按滴定所得数据来计算出的烧碱样品中NaOH的质量分数为________ 。
A.在250 mL 容量瓶中定容,配制成250 mL 烧碱溶液
B.用移液管(或碱式滴定管)量取25.00 mL 烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品20.5 g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为1.00 mol/L 的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度数V1 mL
E.在锥形瓶下垫一张白纸,滴定至溶液变为橙色为止,记录终点耗酸体积V2 mL
回答下列问题:
(1)正确的操作步骤的顺序是(填写字母)
(2)滴定管读数应注意
(3)E步骤的操作中在锥形瓶下垫一张白纸的作用是
(4)下列操作中可能使所测NaOH的质量分数偏低的是
a.A步操作中未将溶液冷却至室温就转移到容量瓶中定容
b.C步操作中,称量药品时,砝码放在左盘,NaOH放在右盘
c.D步操作中酸式滴定管在装入标准H2SO4溶液前未用标准液润洗
d.读取硫酸体积时,开始时仰视读数,结束时俯视读数
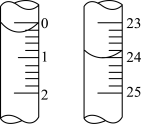
(5)硫酸的初读数和末读数如图所示。末读数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组为探究 Na2CO3溶液的性质, 需要480mL 0.2 mol∙L−1的Na2CO3溶液。溶液的配制过程如图所示:
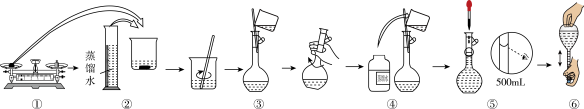
(1)配制过程中有一处明显错误为___________ (填序号)。
(2)若用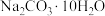 来配制溶液,需选择的玻璃仪器为量筒、玻璃棒、烧杯、
来配制溶液,需选择的玻璃仪器为量筒、玻璃棒、烧杯、___________ 、___________ 。
(3)用托盘天平称取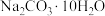 ,若所取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度
,若所取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度___________ (填“偏大”、 “偏小”或“无影响”)。
(4)若配制得到的 溶液中混有部分
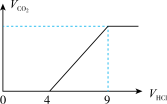
溶液中混有部分 ,为确定其纯度,取适量溶液,向溶液中滴加稀盐酸(边滴边振荡,假设生成的气体完全逸出),记录生成二氧化碳的体积和消耗盐酸的体积并绘制图像如图,V(HCl)的体积为4~9阶段,发生反应的离子方程式为
,为确定其纯度,取适量溶液,向溶液中滴加稀盐酸(边滴边振荡,假设生成的气体完全逸出),记录生成二氧化碳的体积和消耗盐酸的体积并绘制图像如图,V(HCl)的体积为4~9阶段,发生反应的离子方程式为___________ ,根据图计算可知,样品中纯碱和小苏打的物质的量之比为___________ 。

(1)配制过程中有一处明显错误为
(2)若用
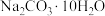 来配制溶液,需选择的玻璃仪器为量筒、玻璃棒、烧杯、
来配制溶液,需选择的玻璃仪器为量筒、玻璃棒、烧杯、(3)用托盘天平称取
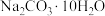 ,若所取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度
,若所取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度(4)若配制得到的
 溶液中混有部分
溶液中混有部分 ,为确定其纯度,取适量溶液,向溶液中滴加稀盐酸(边滴边振荡,假设生成的气体完全逸出),记录生成二氧化碳的体积和消耗盐酸的体积并绘制图像如图,V(HCl)的体积为4~9阶段,发生反应的离子方程式为
,为确定其纯度,取适量溶液,向溶液中滴加稀盐酸(边滴边振荡,假设生成的气体完全逸出),记录生成二氧化碳的体积和消耗盐酸的体积并绘制图像如图,V(HCl)的体积为4~9阶段,发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钛酸钡( )具有高介电常数和低介电损耗,是压电陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是压电陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。 的电离方程式为
的电离方程式为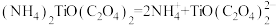 请回答:
请回答:
(1)下列说法正确的是___________。
(2)用溶液2提取的一种副产物可作肥料,该物质是___________ (写电子式);得到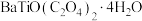 沉淀后需要洗涤,请写出实验操作以检验洗涤是否完全
沉淀后需要洗涤,请写出实验操作以检验洗涤是否完全___________ 。
(3)请写出煅烧过程发生反应的化学方程式___________ 。
(4)如何设计实验方案检验气体A经干燥处理后的剩余气体成分________ 。
 )具有高介电常数和低介电损耗,是压电陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是压电陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。
 的电离方程式为
的电离方程式为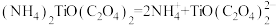 请回答:
请回答:(1)下列说法正确的是___________。
| A.压电陶瓷属于新型无机非金属材料,能实现机械能与电能的相互转化 |
B.溶液1中加入 溶液的离子方程式为 溶液的离子方程式为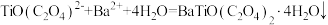 |
| C.实验室中煅烧用到的主要仪器有酒精喷灯、三脚架、泥三角和蒸发皿 |
| D.流程中的三步反应均为非氧化还原反应 |
(2)用溶液2提取的一种副产物可作肥料,该物质是
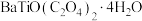 沉淀后需要洗涤,请写出实验操作以检验洗涤是否完全
沉淀后需要洗涤,请写出实验操作以检验洗涤是否完全(3)请写出煅烧过程发生反应的化学方程式
(4)如何设计实验方案检验气体A经干燥处理后的剩余气体成分
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】元素周期表的建立是化学发展史上的重要里程碑之一,部分元素在元素周期表中的位置如图:
(1)a、b、d、f、h五种元素原子的最外层电子数之和为_______ 。
(2)能比较得出h、j非金属性强弱的离子反应方程式为_______ (用化学符号表示,下同)。
(3)b、c、f、g四种元素简单离子中,半径最大的是_______ ,半径最小的是_______ 。
(4)写出d的最高价氧化物和b的最高价氧化物的水化物在水溶液中发生的离子反应方程式_______ 。
(5)比较e、g、h最高价含氧酸酸性强弱:_______ >_______ >_______ (写出具体物质化学式)。
| 族 周期 | ⅠA | ||||||
| 1 | a | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | f | ||||||
| 3 | b | c | d | e | g | h | |
| 4 | i | Ca | j |
(2)能比较得出h、j非金属性强弱的离子反应方程式为
(3)b、c、f、g四种元素简单离子中,半径最大的是
(4)写出d的最高价氧化物和b的最高价氧化物的水化物在水溶液中发生的离子反应方程式
(5)比较e、g、h最高价含氧酸酸性强弱:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】电池级碳酸锂是制造LiCoO2等锂离子电池必不可少的原材料。以锂云母浸出液(含Li+、Al3+、Fe3+、Ca2+、 等)制取电池级Li2CO3的工艺流程如下:
等)制取电池级Li2CO3的工艺流程如下:
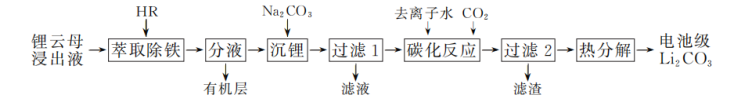
已知:①HR为酸性磷类有机萃取剂,难溶于水,可萃取Fe3+,萃取时发生反应:Fe3++3HR⇌FeR3+3H+,生成的FeR3可溶解在HR中。
②Li2CO3、LiHCO3的溶解度如图1所示:

(1)HR萃取剂使用前先用一定量的NaOH进行处理的目的是___________ 。
(2)沉锂过程中会有Li2CO3、CaCO3和Al(OH)3生成。写出沉锂时生成Al(OH)3反应的离子方程式:___________ 。
(3)过滤1后所得沉淀用热水洗涤的目的是___________ 。
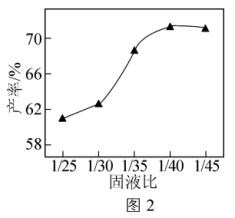
(4)其他条件相同,向过滤1所得滤渣加入不同体积的去离子水,以一定流速通入CO2气体,测得热分解后电池级Li2CO3的产率随碳化反应固液比[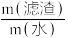 ]变化曲线如图2所示。Li2CO3产率随固液比减小而增加的原因是
]变化曲线如图2所示。Li2CO3产率随固液比减小而增加的原因是___________ 。
 等)制取电池级Li2CO3的工艺流程如下:
等)制取电池级Li2CO3的工艺流程如下:
已知:①HR为酸性磷类有机萃取剂,难溶于水,可萃取Fe3+,萃取时发生反应:Fe3++3HR⇌FeR3+3H+,生成的FeR3可溶解在HR中。
②Li2CO3、LiHCO3的溶解度如图1所示:

(1)HR萃取剂使用前先用一定量的NaOH进行处理的目的是
(2)沉锂过程中会有Li2CO3、CaCO3和Al(OH)3生成。写出沉锂时生成Al(OH)3反应的离子方程式:
(3)过滤1后所得沉淀用热水洗涤的目的是
(4)其他条件相同,向过滤1所得滤渣加入不同体积的去离子水,以一定流速通入CO2气体,测得热分解后电池级Li2CO3的产率随碳化反应固液比[
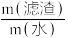 ]变化曲线如图2所示。Li2CO3产率随固液比减小而增加的原因是
]变化曲线如图2所示。Li2CO3产率随固液比减小而增加的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】工业上用钛铁矿[主要成分为 (钛酸亚铁),还含
(钛酸亚铁),还含 、
、 等杂质]制备
等杂质]制备 ,其流程如下:
,其流程如下:

已知:钛液Ⅰ和钛液Ⅱ中,Ti元素均主要以TiO2+的形式存在。
(1)钛铁矿中加硫酸后为了提高浸出率,可以采取的方法是_______ ;钛液中加入铁粉的目的是________ (用离子方程式表示)。
(2)检验钛液Ⅰ中含有Fe2+的方法是___________ 。
(3)①步骤Ⅱ需冷却至70℃左右,若温度过高会导致产品TiO2回收率降低,原因是___________ 。
②步骤Ⅲ得到了170g TiO2·xH2O,经煅烧后的质量为80g,则
__________ 。
③步骤Ⅲ需不断通入高温水蒸气以维持温度在90℃,请从化学平衡角度分析通入高温水蒸气的两个作用:___________ 、___________ 。
 (钛酸亚铁),还含
(钛酸亚铁),还含 、
、 等杂质]制备
等杂质]制备 ,其流程如下:
,其流程如下:
已知:钛液Ⅰ和钛液Ⅱ中,Ti元素均主要以TiO2+的形式存在。
(1)钛铁矿中加硫酸后为了提高浸出率,可以采取的方法是
(2)检验钛液Ⅰ中含有Fe2+的方法是
(3)①步骤Ⅱ需冷却至70℃左右,若温度过高会导致产品TiO2回收率降低,原因是
②步骤Ⅲ得到了170g TiO2·xH2O,经煅烧后的质量为80g,则

③步骤Ⅲ需不断通入高温水蒸气以维持温度在90℃,请从化学平衡角度分析通入高温水蒸气的两个作用:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一 《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二 公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
(1)某研究性学习小组用如图所示试验装置对绿矾的焙烧反应进行探究。

①实验过程中,装置A玻管中可观察到的实验现象是__ 。
②装置C的作用是__ 。
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入__ (填试剂名称),溶液呈红色,说明“矾精”中含有H+;检验“矾精”中含有SO42-的方法是__ 。
(2)某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160kg,计算理论上所需绿矾的质量,写出计算过程。___ 。
材料一 《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二 公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
(1)某研究性学习小组用如图所示试验装置对绿矾的焙烧反应进行探究。

①实验过程中,装置A玻管中可观察到的实验现象是
②装置C的作用是
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入
(2)某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160kg,计算理论上所需绿矾的质量,写出计算过程。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】硫酸铁铵[化学式可表示为NH4Fe(SO4)2]可用作分析试剂等。某兴趣小组利用铁矿石(主要成分为FeO、Fe2O3 )制硫酸铁铵的流程如下:
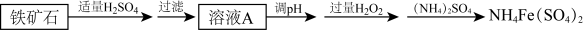
回答下列问题:
(1)溶液A中所含金属阳离子有___________ 。
(2)写出FeO与稀硫酸反应的离子方程式:___________ 。
(3)加入H2O2的作用是___________ 。
(4)若想探究NH4Fe(SO4)2与Ba(OH)2反应生成最大质量沉淀的条件,某同学向含a molNH4Fe(SO4)2的溶液中滴加含b mol Ba(OH)2的溶液,与OH-反应的顺序:先是Fe3+,后是NH ,当a=b时,发生的离子反应为
,当a=b时,发生的离子反应为___________ ,当b=1. 5a时,反应后溶液中NH 与SO
与SO 的浓度之比为
的浓度之比为___________ ,当___________ 时,沉淀的质量达到最大。
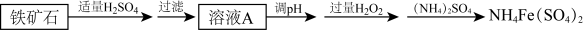
回答下列问题:
(1)溶液A中所含金属阳离子有
(2)写出FeO与稀硫酸反应的离子方程式:
(3)加入H2O2的作用是
(4)若想探究NH4Fe(SO4)2与Ba(OH)2反应生成最大质量沉淀的条件,某同学向含a molNH4Fe(SO4)2的溶液中滴加含b mol Ba(OH)2的溶液,与OH-反应的顺序:先是Fe3+,后是NH
 ,当a=b时,发生的离子反应为
,当a=b时,发生的离子反应为 与SO
与SO 的浓度之比为
的浓度之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】利用铜转炉烟灰(主要成分为ZnO,含少量 及Pb、Cu、As元素的化合物)制取活性氧化锌的工艺流程如下:
及Pb、Cu、As元素的化合物)制取活性氧化锌的工艺流程如下:
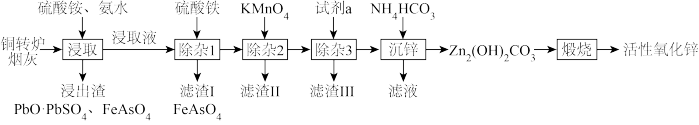
已知:“浸取”后,锌元素以 存在;25℃时,部分金属离子开始沉淀和完全沉淀的pH见下表(当溶液中某离子浓度
存在;25℃时,部分金属离子开始沉淀和完全沉淀的pH见下表(当溶液中某离子浓度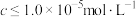 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
回答下列问题:
(1)“浸取”时控制温度为45~55℃之间,理由是________ 。
(2)“除杂2”中,需先将溶液的pH调至4~4.5,此时应选择的最佳试剂是______ (填标号);
A.氨水 B.氧化锌 C.硫酸 D.盐酸
滴加 溶液有
溶液有 生成,该反应的离子方程式为
生成,该反应的离子方程式为______ ;25℃时,体系中 残留最大浓度为
残留最大浓度为______  (忽略反应对溶液pH的影响)。
(忽略反应对溶液pH的影响)。
(3)“除杂3”是置换除杂过程,则试剂a是________ (填化学式);“沉锌”时,锌元素以 形式存在,发生反应的离子方程式为
形式存在,发生反应的离子方程式为________ 。
(4)该流程中可以循环使用的物质是_______ (填化学式)。
 及Pb、Cu、As元素的化合物)制取活性氧化锌的工艺流程如下:
及Pb、Cu、As元素的化合物)制取活性氧化锌的工艺流程如下:
已知:“浸取”后,锌元素以
 存在;25℃时,部分金属离子开始沉淀和完全沉淀的pH见下表(当溶液中某离子浓度
存在;25℃时,部分金属离子开始沉淀和完全沉淀的pH见下表(当溶液中某离子浓度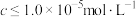 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。| 金属离子 |  |  |  |
| 开始沉淀pH | 1.9 | 7.0 | 4.5 |
| 完全沉淀pH | 3.2 | 9.0 | 6.4 |
(1)“浸取”时控制温度为45~55℃之间,理由是
(2)“除杂2”中,需先将溶液的pH调至4~4.5,此时应选择的最佳试剂是
A.氨水 B.氧化锌 C.硫酸 D.盐酸
滴加
 溶液有
溶液有 生成,该反应的离子方程式为
生成,该反应的离子方程式为 残留最大浓度为
残留最大浓度为 (忽略反应对溶液pH的影响)。
(忽略反应对溶液pH的影响)。(3)“除杂3”是置换除杂过程,则试剂a是
 形式存在,发生反应的离子方程式为
形式存在,发生反应的离子方程式为(4)该流程中可以循环使用的物质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】碘是人体必需的生命元素,对人类的生长发育起着重要作用。碘主要存在于海带、海水和盐矿中。从海带中提取碘的实验过程如图所示。
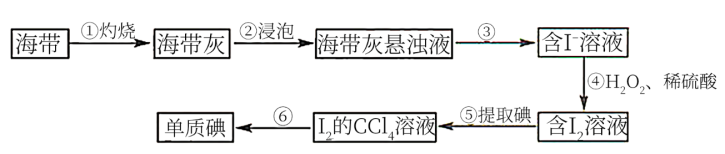
已知:① 的升华温度:45℃~77℃;②
的升华温度:45℃~77℃;② 沸点:76.8℃。回答下列问题:
沸点:76.8℃。回答下列问题:
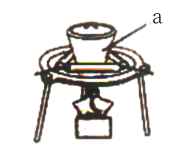
(1)步骤①灼烧海带,实验室通常在如图所示装置中进行,仪器a的名称为___________ 。
(2)步骤③涉及的操作名称为___________ ,实验室进行该操作时用到的玻璃仪器有___________ 。
(3)步骤④中涉及的主要反应的离子方程式为___________ 。
(4)海带灰中还含有其他可溶性无机盐类(硫酸盐、硝酸盐、碳酸盐等),这些盐类是在流程图中的第___________ 步(填编号)与碘分离,若要使碘尽可能地完全转移,应采取的操作是___________ 。
(5)步骤⑥将 与
与 分离可以采用
分离可以采用___________ (填“常压”或“减压”)蒸馏方法,原因是___________ 。
(6)若实验室称得海带的质量为m g,提取单质碘的过程中,碘损失了n%,最后得到单质碘b g,则海带中碘的百分含量为___________ (用含m、n、b的式子表示)

已知:①
 的升华温度:45℃~77℃;②
的升华温度:45℃~77℃;② 沸点:76.8℃。回答下列问题:
沸点:76.8℃。回答下列问题:(1)步骤①灼烧海带,实验室通常在如图所示装置中进行,仪器a的名称为

(2)步骤③涉及的操作名称为
(3)步骤④中涉及的主要反应的离子方程式为
(4)海带灰中还含有其他可溶性无机盐类(硫酸盐、硝酸盐、碳酸盐等),这些盐类是在流程图中的第
(5)步骤⑥将
 与
与 分离可以采用
分离可以采用(6)若实验室称得海带的质量为m g,提取单质碘的过程中,碘损失了n%,最后得到单质碘b g,则海带中碘的百分含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】锆产品的主要原料是锆英砂,全球90%的氧氯化锆(ZrOCl2)来源于中国。氧氯化锆可溶于水,微溶于盐酸,工业上以锆英砂(含91.5%ZrSiO4,杂质不与NaOH溶液反应)为原料生产ZrOCl2的一种工艺流程如图所示。
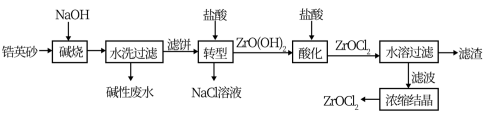
已知:碱金属的锆酸盐在水中溶解度很小,可在酸性条件下水解。
请回答下列问题:
(1)锆英砂在“碱烧”前粉碎的目的是____ ,“碱烧”时ZrSiO4生成了Na2ZrO3和另一种钠盐X,X的化学式为___ ,X的用途是___ (写一种)。
(2)“转型”时发生反应的化学方程式为___ 。
(3)“酸化”过程需加入过量盐酸,该操作中发生反应的化学方程式是___ 。
(4)“水溶过滤”操作后要对滤渣进行洗涤,洗涤液与滤液合并浓缩结晶,检查滤渣已经洗涤干净的实验是___ 。
(5)将锆英砂和焦炭混合,再与Cl2反应生成ZrCl4、SiCl4和一种可燃性气体,ZrCl4水解也可得到ZrOCl2。生成 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为___ 。
(6)某工厂用2t锆英砂来制备ZrOCl2,若这个过程中Zr的损耗率为15%,则最终制得ZrOCl2的质量为___ t。

已知:碱金属的锆酸盐在水中溶解度很小,可在酸性条件下水解。
请回答下列问题:
(1)锆英砂在“碱烧”前粉碎的目的是
(2)“转型”时发生反应的化学方程式为
(3)“酸化”过程需加入过量盐酸,该操作中发生反应的化学方程式是
(4)“水溶过滤”操作后要对滤渣进行洗涤,洗涤液与滤液合并浓缩结晶,检查滤渣已经洗涤干净的实验是
(5)将锆英砂和焦炭混合,再与Cl2反应生成ZrCl4、SiCl4和一种可燃性气体,ZrCl4水解也可得到ZrOCl2。生成
 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为(6)某工厂用2t锆英砂来制备ZrOCl2,若这个过程中Zr的损耗率为15%,则最终制得ZrOCl2的质量为
您最近一年使用:0次



