某种含二价铜微粒[CuII(OH)(NH3)]+的催化剂可用于汽车尾气脱硝,催化机理如图所示,下列说法正确的是
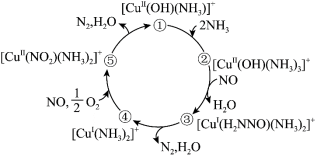

| A.[CuII(OH)(NH3)]+可降低该反应的活化能 |
| B.状态②到状态③的过程中N元素被还原 |
| C.状态③到状态④的过程中有O-H键的断裂 |
D.该脱硝过程的总反应方程式为 |
23-24高二上·湖北荆州·期末 查看更多[2]
更新时间:2024-02-28 09:37:45
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】氧化还原反应的本质是电子转移,下列氧化还原反应中电子转移的表示方法正确的是
A.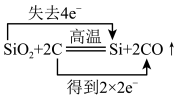 |
B.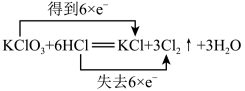 |
C.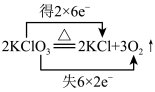 |
D.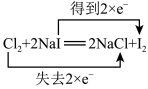 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列关于氧化还原反应的说法中错误的是
| A.氧化还原反应的实质是电子的转移 |
| B.氧化还原反应中一定存在元素化合价的变化 |
| C.氧化还原反应一定有氧元素参加 |
| D.发生氧化反应的物质也可能同时发生还原反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是
| A.活化分子间所发生的碰撞即为有效碰撞 |
| B.能够发生有效碰撞的分子叫做活化分子,活化分子具有的平均能量叫活化能 |
| C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |
| D.升高温度能使化学反应速率增大,是因为增加了反应物中活化分子的百分数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】对于反应 科学家根据光谱学研究提出如下反应历程:
科学家根据光谱学研究提出如下反应历程:
第一步: 快速平衡
快速平衡
第二步: 慢反应
慢反应
第三步: 快反应
快反应
其中可近似认为第二步反应不影响第一步的平衡。下列叙述不正确的是
 科学家根据光谱学研究提出如下反应历程:
科学家根据光谱学研究提出如下反应历程:第一步:
 快速平衡
快速平衡第二步:
 慢反应
慢反应第三步:
 快反应
快反应其中可近似认为第二步反应不影响第一步的平衡。下列叙述不正确的是
A. 与 与 是总反应的催化剂 是总反应的催化剂 |
| B.v(第一步的逆反应)>v(第二步反应) |
| C.总反应快慢主要由第二步反应决定 |
D.选择合适的催化剂能提高单位时间内 的产率 的产率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】对于双氧水的分解,下列说法正确的是
| A.增大H2O2浓度,可增大单位体积内活化分子百分数,从而使有效碰撞次数增大 |
| B.使用催化剂反应速率加快是因为正反应速率比逆反应速率快 |
| C.催化剂不影响活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
| D.升高温度能使反应速率增大,主要原因是增大了反应物分子中活化分子的百分数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】某实验小组以H2O2分解为例,研究浓度、催化剂对反应速率的影响。在常温下按照如下方案完成实验。实验②的反应物应为
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 无 | |
| ③ | 10 mL 5% H2O2溶液 | MnO2固体 |
| A.5 mL 2% H2O2溶液 | B.10 mL 2% H2O2溶液 |
| C.10 mL 5% H2O2溶液 | D.5 mL 10% H2O2溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】类比推理是化学中常用的思维方法,下列“类比”结果正确的是
A. 由于键能大而结构稳定,则 由于键能大而结构稳定,则 键能也大结构也很稳定 键能也大结构也很稳定 |
B. 为含极性键的非极性分子,则 为含极性键的非极性分子,则 也是含极性键的非极性分子 也是含极性键的非极性分子 |
C. 可以溶解在浓氨水中,则 可以溶解在浓氨水中,则 也可以溶解在浓氨水中 也可以溶解在浓氨水中 |
D. 的空间构型为正四面体型,则 的空间构型为正四面体型,则 碳骨架的空间构型也为正四面体型 碳骨架的空间构型也为正四面体型 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】向盛有天蓝色CuSO4水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是( )
| A.反应后溶液中不存在任何沉淀,所以反应前后溶质成分不变 |
| B.溶液呈天蓝色是因为存在[Cu(H2O)4]2+,该离子的空间构型为正四面体 |
| C.深蓝色的配离子为[Cu(NH3)4]2+,说明[Cu(NH3)4]2+比[Cu(H2O)4]2+稳定 |
| D.若向反应后的溶液加入乙醇,将会有[Cu(H2O)4]SO4晶体析出 |
您最近一年使用:0次

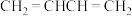 与H2按1∶1发生加成反应可得
与H2按1∶1发生加成反应可得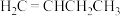 和
和 两种产物,其能量与反应进程如图所示:
两种产物,其能量与反应进程如图所示: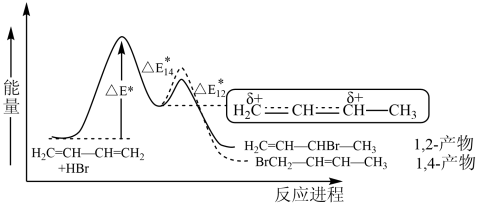
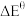 的值
的值



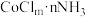 ,若1mol该配合物与足量
,若1mol该配合物与足量 溶液作用生成1molAgCl沉淀,则m、n的值是
溶液作用生成1molAgCl沉淀,则m、n的值是

