一定条件下,水气变换反应CO+H2O⇌CO2+H2的中间产物是HCOOH。为探究该反应过程,研究 水溶液在密封石英管中的分子反应:
水溶液在密封石英管中的分子反应:
I.HCOOH⇌CO+H2O (快)
Ⅱ.HCOOH⇌CO2+H2 (慢)
(1) 温度下,在密封石英管内完全充满1.0mol·L-1HCOOH水溶液,使
温度下,在密封石英管内完全充满1.0mol·L-1HCOOH水溶液,使 分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。 时刻测得CO、CO2的浓度分别为0.70mol·L-1、0.16mol·L-1,反应Ⅱ达平衡时,测得H2的浓度为ymol·L-1。体系达平衡后
时刻测得CO、CO2的浓度分别为0.70mol·L-1、0.16mol·L-1,反应Ⅱ达平衡时,测得H2的浓度为ymol·L-1。体系达平衡后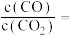
_______ (用含y的代数式表示,下同),反应Ⅱ的平衡常数为_______ 。
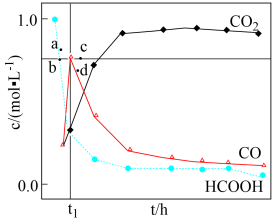
(2)相同条件下,若反应起始时溶液中同时还含有0.10mol·L-1盐酸,则图示点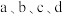 中,CO的浓度峰值点可能是
中,CO的浓度峰值点可能是_______ (填标号)。与不同盐酸相比,CO达浓度峰值时,CO2浓度_______ (填“增大”“减小”或“不变”), 的反应
的反应_______ (填“增大”“减小”或“不变”)。
 水溶液在密封石英管中的分子反应:
水溶液在密封石英管中的分子反应:I.HCOOH⇌CO+H2O (快)
Ⅱ.HCOOH⇌CO2+H2 (慢)
(1)
 温度下,在密封石英管内完全充满1.0mol·L-1HCOOH水溶液,使
温度下,在密封石英管内完全充满1.0mol·L-1HCOOH水溶液,使 分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。 时刻测得CO、CO2的浓度分别为0.70mol·L-1、0.16mol·L-1,反应Ⅱ达平衡时,测得H2的浓度为ymol·L-1。体系达平衡后
时刻测得CO、CO2的浓度分别为0.70mol·L-1、0.16mol·L-1,反应Ⅱ达平衡时,测得H2的浓度为ymol·L-1。体系达平衡后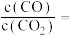

(2)相同条件下,若反应起始时溶液中同时还含有0.10mol·L-1盐酸,则图示点
 中,CO的浓度峰值点可能是
中,CO的浓度峰值点可能是 的反应
的反应
2024高三下·全国·专题练习 查看更多[1]
(已下线)题型四 平衡图像原因解释-备战2024年高考化学答题技巧与模板构建
更新时间:2024-03-01 09:32:39
|
相似题推荐
【推荐1】氨气是一种重要的化工原料,在工农业生产中有广泛的应用。
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:CO+2H2 CH3OH(g)。该可逆反应达到平衡的标志是
CH3OH(g)。该可逆反应达到平衡的标志是________ 。
A.2 v正(H2)= v逆(CH3OH)
B.单位时间生成m molCO的同时生成2m molH2
C.容器内气体的平均相对分子质量不再随时间而变化
D.混合气体的密度不再随时间变化
(2)工业上可用天然气为原料来制取化工原料气氢气,某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,体积为2L的恒容密闭容器中,测得如下表所示数据。
请回答下列问题:
①该温度下,上述反应的平衡常数K=________ ;
②反应在7~10 min内,CO的物质的量减少的原因可能是____________ (填字母)。
A.减少CH4的物质的量 B.降低温度
C.升高温度 D.充入H2
③若保持相同的温度,向2L的恒容器密闭容器中同时充入0.2molCH4、0.62molH2O、a molCO和0.5molH2,当a =0.2时,上述反应向_____ (填“正反应”或“逆反应”)方向进行。若要使上述反应开始时向逆反应方向进行,则a的取值范围为__________ 。
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:CO+2H2
 CH3OH(g)。该可逆反应达到平衡的标志是
CH3OH(g)。该可逆反应达到平衡的标志是A.2 v正(H2)= v逆(CH3OH)
B.单位时间生成m molCO的同时生成2m molH2
C.容器内气体的平均相对分子质量不再随时间而变化
D.混合气体的密度不再随时间变化
(2)工业上可用天然气为原料来制取化工原料气氢气,某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,体积为2L的恒容密闭容器中,测得如下表所示数据。
| 时间/min | CH4(mol) | H2O(mol) | CO(mol) | H2(mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | a | 0.80 | c | 0.60 |
| 7 | 0.20 | b | 0.20 | d |
| 10 | 0.21 | 0.81 | 0.19 | 0.64 |
①该温度下,上述反应的平衡常数K=
②反应在7~10 min内,CO的物质的量减少的原因可能是
A.减少CH4的物质的量 B.降低温度
C.升高温度 D.充入H2
③若保持相同的温度,向2L的恒容器密闭容器中同时充入0.2molCH4、0.62molH2O、a molCO和0.5molH2,当a =0.2时,上述反应向
您最近一年使用:0次
【推荐2】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
2NO(g)+Cl2(g) 2NOCl(g) K2 ΔH2<0 (Ⅱ)
2NOCl(g) K2 ΔH2<0 (Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________ (用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(NOCl)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=________ mol,NO的转化率α1=________ 。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2________ α1(填“>”“<”或“=”),平衡常数K2________ (填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是____________ 。
2NO2(g)+NaCl(s)
 NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)2NO(g)+Cl2(g)
 2NOCl(g) K2 ΔH2<0 (Ⅱ)
2NOCl(g) K2 ΔH2<0 (Ⅱ)(1)4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(NOCl)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】一定温度下,有容积相等的甲、乙两个容器中,甲容器中加入0.1mol A和0.2mol B,乙容器中加入0.2mol A和0.2 mol B,两容器中均发生反应:A(s)+2B(g) ⇌2C(g)+D(g)。
(1)甲容器与乙容器中,平衡常数(K):甲__________ 乙(填 “>”、“=” 或“<”,下同),物质B的转化率:甲___________ 乙。
(2)如果甲的容积为2L,分别在三种不同实验条件下进行反应,反应物B的浓度随时间的变化如图所示。
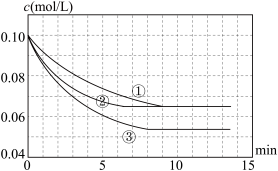
a.实验②,0~4 min 平均反应速度率:v(D)=_____________________ 。
b.与实验①相比,实验②和③分别改变了一种反应条件。请分析判断并填写下表:
(3)该反应为________ 反应(填“放热”或“吸热”)。
(4)不能说明该反应已达到平衡状态的是_______________
A.v正(B)= 2v逆(D) B. A的浓度保持不变
C.气体的平均摩尔质量不变 D.气体的密度保持不变
(1)甲容器与乙容器中,平衡常数(K):甲
(2)如果甲的容积为2L,分别在三种不同实验条件下进行反应,反应物B的浓度随时间的变化如图所示。

a.实验②,0~4 min 平均反应速度率:v(D)=
b.与实验①相比,实验②和③分别改变了一种反应条件。请分析判断并填写下表:
| 实验 | 改变条件 | 判断理由 |
| ② | ||
| ③ |
(3)该反应为
(4)不能说明该反应已达到平衡状态的是
A.v正(B)= 2v逆(D) B. A的浓度保持不变
C.气体的平均摩尔质量不变 D.气体的密度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】勒夏特列通过深入研究高炉炼铁后发现了该过程的主要反应为可逆反应。某科研小组进行类似的研究,以Fe3O4为原料炼铁,主要发生如下反应:
反应I:Fe3O4(s)+CO(g)⇌3FeO(s)+CO2(g) △H1=Q1(Q1>0)
反应II:Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g) △H2=Q2
将一定体积CO通入装有Fe3O4粉末的反应器,其它条件不变,反应达平衡,测得CO的体积分数随温度的变化关系如图所示。

回答下列问题:
(1)判断Q2的正、负值,并说明理由___________ 。
(2)温度升高,反应器中CO体积分数降低,分析可能的原因为___________ 。
(3)1040℃时,反应一段时间后,体系内2个反应均达成平衡,试计算各自的平衡常数Kp___________ 。
(4)炉温不变,扩大炼铁反应器的容积,通过分析说明等量的还原剂能否提升铁矿石的平衡转化率___________ ,能否提升平衡前铁矿石的单位时间转化率___________ 。
(5)将Fe2O3、铁粉和NaOH溶液置于反应器中,在温度大于100℃下搅拌反应半小时以上,反应产物经过一次过滤、水洗、二次过滤、干燥、研磨,可直接得到黑色的Fe3O4细末。试写出该过程的总反应方程式___________ 。
反应I:Fe3O4(s)+CO(g)⇌3FeO(s)+CO2(g) △H1=Q1(Q1>0)
反应II:Fe3O4(s)+4CO(g)⇌3Fe(s)+4CO2(g) △H2=Q2
将一定体积CO通入装有Fe3O4粉末的反应器,其它条件不变,反应达平衡,测得CO的体积分数随温度的变化关系如图所示。

回答下列问题:
(1)判断Q2的正、负值,并说明理由
(2)温度升高,反应器中CO体积分数降低,分析可能的原因为
(3)1040℃时,反应一段时间后,体系内2个反应均达成平衡,试计算各自的平衡常数Kp
(4)炉温不变,扩大炼铁反应器的容积,通过分析说明等量的还原剂能否提升铁矿石的平衡转化率
(5)将Fe2O3、铁粉和NaOH溶液置于反应器中,在温度大于100℃下搅拌反应半小时以上,反应产物经过一次过滤、水洗、二次过滤、干燥、研磨,可直接得到黑色的Fe3O4细末。试写出该过程的总反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。回答下列问题:
(1) CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C2H4):n(H2O)=_______ 。当反应达到平衡时,若增大压强,则n(C2H4)_______ (填“变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成n(CO2):n(H2O)=1:3,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
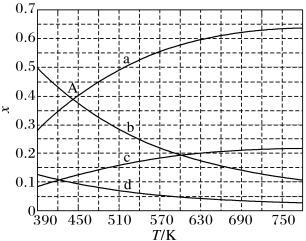
图中,表示C2H4、CO2变化的曲线分别是_______ 、_______ 。CO2催化加氢合成C2H4反应的△H_______ 0(填“大于”或“小于”)。
(3)根据图中点A(440,0.39),计算该温度时反应的平衡常数Kp=_______ (MPa)-3 (列出计算式。以分压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H4、C3H5、C4H3等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当_______ 。
(1) CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C2H4):n(H2O)=
(2)理论计算表明,原料初始组成n(CO2):n(H2O)=1:3,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。

图中,表示C2H4、CO2变化的曲线分别是
(3)根据图中点A(440,0.39),计算该温度时反应的平衡常数Kp=
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H4、C3H5、C4H3等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】高炉炼铁过程中发生的主要反应为:
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:

请回答下列问题:
(1)该反应的平衡常数表达式K=_________ ,ΔH______ 0(填“>”、“<”或“=”);
(2)在一个容积为10 L的密闭容器中,1 000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。求该时间范围内反应的平衡反应速率v(CO2)=_________ 、CO的平衡转化率=___________ 。
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g)
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:

请回答下列问题:
(1)该反应的平衡常数表达式K=
(2)在一个容积为10 L的密闭容器中,1 000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。求该时间范围内反应的平衡反应速率v(CO2)=
您最近一年使用:0次



