常温下, 在水中的沉淀溶解平衡曲线如图所示,已知常温下
在水中的沉淀溶解平衡曲线如图所示,已知常温下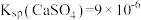 。下列说法正确的是
。下列说法正确的是
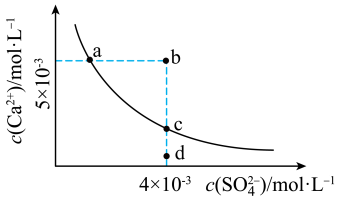
 在水中的沉淀溶解平衡曲线如图所示,已知常温下
在水中的沉淀溶解平衡曲线如图所示,已知常温下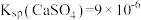 。下列说法正确的是
。下列说法正确的是
| A.升高温度曲线会往右上方移动 |
B.d点表示 的过饱和溶液,b点表示 的过饱和溶液,b点表示 的不饱和溶液 的不饱和溶液 |
C.b点加水可以变到如图的曲线上,且此时的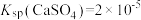 |
D.加入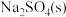 ,可以使溶液由c点变到a点 ,可以使溶液由c点变到a点 |
更新时间:2024-03-02 14:20:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是
| A.25℃时 Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度 |
| B.常温下,NaClO溶液显碱性的原因:ClO-+ H2O =HClO+OH- |
| C.2NO(g) + 2CO(g) = N2(g) + 2CO2(g),在常温下能自发进行,则该反应的△H >0 |
| D.25℃时向水中加入少量NaOH后,由水电离出的c(H+)•c(OH-)不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16.下列叙述正确的是
| A.饱和AgCl、AgI溶液中所含Ag+的浓度相同 |
| B.向饱和AgCl溶液中加入盐酸,Ksp大 |
| C.向AgCl的悬浊液中加入KI溶液,白色沉淀转化为黄色 |
| D.向含相同物质的量浓度的Cl-和I-的溶液中逐滴加入AgNO3溶液,Cl-先沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,难溶强电解质的饱和溶液中存在着沉淀溶解平衡,其平衡常数如下:
对于1L含 、
、 和
和 各
各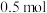 的混合溶液,根据表中数据判断,下列说法错误的是
的混合溶液,根据表中数据判断,下列说法错误的是
| 物质 |  |  |  |
 | 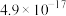 | 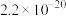 |  |
 、
、 和
和 各
各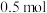 的混合溶液,根据表中数据判断,下列说法错误的是
的混合溶液,根据表中数据判断,下列说法错误的是A.向混合溶液中逐滴加入 溶液,最先看到红褐色沉淀 溶液,最先看到红褐色沉淀 |
B.向溶液中加入双氧水,并用 粉末调节 粉末调节 ,过滤后可获得较纯净的 ,过滤后可获得较纯净的 溶液 溶液 |
C.该溶液中 |
D.将少量 粉末加入 粉末加入 悬浊液中, 悬浊液中, 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验的现象与结论相对应的是
| A | B | C | D | |
| 实验 |  |  | 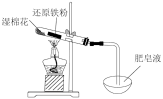 |  |
| 现象 | 电流计指针向右偏(电子由Fe转移到Cu),片刻后向左偏 | 产生黑色沉淀 | 加热,肥皂液中产生无色气体泡 | 高锰酸钾溶液褪色 |
| 结论 | 铁片作负极,片刻后铜片作负极 | Ksp(CuS)<Ksp(ZnS) | 铁粉与水蒸气反应生成H2 | 乙醇发生消去反应生成了乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
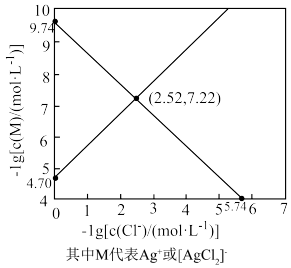
【推荐1】向AgNO3溶液中滴加NaCl溶液发生反应Ag+(aq)+Cl-(aq) AgCl(s)和AgCl(s)+Cl-(aq)
AgCl(s)和AgCl(s)+Cl-(aq) [AgCl2]-(aq);-lgc[(M)/(mol•L-1)]与-lgc[(Cl-)/(mol•L-1)]的关系如图所示(其中M代表Ag+或[AgCl2]-)。下列说法不正确的是
[AgCl2]-(aq);-lgc[(M)/(mol•L-1)]与-lgc[(Cl-)/(mol•L-1)]的关系如图所示(其中M代表Ag+或[AgCl2]-)。下列说法不正确的是
 AgCl(s)和AgCl(s)+Cl-(aq)
AgCl(s)和AgCl(s)+Cl-(aq) [AgCl2]-(aq);-lgc[(M)/(mol•L-1)]与-lgc[(Cl-)/(mol•L-1)]的关系如图所示(其中M代表Ag+或[AgCl2]-)。下列说法不正确的是
[AgCl2]-(aq);-lgc[(M)/(mol•L-1)]与-lgc[(Cl-)/(mol•L-1)]的关系如图所示(其中M代表Ag+或[AgCl2]-)。下列说法不正确的是
A.c(Cl-)=10-2.52mol•L-1时,溶液中c(NO )>2c([AgCl2]-) )>2c([AgCl2]-) |
B.c(Cl-)=10-3mol•L-1时,溶液中c(NO )>c(Ag+)>c([AgCl2]-) )>c(Ag+)>c([AgCl2]-) |
C.反应Ag++2Cl-(aq) [AgCl2]-(aq)的平衡常数K=105.04 [AgCl2]-(aq)的平衡常数K=105.04 |
| D.用Ag+滴定NaCl溶液测定Cl-浓度时,当Cl-浓度降至10-5mol•L-1时,溶液中的Ag+浓度为10-4.74mol•L-1 |
您最近一年使用:0次
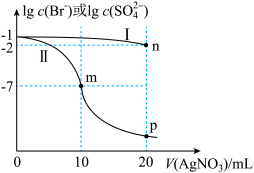
【推荐2】某温度下,分别向10mL浓度均为 的NaBr溶液和
的NaBr溶液和 溶液中滴加0.1
溶液中滴加0.1 的
的 溶液,滴加过程中
溶液,滴加过程中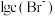 或
或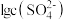 随加入
随加入 溶液体积的变化如图所示。下列说法错误的是
溶液体积的变化如图所示。下列说法错误的是
 的NaBr溶液和
的NaBr溶液和 溶液中滴加0.1
溶液中滴加0.1 的
的 溶液,滴加过程中
溶液,滴加过程中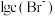 或
或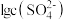 随加入
随加入 溶液体积的变化如图所示。下列说法错误的是
溶液体积的变化如图所示。下列说法错误的是
A.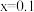 |
B.该温度下,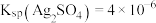 |
C.m、n、p三点溶液中 :p>n>m :p>n>m |
| D.其他条件不变,若将NaBr溶液的浓度减小为原来的一半,则此时m点坐标为(5,-3.5) |
您最近一年使用:0次

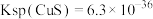 ,
, ,随着温度的升高两者的Ksp都增大。298K时,饱和溶液中
,随着温度的升高两者的Ksp都增大。298K时,饱和溶液中 和
和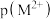 的关系如图所示,其中
的关系如图所示,其中 ,
,
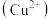 或
或 ,下列说法正确的是
,下列说法正确的是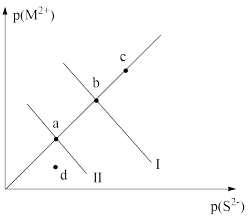
 固体,可使溶液由a点变为d点
固体,可使溶液由a点变为d点 溶液中混有的少量
溶液中混有的少量 ,可加入适量
,可加入适量 固体,充分搅拌后过滤
固体,充分搅拌后过滤 ,平衡常数K约为
,平衡常数K约为
 和黄色的
和黄色的 。常温下,
。常温下,
 为
为 数量级为
数量级为
 转化为
转化为 较由
较由


