含铜物质在生产生活中有着广泛应用。回答下列问题:
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为_______ ;基态 较基态
较基态 更稳定的原因是
更稳定的原因是_______ 。
(2) 稀溶液中存在
稀溶液中存在 ,
, 的空间构型为八面体形:下列对
的空间构型为八面体形:下列对 中
中 杂化方式推断合理的是_______(填标号)。
杂化方式推断合理的是_______(填标号)。
(3) 可形成
可形成 ,其中en代表
,其中en代表 。1mol该配合物中,VSEPR模型为四面体的非金属原子共有
。1mol该配合物中,VSEPR模型为四面体的非金属原子共有_______ 个;C、N、F的电负性由大到小的顺序为_______ 。
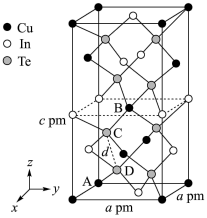
(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为_______ ;该晶体的化学式为_______ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点,B点原子的分数坐标分别为(0,0,0)、 ,则C点原子的分数坐标为
,则C点原子的分数坐标为_______ ,晶胞中C、D间距离
_______ pm。
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。原子中电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为 较基态
较基态 更稳定的原因是
更稳定的原因是(2)
 稀溶液中存在
稀溶液中存在 ,
, 的空间构型为八面体形:下列对
的空间构型为八面体形:下列对 中
中 杂化方式推断合理的是_______(填标号)。
杂化方式推断合理的是_______(填标号)。A. | B. | C.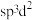 | D. |
(3)
 可形成
可形成 ,其中en代表
,其中en代表 。1mol该配合物中,VSEPR模型为四面体的非金属原子共有
。1mol该配合物中,VSEPR模型为四面体的非金属原子共有(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为
 ,则C点原子的分数坐标为
,则C点原子的分数坐标为

2024·四川成都·二模 查看更多[3]
2024届四川省成都市第七中学高三下学期二模诊断考试理综试题-高中化学(已下线) 2024届四川省成都市第七中学高三下学期二诊模拟考试理综试卷-高中化学2024届四川省仁寿第一中学校(北校区)二模理综试题-高中化学
更新时间:2024-04-04 03:40:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请根据所学知识回答下列问题:
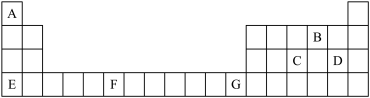
(1)B、C、D三种元素的电负性由大到小的顺序是_______ (用元素符号表示)。A与B、D分别形成的最简单化合物的沸点由大到小的顺序是_______ (填化学式),原因为_______ 。
(2)上述元素的原子中,未成对电子数量多的是_______ (填元素符号),写出该元素基态原子的核外电子排布式:_______ 。
(3)上述7种元素中金属性最强的为_______ (填名称)。该元素与B可形成原子个数比为1∶1的化合物甲,则甲的电子式为_______ ,其中所含的化学键类型为_______ 。

(1)B、C、D三种元素的电负性由大到小的顺序是
(2)上述元素的原子中,未成对电子数量多的是
(3)上述7种元素中金属性最强的为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)在周期表中,与元素b的化学性质最相似的邻族元素是________ (填写以上表中字母对应的元素符号),该元素基态原子核外M层电子的自旋状态________ (填“相同”或“相反”)。
(2)元素As与________ 同族(填写以上表中字母对应的元素符号),其简单气态氢化物的稳定性由大到小的顺序是________ 。
(3)基态ρ原子成为阳离子时首先失去________ 轨道电子,基态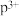 的最外层电子排布式
的最外层电子排布式________ 。
(4)i的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式为________________ 。
(5)下列关于上图表中元素说法正确的是________ (填序号)。
①未成对电子数最多的元素是O
②元素的电负性强弱;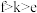
③元素的第一电离能:
④简单离子半径: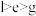
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p |
(2)元素As与
(3)基态ρ原子成为阳离子时首先失去
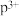 的最外层电子排布式
的最外层电子排布式(4)i的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式为
(5)下列关于上图表中元素说法正确的是
①未成对电子数最多的元素是O
②元素的电负性强弱;
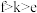
③元素的第一电离能:

④简单离子半径:
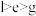
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为___________ ;第一电离能I1(Si)___________ I1(Ge)(填“>”或“<”)。
(2)基态Ge原子价电子排布式为___________ ;SiO2、GeO2具有类似的晶体结构,SiO2熔点较高,其原因是___________
(3)如图为硼酸晶体的片层结构,其中硼原子的杂化方式为___________ 。该晶体中存在的作用力有___________ 。
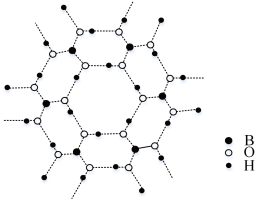
A.共价键B.离子键C.氢键
(4)Fe和Cu可分别与氧元素形成低价态氧化物FeO和Cu2O。
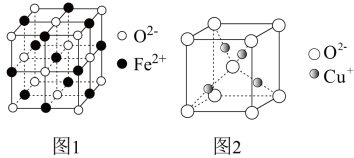
①FeO立方晶胞结构如图1所示,则Fe2+的配位数为___________ 。
②Cu2O立方晶胞结构如图2所示,若晶胞边长为acm,则该晶体的密度为___________ g·cm-3。(用含a、NA的代数式表示,NA代表阿伏加 德罗常数)
(1)C、O、Si三种元素电负性由大到小的顺序为
(2)基态Ge原子价电子排布式为
(3)如图为硼酸晶体的片层结构,其中硼原子的杂化方式为

A.共价键B.离子键C.氢键
(4)Fe和Cu可分别与氧元素形成低价态氧化物FeO和Cu2O。

①FeO立方晶胞结构如图1所示,则Fe2+的配位数为
②Cu2O立方晶胞结构如图2所示,若晶胞边长为acm,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硒可防止人体因氧化而引起的衰老、组织硬化。回答下列问题:
(1)写出基态硒(Se)原子的价电子排布式____________ ;其中未成对电子数为_________ ;
(2)砷(As)和硒(Se)的第一电离能较大的是__________________ ;
(3)SeF2的立体构型为______________ ,Se原子的杂化方式为____________________ ;
(4)H2Se和H2O的熔沸点较高的是_________ ,原因是___________________________ ;

(5)Se和Zn组成的某种晶胞如图所示,则该晶体的化学式为________________ ,若已知该晶胞的密度为ρg/cm3,则该晶胞的棱长a=_______ cm。
(1)写出基态硒(Se)原子的价电子排布式
(2)砷(As)和硒(Se)的第一电离能较大的是
(3)SeF2的立体构型为
(4)H2Se和H2O的熔沸点较高的是

(5)Se和Zn组成的某种晶胞如图所示,则该晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、B、C、D、E、F、G是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如下表所示:
回答下列问题:
(1)G元素位于第___________ 族___________ 区。
(2) 的电子排布式为
的电子排布式为___________ 。
(3)F元素基态原子的最高能级具有的原子轨道数为___________ ,该原子轨道呈___________ 形。
(4)F的最高价氧化物中心原子的价层电子对数___________ ,写出一种与其是等电子体的阴离子的化学式___________ 。
(5)A、B、C氢化物的稳定性由强到弱顺序___________ (用氢化物分子式表示)。A、B氨化物的键角A大于B的原因___________ 。
(6)B、D形成的化合物能与水反应,化学方程式为___________ 。
(7)D、E元素第一电离能大小比较为:___________ (用元素符号表示),原因是___________ 。
| 元素代号 | 相关信息 |
| A | 原子核外有6种运动状态不同的电子 |
| B | 基态原子的最外层为3个未成对电子 |
| C | 电负性为4.0 |
| D | 其第一至第四电离能分别是: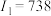 kJ/mol, kJ/mol, kJ/mol, kJ/mol,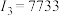 kJ/mol, kJ/mol,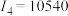 kJ/mol kJ/mol |
| E | 价电子数等于其电子层数 |
| F | 基态原子的价层电子排布式为 |
| G | 基态原子核外有7个能级上有电子,且能量最高的能级上有6个电子 |
(1)G元素位于第
(2)
 的电子排布式为
的电子排布式为(3)F元素基态原子的最高能级具有的原子轨道数为
(4)F的最高价氧化物中心原子的价层电子对数
(5)A、B、C氢化物的稳定性由强到弱顺序
(6)B、D形成的化合物能与水反应,化学方程式为
(7)D、E元素第一电离能大小比较为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】氨、磷、砷、铁等元素及其化合物在现代农业、科技和国防建设中有着许多独特的用途。
(一)如 ,是新型锂离子电池的电极材料,可采用
,是新型锂离子电池的电极材料,可采用 、
、 、LiC1和苯胺等作为原料制备。
、LiC1和苯胺等作为原料制备。
(1)基态铁原子的价电子排布式为___________ , 中,除氢元素外,其余三种元素第一电离能最大的是
中,除氢元素外,其余三种元素第一电离能最大的是___________ (填元素符号)。
(2) 的熔点为306℃,沸点为315℃,
的熔点为306℃,沸点为315℃, 的晶体类型是
的晶体类型是___________ 。
(3)苯胺(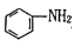 )和
)和 中的N原子杂化方式分别为
中的N原子杂化方式分别为___________ 、___________ 。
(4)苯胺和甲苯相对分子质量接近,但苯胺熔点比甲苯的高,原因是___________ 。
(二)。氮、磷、砷、锑等第ⅤA族元素及其化合物在生产、生活中用途广泛。
(5)白磷在氯气中燃烧可得到 和
和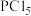 ,气态
,气态 分子的立体构型为
分子的立体构型为___________ 。
(6)锑酸亚铁晶胞如图所示,其晶胞参数分别为a nm、b nm、c nm, ,
,
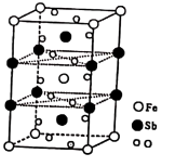
①锑酸亚铁的化学式为___________ 。
②晶体的密度为___________  (设
(设 为阿伏加德罗常数的值)。(1nm=10-7cm)
为阿伏加德罗常数的值)。(1nm=10-7cm)
(一)如
 ,是新型锂离子电池的电极材料,可采用
,是新型锂离子电池的电极材料,可采用 、
、 、LiC1和苯胺等作为原料制备。
、LiC1和苯胺等作为原料制备。(1)基态铁原子的价电子排布式为
 中,除氢元素外,其余三种元素第一电离能最大的是
中,除氢元素外,其余三种元素第一电离能最大的是(2)
 的熔点为306℃,沸点为315℃,
的熔点为306℃,沸点为315℃, 的晶体类型是
的晶体类型是(3)苯胺(
 )和
)和 中的N原子杂化方式分别为
中的N原子杂化方式分别为(4)苯胺和甲苯相对分子质量接近,但苯胺熔点比甲苯的高,原因是
(二)。氮、磷、砷、锑等第ⅤA族元素及其化合物在生产、生活中用途广泛。
(5)白磷在氯气中燃烧可得到
 和
和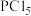 ,气态
,气态 分子的立体构型为
分子的立体构型为(6)锑酸亚铁晶胞如图所示,其晶胞参数分别为a nm、b nm、c nm,
 ,
,
①锑酸亚铁的化学式为
②晶体的密度为
 (设
(设 为阿伏加德罗常数的值)。(1nm=10-7cm)
为阿伏加德罗常数的值)。(1nm=10-7cm)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】【化学——选修3:物质结构与性质】
(1)含碳物质不完全燃烧会产生CO。血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒,写出铁离子(Fe3+)的核外电子排布式为_______________________ ,CO有多种等电子体,其中常见的一种分子是________ 。利用CO可以合成化工原料COCl2、配合物Fe(CO)5等,已知一个COCl2分子中每个原子最外层都形成8电子的稳定结构,则一个COCl2分子内含有_____ 个δ键,C原子的杂化方式为______ 。Fe(CO)5等在一定条件下分解生成CO和铁,反应过程中断裂的化学键是____________ ,形成的化学键是_______________ 。
(2)A、B均为短周期金属元素。依据下表数据,回答问题:
写出A原子的电子排布图__________________ ,Al原子的第一电离能______ 填:“大于”、“小于”或“等于”)738 kJ·mol-1,原因是________________________ 。
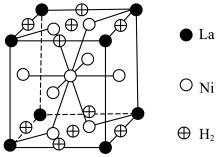
(3)下图是一种镍(Ni)镧(La)合金储氢后的晶胞结构图。该合金储氢后,含0.5mol Ni的合金可吸附氢气的体积(标况)为_______ 。
(1)含碳物质不完全燃烧会产生CO。血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒,写出铁离子(Fe3+)的核外电子排布式为
(2)A、B均为短周期金属元素。依据下表数据,回答问题:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(3)下图是一种镍(Ni)镧(La)合金储氢后的晶胞结构图。该合金储氢后,含0.5mol Ni的合金可吸附氢气的体积(标况)为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】[Cu(NH3)4]SO4是一 种深蓝色的配位化合物。
(1)Cu2+可被还原成Cu+,Cu+基态核外的外围电子排布式为_________________________ 。
(2)H元素与N元素可形成分子式为N2H2的化合物,该物质的分子具有平面结构,则该分子中N原子的杂化轨道类型为______________________ 。
(3)与CS2分子互为等电子体的SCN-离子的电子式为_________________ 。
(4) Cu可形成多种配合物,且各种配合物有广乏的用途。某Cu的配合物结构如图1所示,则该配合物中心原子Cu的配体数为____ ; 其分子内含有的作用力有________ (填序号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键


(5)Cu元素与S元素形成的一种化合物品跑如图2所示,其中S的配位数为______________ 。
(1)Cu2+可被还原成Cu+,Cu+基态核外的外围电子排布式为
(2)H元素与N元素可形成分子式为N2H2的化合物,该物质的分子具有平面结构,则该分子中N原子的杂化轨道类型为
(3)与CS2分子互为等电子体的SCN-离子的电子式为
(4) Cu可形成多种配合物,且各种配合物有广乏的用途。某Cu的配合物结构如图1所示,则该配合物中心原子Cu的配体数为
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键


(5)Cu元素与S元素形成的一种化合物品跑如图2所示,其中S的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】艾姆斯实验室已制造出包含钙、钾、铁和砷以及少量镍的CaK(Fe1-xNix)4As4新型化合物材料。回答下列问题:
(1)基态镍原子的外围电子排布式为___________ 。
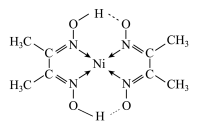
(2)在稀氨水介质中,Ni2+与丁二酮肟(分子式为C4H8N2O2)反应可生成鲜红色沉淀,其分子结构如下图所示,该结构中碳原子的杂化方式为___________ ;其中碳、氮、氧三种元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4;1mol Fe(CO)5分子中含有σ 键数目为___________ ;已知Ni(CO)4分子为正四面体构型,下列溶剂能够溶解Ni(CO)4的是___________ (填字母)。
a.四氯化碳 b.苯 c.水 d.液氨
(4)K3AsO3可用于碘的微量分析,AsO 的立体构型为
的立体构型为___________ ,写出一种与其互为等电子体的分子___________ (填化学式)。
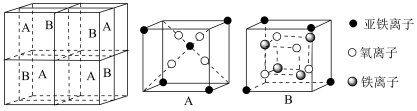
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。则该化合物中Fe2+、Fe3+、O2-的个数比为___________ (填最简整数比);已知该晶体的密度dg/cm3,阿伏加德罗常数的值为NA,则晶胞参数为___________ nm(用含d和NA的代数式表示)。
(1)基态镍原子的外围电子排布式为
(2)在稀氨水介质中,Ni2+与丁二酮肟(分子式为C4H8N2O2)反应可生成鲜红色沉淀,其分子结构如下图所示,该结构中碳原子的杂化方式为

(3)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4;1mol Fe(CO)5分子中含有σ 键数目为
a.四氯化碳 b.苯 c.水 d.液氨
(4)K3AsO3可用于碘的微量分析,AsO
 的立体构型为
的立体构型为(5)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。则该化合物中Fe2+、Fe3+、O2-的个数比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】请回答:
(1)下列状态的钙中,电离最外层的一个电子所需能量最大的是__________ 。
A.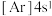 B.
B.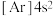 C.
C.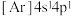 D.
D.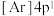
 和
和 的半径比较:
的半径比较: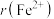
__________ 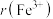 [填“
[填“ ”、“
”、“ ”或“
”或“ ”,下同]。
”,下同]。 和
和 的键角比较
的键角比较
________  。
。
(2)常温下, 苯和
苯和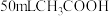 混合,溶液的总体积大于
混合,溶液的总体积大于 ,理由是
,理由是___________ 。 熔点为
熔点为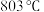 ,而等物质的量的
,而等物质的量的 和
和 组成的混合体系的熔点却只有
组成的混合体系的熔点却只有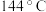 ,解析原因
,解析原因__________ 。
(3)某晶体的晶胞在 平面上的投影图如下(A为K、B为Fe、C为Se):则该晶体的化学式为
平面上的投影图如下(A为K、B为Fe、C为Se):则该晶体的化学式为___________ 。

(1)下列状态的钙中,电离最外层的一个电子所需能量最大的是
A.
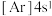 B.
B.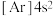 C.
C.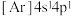 D.
D.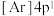
 和
和 的半径比较:
的半径比较: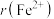
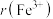 [填“
[填“ ”、“
”、“ ”或“
”或“ ”,下同]。
”,下同]。 和
和 的键角比较
的键角比较
 。
。(2)常温下,
 苯和
苯和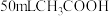 混合,溶液的总体积大于
混合,溶液的总体积大于 ,理由是
,理由是 熔点为
熔点为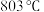 ,而等物质的量的
,而等物质的量的 和
和 组成的混合体系的熔点却只有
组成的混合体系的熔点却只有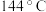 ,解析原因
,解析原因(3)某晶体的晶胞在
 平面上的投影图如下(A为K、B为Fe、C为Se):则该晶体的化学式为
平面上的投影图如下(A为K、B为Fe、C为Se):则该晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮化镓(GaN)已成为固态射频功率应用领域无可争议的冠军,它在雷达,5G无线领域等方面应用广泛。回答下列问题:

(1)GaN是坚硬的高熔点材料,熔点约为1700℃,科研人员可以利用_______ 实验测定晶体氮化镓中原子的空间排布。晶体GaN的熔点高于晶体GaAs(熔点1238℃)熔点的原因是_______ 。
(2)氮化镓的晶胞结构如图1所示,晶胞中Ga的配位数为_______ ,每个晶胞中含有GaN的单元数有_______ 个。
(3)氮化镓晶胞的边长分别为为anm、bnm、cnm,阿伏加德罗常数的值用NA表示,则GaN晶体的密度为_______ g·cm-3(列出计算表达式)。
(4)氮元素与铁元素形成的一种化合物平面结构如图2所示(大球表示Fe,小球表示N),则该化合物的化学式为_______ 。

(1)GaN是坚硬的高熔点材料,熔点约为1700℃,科研人员可以利用
(2)氮化镓的晶胞结构如图1所示,晶胞中Ga的配位数为
(3)氮化镓晶胞的边长分别为为anm、bnm、cnm,阿伏加德罗常数的值用NA表示,则GaN晶体的密度为
(4)氮元素与铁元素形成的一种化合物平面结构如图2所示(大球表示Fe,小球表示N),则该化合物的化学式为
您最近一年使用:0次
【推荐3】我国在化学领域取得了丰硕的成果,从古至今都有着重要的贡献。
(1)《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的Al3+、Ca2+生成的红色配合物X是最早的媒染染料。 外还有
外还有___________ ,茜素水溶性较好的主要原因是①___________ ,②___________ 。
(2)单质S和H2在低温高压下可形成一种新型超导材料,其晶胞如图。该物质的晶体类型是___________ ,该化合物的化学式为___________ 。___________ ,该晶体密度为___________ g·cm-3(写出计算式,用NA表示阿伏加德罗常数的值)。在该晶体中掺杂少量ZnO后形成的催化剂,化学式可表示为ZnxZr1-xOy,则y=___________ (用x表达)。
(1)《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的Al3+、Ca2+生成的红色配合物X是最早的媒染染料。

 外还有
外还有(2)单质S和H2在低温高压下可形成一种新型超导材料,其晶胞如图。该物质的晶体类型是


您最近一年使用:0次



