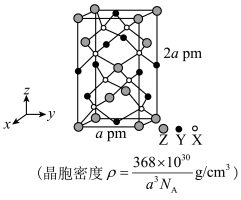
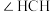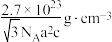原子序数依次增大的三种前四周期元素X、Y、Z组成的某天然矿石的晶体结构如图所示。其中Y元素的一种氧化物具有磁性,Z元素的价电子数为11,下列说法正确的是

| A.Y、Z均位于元素周期表的d区 | B.第三电离能 |
C.电负性: | D.键角: |
更新时间:2024-03-14 12:28:34
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】短周期非金属元素X、Y、Z、W的原子序数依次增大,基态X原子的未成对电子数是其所在周期中最多的,基态W原子的电子总数是其最高能级电子数的4倍,这四种元素与 元素组成的化合物的结构如图所示,下列说法错误的是
元素组成的化合物的结构如图所示,下列说法错误的是
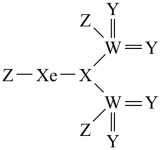
 元素组成的化合物的结构如图所示,下列说法错误的是
元素组成的化合物的结构如图所示,下列说法错误的是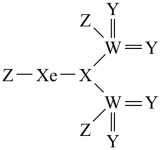
A.简单氢化物的沸点: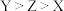 | B. 和 和 的VSEPR模型不同 的VSEPR模型不同 |
C.第一电离能: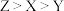 | D.同浓度时,最高价含氧酸的 : : |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为周期表的一小部分, A、B、C、D、E的位置关系如图所示。其中B元素最高化合价是最低化合价绝对值的3倍,它的最高价氧化物中含氧60%。下列说法正确的是
| A | ||
| D | B | E |
| C |
| A.D、B、E三种元素的第一电离能逐渐增大 |
| B.B元素最高价氧化物对应的水化物是强酸 |
| C.A元素是空气中含量最多的元素 |
D.简单气态氢化物的稳定性: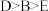 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】现有三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p63s23p5,下列排序正确的是
| A.含氧酸的酸性:③>①>② |
| B.原子半径:③>②>① |
| C.第一电离能:③>②>① |
| D.电负性:③>②>① |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】元素的性质及其在周期表中的位置与原子结构密切相关,下列有关判断不正确的是
| A.第四周期元素中,未成对电子数最多的元素位于钾元素后面第五位 |
| B.电负性的大小可以作为判断元素非金属性强弱的依据 |
| C.第一电离能的大小可以作为判断元素金属性强弱的依据 |
| D.共价化合物中,电负性大的成键元素表现为负价 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】右丙氧芬与左丙氧芬结构如图所示,前者具有镇痛作用,后者具有止咳作用。下列说法正确的是。
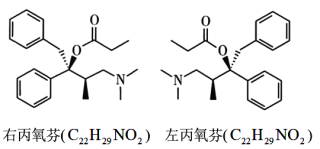
说明:左图中,实线表示处于纸平面内的键,实楔形线( )表示伸向纸平面前方的键,虚楔形线(
)表示伸向纸平面前方的键,虚楔形线( )表示伸向纸平面后方的键。
)表示伸向纸平面后方的键。

说明:左图中,实线表示处于纸平面内的键,实楔形线(
 )表示伸向纸平面前方的键,虚楔形线(
)表示伸向纸平面前方的键,虚楔形线( )表示伸向纸平面后方的键。
)表示伸向纸平面后方的键。| A.右丙氧芬和左丙氧芬分子中都只含有1个手性碳原子 |
| B.右丙氧芬与左丙氧芬互为对映异构体 |
C.右丙氧芬分子中氮碳键之间的夹角与 中氮氢键之间的夹角相同 中氮氢键之间的夹角相同 |
| D.右丙氧芬和左丙氧芬均易溶于水 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正确的是
| A.SO2、CO2都是直线形的分子 | B. 键角为120°,O3键角为180° 键角为120°,O3键角为180° |
| C.BF3和PCl3都是三角锥形的分子 | D.AlCl3、SO3都是平面三角形的粒子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】以铝土矿粉(主要含Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐);为原料生产Al2O3和Fe3O4的部分流程如下,已知有一种立方型晶体FeS2的结构如下图所示:

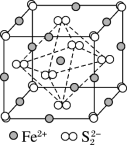
下列说法正确的是


下列说法正确的是
| A.“焙烧I”时,加入少量CaO可提高矿粉中硫的去除率 |
B.用NaOH溶液吸收过量SO2的离子方程式为:2OH- +SO2=SO +H2O +H2O |
| C.滤液中通入足量CO2,过滤后可得到Al2O3 |
D.与Fe2+距离最近且相等距离的S 的数目为6 的数目为6 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】叠氮化合物是重要的有机合成试剂,化学兴趣小组的同学在实验室制备了一种叠氮化合物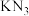 ,结构如图,下列说法正确的是
,结构如图,下列说法正确的是
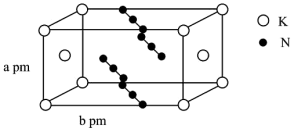
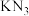 ,结构如图,下列说法正确的是
,结构如图,下列说法正确的是
| A.测定该晶体结构的方法是X射线衍射法 |
B.该晶体中每个 周围离最近且相等的 周围离最近且相等的 共有12个 共有12个 |
C. 与 与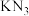 相比, 相比, 的熔点低于 的熔点低于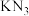 的熔点 的熔点 |
D.该叠氮化合物的密度为 |
您最近半年使用:0次

 含有相同的电子数,W原子最高能级和最低能级填充电子的数目相等,下列说法正确的是
含有相同的电子数,W原子最高能级和最低能级填充电子的数目相等,下列说法正确的是
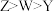
 键与s-p
键与s-p 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是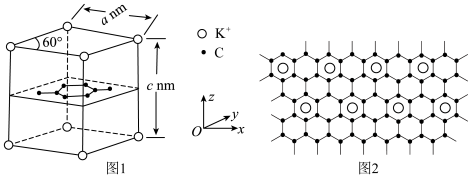
 中
中 大于
大于 中
中