某兴趣小组做了以下实验,实验结果记录如下
(1)实验1、2中Al电极的作用是否相同?_______ 。
(2)实验3中铝为_______ 极,电极反应式为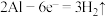 石墨为
石墨为_______ 极;电池总反应式为_______ 。
(3)实验4中铝为_______ 极,原因是_______ ,写出铝电极的电极反应式_______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
(2)实验3中铝为
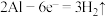 石墨为
石墨为(3)实验4中铝为
更新时间:2024-03-15 14:28:40
|
相似题推荐
【推荐1】化学能与电能之间的相互转化与人类的生活实际密切相关,在生产、生活中有重要的应用,同时也是学生形成化学学科核心素养的重要组成部分。
(1)熔融状态下,钠的单质和氯化亚铁能组成可充电电池,工作原理如图所示,反应原理为 ,该电池放电时,正极反应式为
,该电池放电时,正极反应式为___________ ;充电时,___________ (写物质名称)电极接电源的负极;该电池的电解质为___________ 。

(2)某同学用铜片、石墨作电极电解一定浓度的硫酸铜溶液,工作原理如图所示,一段时间后停止通电取出电极。若在电解后的溶液中加入0.98g氢氧化铜粉末恰好完全溶解,经测定所得的溶液与电解前完全相同。请回答下列问题:
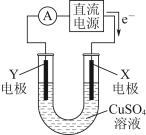
①Y电极材料是___________ 。
②电解过程中X电极上发生的电极反应是___________ 。
③如在电解后的溶液中加入足量的小苏打,充分反应后产生的气体在标准状况下所占的体积是___________ 。
(1)熔融状态下,钠的单质和氯化亚铁能组成可充电电池,工作原理如图所示,反应原理为
 ,该电池放电时,正极反应式为
,该电池放电时,正极反应式为
(2)某同学用铜片、石墨作电极电解一定浓度的硫酸铜溶液,工作原理如图所示,一段时间后停止通电取出电极。若在电解后的溶液中加入0.98g氢氧化铜粉末恰好完全溶解,经测定所得的溶液与电解前完全相同。请回答下列问题:

①Y电极材料是
②电解过程中X电极上发生的电极反应是
③如在电解后的溶液中加入足量的小苏打,充分反应后产生的气体在标准状况下所占的体积是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】合理开发利用能源具有重要意义。回答下列问题:
(1)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。
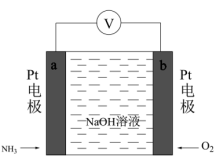
①电极b的名称是___________ ,电子的流动方向为___________ 。
②a极的电极反应式为___________ 。
③电池工作时,理论上反应消耗NH3与O2的物质的量之比为___________ 。
(2)通过如下流程可实现SO2和NO综合处理并获得保险粉( )和硝铵。
)和硝铵。

①装置Ⅲ中生成 与
与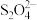 的物质的量之比为
的物质的量之比为___________ 。
②装置Ⅳ中溶液含有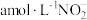 和
和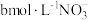 ,欲将cL该溶液完全转化为硝铵,需要通入
,欲将cL该溶液完全转化为硝铵,需要通入 与
与 的体积比为
的体积比为___________ (同温同压下)。
(1)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。

①电极b的名称是
②a极的电极反应式为
③电池工作时,理论上反应消耗NH3与O2的物质的量之比为
(2)通过如下流程可实现SO2和NO综合处理并获得保险粉(
 )和硝铵。
)和硝铵。
①装置Ⅲ中生成
 与
与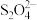 的物质的量之比为
的物质的量之比为②装置Ⅳ中溶液含有
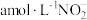 和
和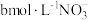 ,欲将cL该溶液完全转化为硝铵,需要通入
,欲将cL该溶液完全转化为硝铵,需要通入 与
与 的体积比为
的体积比为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】I.化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热量的形式表现出来,叫做反应热。由于反应的情况不同,反应热可分为许多种,如标准燃烧热和中和反应反应热等。
(1)下列△H表示物质标准燃烧热的是_____ ;表示中和反应反应热的是_____ 。(填“△H1”、“△H2”、“△H3”等)
A.2H2(g)+O2(g)=2H2O(l) △H1
B.C(s)+ O2(g)=CO(g) △H2=-Q1kJ•mol-1
O2(g)=CO(g) △H2=-Q1kJ•mol-1
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3
D.C(s)+O2(g)=CO2(g) △H4=-Q2kJ•mol-1
E.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(aq)+2H2O(l) △H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H6
(2)工业上可通过天然气跟水蒸气反应制取H2,有关反应的能量变化如图所示,则该反应的CH4(g)+H2O(g) CO(g)+3H2(g) △H=
CO(g)+3H2(g) △H=______ (用含a、b、c的式子表示)。
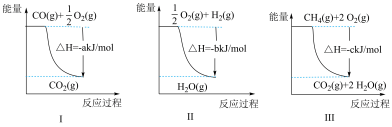
Ⅱ.电池的研发与生产、生活、军事等领域的发展密切相关。
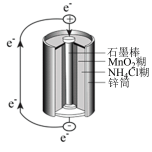
(3)锌锰干电池是最早使用的化学电池,其基本构造如图所示:电路中每通过0.4mole-,负极质量减少______ g。
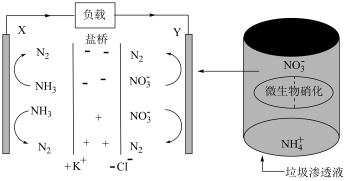
(4)一种利用垃圾渗透液实现发电装置示意图如图,当该装置工作时,Y极发生的电极反应式为:______ 。
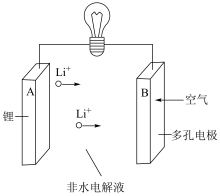
“锂-空气”电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(5)“锂-空气”电池的反应原理可表示为:2Li+O2 Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是______ 极(填“A”或“B”)。
(1)下列△H表示物质标准燃烧热的是
A.2H2(g)+O2(g)=2H2O(l) △H1
B.C(s)+
 O2(g)=CO(g) △H2=-Q1kJ•mol-1
O2(g)=CO(g) △H2=-Q1kJ•mol-1C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3
D.C(s)+O2(g)=CO2(g) △H4=-Q2kJ•mol-1
E.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(aq)+2H2O(l) △H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H6
(2)工业上可通过天然气跟水蒸气反应制取H2,有关反应的能量变化如图所示,则该反应的CH4(g)+H2O(g)
 CO(g)+3H2(g) △H=
CO(g)+3H2(g) △H=
Ⅱ.电池的研发与生产、生活、军事等领域的发展密切相关。
(3)锌锰干电池是最早使用的化学电池,其基本构造如图所示:电路中每通过0.4mole-,负极质量减少

(4)一种利用垃圾渗透液实现发电装置示意图如图,当该装置工作时,Y极发生的电极反应式为:

“锂-空气”电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(5)“锂-空气”电池的反应原理可表示为:2Li+O2
 Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
您最近半年使用:0次
【推荐1】酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物。该电池放电过程产生MnOOH。回收处理该废电池可得到多种化工原料。有关数据如下表所示:
物质的溶度积(Ksp)
回答下列问题:
(1)电池反应的离子方程式为___________ 。
(2)维持电流强度为0.5A,电池工作5分钟,理论上消耗锌___________ g.(已知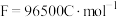 )
)
(3)用废电池的锌皮制备 的过程中,需除去锌皮中的少量杂质铁,其方法是加稀H2SO4和H2O2溶解,加碱调节至pH为
的过程中,需除去锌皮中的少量杂质铁,其方法是加稀H2SO4和H2O2溶解,加碱调节至pH为___________ 时,铁刚好沉淀完全(离子浓度小于 时,即可认为该离子沉淀完全);上述过程加入H2O2的原因
时,即可认为该离子沉淀完全);上述过程加入H2O2的原因___________ 。
(4)我国科学家研究Li-CO2电池,取得了重大科研成果。回答下列问题:Li-CO2电池中,Li为单质锂片,该电池中的CO2在正极发生电化学反应,研究表明,该电池反应产物为碳酸锂和单质碳,且CO2还原后与锂离子结合形成碳酸锂按以下4步骤进行,写出步骤Ⅲ的离子方程式:
Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ.___________
Ⅳ.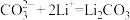
②研究表明,在电解质水溶液中,CO2气体可被电化学还原。
Ⅰ.CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为___________ 。
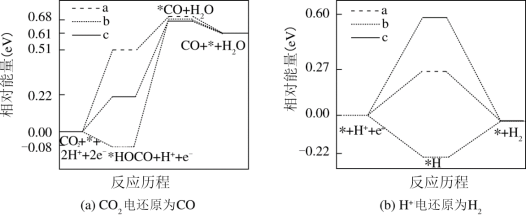
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上CO2电还原为CO的反应进程中(H+电还原为H2的反应可同时发生),相对能量变化如图。由此判断,CO2电还原为CO从易到难的顺序为___________ (用a、b、c字母排序)。
物质的溶度积(Ksp)
| 化合物 |  |  |  |
| Ksp近似值 | 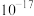 | 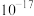 | 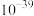 |
回答下列问题:
(1)电池反应的离子方程式为
(2)维持电流强度为0.5A,电池工作5分钟,理论上消耗锌
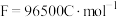 )
)(3)用废电池的锌皮制备
 的过程中,需除去锌皮中的少量杂质铁,其方法是加稀H2SO4和H2O2溶解,加碱调节至pH为
的过程中,需除去锌皮中的少量杂质铁,其方法是加稀H2SO4和H2O2溶解,加碱调节至pH为 时,即可认为该离子沉淀完全);上述过程加入H2O2的原因
时,即可认为该离子沉淀完全);上述过程加入H2O2的原因(4)我国科学家研究Li-CO2电池,取得了重大科研成果。回答下列问题:Li-CO2电池中,Li为单质锂片,该电池中的CO2在正极发生电化学反应,研究表明,该电池反应产物为碳酸锂和单质碳,且CO2还原后与锂离子结合形成碳酸锂按以下4步骤进行,写出步骤Ⅲ的离子方程式:
Ⅰ.
 ;
;Ⅱ.
 ;
;Ⅲ.
Ⅳ.
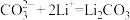
②研究表明,在电解质水溶液中,CO2气体可被电化学还原。
Ⅰ.CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上CO2电还原为CO的反应进程中(H+电还原为H2的反应可同时发生),相对能量变化如图。由此判断,CO2电还原为CO从易到难的顺序为

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】硫元素的单质及其化合物在科学研究、工农业生产、农药的制备与使用等方面具有广泛用途。请
根据以下应用回答有关问题:
(1)已知单质硫有S2、S4、S6、S8、Sn等多种形式,在Sn分子内S原子以S—S单键形成“锯齿形”的n
元环。试画出S8的八元环结构式___________ 。
(2)绿色农药“石硫合剂”的有效成分为五硫化钙(CaS5)和硫代硫酸钙(CaS2O3),可由单质硫和熟石灰在加热条件下制得,该反应的化学方程式为(反应中单质硫要求用S4表示);____________ 。
已知多硫化钙为离子化合物,其中S原子以S—S单键连接成多硫链而形成—2价的原子团,试画出五硫化钙的电子式_________________ 。
(3)科学家探测出火星大气中含有一种称为硫化羰的物成,其化学式为COS,结构与二氧化碳分子相似。硫化羰可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。请你利用下表中相关共价键的键能数据:
根据有关反应原理写出硫化羰气体与水蒸气反应生成CO2和H2S的热化学方程式:______________ .
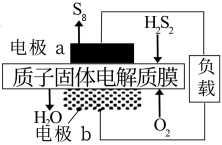
(4)S4广泛用于杀菌剂和抗真菌剂中,可由H2S2的燃料电池获得,其装置如下图所示。
①H2S2的名称是________ 。
②电极b为________ (选填“正极”、 “负极”)。
③电极a上发生的电极反应为:_______________ 。
(5)一氧化二硫(S2O)常温下是一种无色、不稳定的气体,实验室可由S8和氧化铜共热制得,同时生成硫化铜和SO2(注:生成物中气体产物等物质的量:升价与降价的硫也是等物质的量)。
该制备反应的化学方程式为________ ;
已知S2O常温时分解生成两种含硫的常见物质,请依据S2O中硫元素的价态分析并写出该分解反应的化学方程式_____________________ 。
根据以下应用回答有关问题:
(1)已知单质硫有S2、S4、S6、S8、Sn等多种形式,在Sn分子内S原子以S—S单键形成“锯齿形”的n
元环。试画出S8的八元环结构式
(2)绿色农药“石硫合剂”的有效成分为五硫化钙(CaS5)和硫代硫酸钙(CaS2O3),可由单质硫和熟石灰在加热条件下制得,该反应的化学方程式为(反应中单质硫要求用S4表示);
已知多硫化钙为离子化合物,其中S原子以S—S单键连接成多硫链而形成—2价的原子团,试画出五硫化钙的电子式
(3)科学家探测出火星大气中含有一种称为硫化羰的物成,其化学式为COS,结构与二氧化碳分子相似。硫化羰可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。请你利用下表中相关共价键的键能数据:
| 共价键 | C=O | C=S | H—O | H—S |
| 键能/kJ.mol-1 | 745 | 536 | 464 | 339 |
(4)S4广泛用于杀菌剂和抗真菌剂中,可由H2S2的燃料电池获得,其装置如下图所示。
①H2S2的名称是
②电极b为
③电极a上发生的电极反应为:
(5)一氧化二硫(S2O)常温下是一种无色、不稳定的气体,实验室可由S8和氧化铜共热制得,同时生成硫化铜和SO2(注:生成物中气体产物等物质的量:升价与降价的硫也是等物质的量)。
该制备反应的化学方程式为
已知S2O常温时分解生成两种含硫的常见物质,请依据S2O中硫元素的价态分析并写出该分解反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有X、Y、Z、W四种短周期元素,原子序数依次增大。X的阳离子就是一个质子。Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体。Y原子的最外层电子数是次外层电子数的2倍。请回答:
(1)Z2的电子式为_________ ,Y的原子结构示意图为________ ,YW2的结构式为________ 。
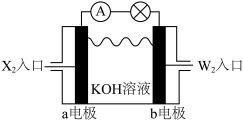
(2)将X2、W2 按下图所示通入某燃料电池中,其中,b电极的电极反应式为________ 。若有16gW2参加反应,转移的电子数是_______ NA。
(3)由X、Y、Z、W四种元素组成的无机酸酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为______________________________________________
(1)Z2的电子式为
(2)将X2、W2 按下图所示通入某燃料电池中,其中,b电极的电极反应式为

(3)由X、Y、Z、W四种元素组成的无机酸酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】完成下列问题。
I.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。
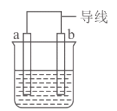
(1)当电极a为Al、电极b为Cu、电解质溶液为浓硝酸时,正极的电极反应式为_____ ,当电路中有0.2mol电子通过时,负极的质量减少_____ g。当电解质溶液为氢氧化钠溶液时,该装置负极的电极反应式为:_____ 。
II.X、Y、Z是同主族的三种元素,已知其最高价氧化物对应的水化物的酸性由强到弱的顺序是HXO4>HYO4>HZO4。则下列说法正确的是
(2)原子半径:_____ 。
(3)元素的非金属性:_____ 。
(4)气态氢化物稳定性:_____ 。
I.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。

(1)当电极a为Al、电极b为Cu、电解质溶液为浓硝酸时,正极的电极反应式为
II.X、Y、Z是同主族的三种元素,已知其最高价氧化物对应的水化物的酸性由强到弱的顺序是HXO4>HYO4>HZO4。则下列说法正确的是
(2)原子半径:
(3)元素的非金属性:
(4)气态氢化物稳定性:
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】运用化学反应原理研究NH3的性质具有重要意义。请回答下列问题:
(1)已知:①NH3 (g)+3O2(g)=2N2(g)+6H2O(g) △H=-1266.5kJ·mol-1
②N2(g)+O2(g)=2NO(g) △H=+180.5 kJ·mol-1
写出氨高温催化氧化生成NO的热化学方程式___________ 。
(2)氨气、空气可以构成燃料电池,其电池反应原理为:4NH3+302=2N2+6H2O。已知电解质溶液为KOH溶液,则负极的电极反应式为________ 。
(3)合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的化学平衡常数K值和温度的关系如下:

由上表数据可知该反应的△H_______ 0 填“> ”、“< ”或“=”) ;
理论上,为了增大平衡时H2的转化率,可采取的措施是_______ (选填字母);
A.增大压强 B.使用合适的催化剂 C.升高温度 D.及时分离出产物中的NH3
③400℃时,测得某时刻氨气、氮气、氢气的物质的量浓度分别为3mol·L-1、2 mol·L-1、l mol·L-1,此时刻该反应的V正(N2)=______ V逆(N2)。(填“>”、“<”或“=”)。
(4)已知25℃时,Ksp[Fe(OH)3]=1.0×l0-38, Ksp[Al(OH)3]=3.0×l0-34,当溶液中的金属离子浓度小于1.0×10-5mol·L-1时,可以认为沉淀完全。在含Fe3+、A13+的浓度均为1. 05mol·L-1的溶液中加入氨水,当Fe3+完全沉淀时,A13+沉淀的百分数____________ 。
(1)已知:①NH3 (g)+3O2(g)=2N2(g)+6H2O(g) △H=-1266.5kJ·mol-1
②N2(g)+O2(g)=2NO(g) △H=+180.5 kJ·mol-1
写出氨高温催化氧化生成NO的热化学方程式
(2)氨气、空气可以构成燃料电池,其电池反应原理为:4NH3+302=2N2+6H2O。已知电解质溶液为KOH溶液,则负极的电极反应式为
(3)合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的化学平衡常数K值和温度的关系如下:

由上表数据可知该反应的△H
理论上,为了增大平衡时H2的转化率,可采取的措施是
A.增大压强 B.使用合适的催化剂 C.升高温度 D.及时分离出产物中的NH3
③400℃时,测得某时刻氨气、氮气、氢气的物质的量浓度分别为3mol·L-1、2 mol·L-1、l mol·L-1,此时刻该反应的V正(N2)=
(4)已知25℃时,Ksp[Fe(OH)3]=1.0×l0-38, Ksp[Al(OH)3]=3.0×l0-34,当溶液中的金属离子浓度小于1.0×10-5mol·L-1时,可以认为沉淀完全。在含Fe3+、A13+的浓度均为1. 05mol·L-1的溶液中加入氨水,当Fe3+完全沉淀时,A13+沉淀的百分数
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物的探究实验,回答下列问题:
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:___________ 。
(2)装置A中设计g管的作用是___________ 。
(3)装置A中发生反应的离子方程式为___________ 。
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
(4)由实验1、2现象可以得出结论:增大pH,___________ 优先于___________ 放电;
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是___________ ;
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验___________ 作对照实验;
③实验目的ii是___________ ;
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:___________ 。
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:
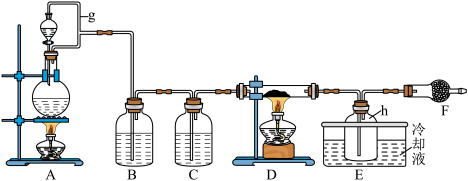
(2)装置A中设计g管的作用是
(3)装置A中发生反应的离子方程式为
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
| 实验编号 | 电压/V | pH | 阳极现象 | 阴极现象 |
| 1 | 1.5 | 1.00 | 无气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
| 2 | 1.5 | 5.52 | 无气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 3 | 3.0 | 5.52 | 少量气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 4 | 4.5 | 5.52 | 大量气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
(4)由实验1、2现象可以得出结论:增大pH,
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
| 实验编号 | c(NH4Cl)/mol·L-1 | 温度/℃ | 待测物理量X | 实验目的 |
| 5 | 0.5 | 30 | a | ___________ |
| 6 | 1.5 | i | b | 探究浓度对氯化铵水解平衡的影响 |
| 7 | 1.5 | 35 | c | ii |
| 8 | 2.0 | 40 | d | 探究温度、浓度同时对氯化铵化解平衡的影响 |
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验
③实验目的ii是
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:
您最近半年使用:0次



