如图,是工业生产中除去电石渣浆(含CaO)中的 并制取硫酸盐的一种常用流程。下列说法错误的是
并制取硫酸盐的一种常用流程。下列说法错误的是
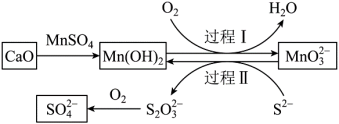
 并制取硫酸盐的一种常用流程。下列说法错误的是
并制取硫酸盐的一种常用流程。下列说法错误的是
A.碱性条件下,氧化性: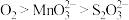 |
| B.过程Ⅰ中氧化剂和还原剂物质的量之比为1∶2 |
C.过程Ⅰ中,反应的离子方程式为 |
D.将1mol  转化为 转化为 理论上需要 理论上需要 的体积为22.4L(标准状况) 的体积为22.4L(标准状况) |
更新时间:2024-03-19 09:24:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列解释实验现象或用途的离子方程式书写不正确的是
A.用硫化钠处理含汞废水: |
B.将 通入氢氧化钠溶液中制消毒液: 通入氢氧化钠溶液中制消毒液: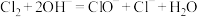 |
C. 溶液腐蚀铜板: 溶液腐蚀铜板: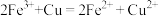 |
D. 溶于稀盐酸: 溶于稀盐酸: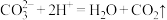 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】能正确表示下列变化的离子方程式是
| A.酸性碘化钾溶液中滴加适量双氧水:2I−+2H++H2O2=I2+2H2O |
| B.向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解:Mg(OH)2+2H+=2Mg2++2H2O |
C.用铝粉和NaOH溶液反应制取少量H2:Al+2OH-= +H2↑ +H2↑ |
| D.四氧化三铁溶于稀硝酸:Fe3O4+8H+=2Fe2+ +Fe3++4H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】几种离子在水溶液(溶液酸碱性可调节)中有如下转化关系。下列说法正确的是
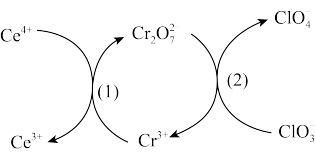

A.氧化性: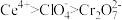 |
B.反应(1)生成 转移3mol电子 转移3mol电子 |
C.将反应(2)设计成原电池, 一定向负极迁移 一定向负极迁移 |
D.由图推知可以发生反应: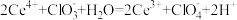 |
您最近一年使用:0次
【推荐2】下列根据实验现象得出的结论正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 废FeCl3蚀刻液X中加入少量铁粉,振荡 | 得到澄清溶液 | X中一定不含Cu2+ |
| B | 浓度均为0.1mol⋅L-1的Na2CO3和Na2S混合溶液中,滴入少量AgNO3溶液 | 产生黑色沉淀 | Ksp(Ag2S)大于Ksp(Ag2CO3) |
| C | KNO3和KOH混合溶液中加入铝粉并加热,管口放湿润的红色石蕊试纸 | 试纸变为蓝色 | NO3-还原为NH3 |
| D | KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机相呈橙色 | 氧化性:Cl2>Br2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意如下。下列说法错误的是
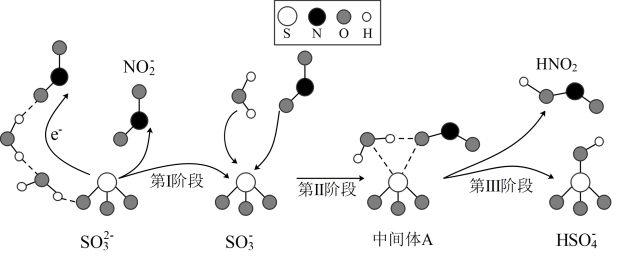

A.第II、III阶段总反应的离子方程式为: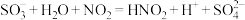 |
B.该过程中 为催化剂 为催化剂 |
C.第I阶段每1mol氧化剂参加反应,转移电子数目为 |
D.还原性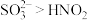 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在3Cl2+6KOH=KClO3+5KCl+3H2O的反应中,下列说法不正确的是
| A.Cl2既是氧化剂,又是还原剂 |
| B.参加反应的氧化剂和还原剂的物质的量之比为5:1 |
| C.反应中每消耗3molCl2,转移电子数为6NA |
| D.该氧化还原反应中只有氯元素化合价发生了改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】钒是一种重要的合金元素,主要用于钢铁工业。以富钒炉渣(主要含FeV2O4,少量P2O5等杂质)为原料回收粗钒的流程如下,已知NH4VO3难溶于水。下列有关说法错误的是
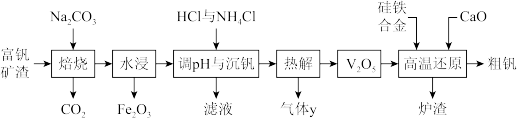

A.“焙烧”步骤中方程式为4FeV2O4+4Na2CO3+5O2 8NaVO3+2Fe2O3+4CO2 8NaVO3+2Fe2O3+4CO2 |
| B.“调pH与沉钒”步骤中磷元素以H3PO4的形式进入滤液中从而除杂 |
| C.“热解”步骤中气体产物为HCl |
| D.“高温还原”步骤中所得粗钒含有硅、铁杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某科研工作者设计用工厂废渣(主要成分为ZnO,另含少量FeO、CuO、SiO2、MnO等)制取高纯ZnO的工艺流程图如图所示。已知常温下 ,
,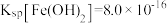 ,
,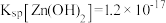 。下列说法错误的是
。下列说法错误的是

 ,
,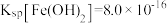 ,
,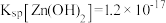 。下列说法错误的是
。下列说法错误的是
| A.“酸浸”中,滤渣A主要成分为SiO2 |
| B.“除锰”中,H2O2的作用是将Mn2+、Fe2+氧化 |
| C.“除铁”中,ZnO与Fe3+发生反应生成Fe |
D.“除锰”后滤液中 ,“除铁”操作中可以调节pH的范围是3<pH<5.5(当离子浓度 ,“除铁”操作中可以调节pH的范围是3<pH<5.5(当离子浓度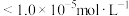 时,表示该离子沉淀完全) 时,表示该离子沉淀完全) |
您最近一年使用:0次



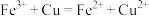
 溶液与过量氨水反应:
溶液与过量氨水反应: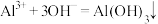
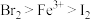 ,向含a个
,向含a个 的溶液中加入含b个
的溶液中加入含b个 的溴水,充分反应。下列说法不正确的是
的溴水,充分反应。下列说法不正确的是
 时,发生离子反应:
时,发生离子反应:
 时,反应后的溶液中
时,反应后的溶液中 、
、 、
、 离子数目之比为
离子数目之比为
 时,发生离子反应:
时,发生离子反应: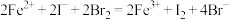
 、
、 、
、 三种溶质,其中
三种溶质,其中 、
、 。据此推测
。据此推测


 是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
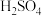 与
与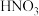 物质的量之比最好为3:2
物质的量之比最好为3:2


