亚硝酸钠(NaNO2)有毒、有咸味,外形与食盐相似,人若误食会引起中毒。某兴趣小组欲研究亚硝酸钠,查阅资料得到如表信息。试根据信息回答下列问题:
(1)已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,则该反应中氧化剂是 _______ ;若有0.75mol电子发生转移,则被氧化的还原剂的粒子数为 _______ (用NA表示阿伏加德罗常数的值)。
(2)人若误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列说法错误的是 _______(填序号)。
(3)下列方法中,可用来区分NaNO2和NaCl的是 _______ (填序号)。
A.焰色反应
B.滴加酸化的FeSO4溶液和KSCN溶液
C.在酸性条件下加入淀粉KI溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式_______ 。
| 药品 | NaNO2(亚硝酸钠) |
| 性质 | 在酸性溶液中有较强氧化性,能将Fe2+氧化成Fe3+。 |
(2)人若误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列说法错误的是 _______(填序号)。
| A.NaNO2被还原 |
| B.维生素C具有还原性 |
| C.还原性:维生素C>Fe2+ |
| D.NaNO2是还原剂 |
A.焰色反应
B.滴加酸化的FeSO4溶液和KSCN溶液
C.在酸性条件下加入淀粉KI溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式
更新时间:2024-03-19 21:40:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】从元素化合价和物质类别两个维度学习、研究物质的性质及转化,是一种行之有效的方法。
(1)下图是氮元素的“价-类二维图”的部分信息。

①共价化合物A的化学式___________ (填“一定”或“不一定”)为NH3。
②图中氮的氧化物中,属于酸性氧化物的有___________ 。(用化学式表示)
③工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,写出其化学方程式:___________ 。
(2)目前我国锅炉烟气脱硝技术有新发现,科学家对O3氧化烟气脱硝同时制硝酸进行了实验研究,其生产硝酸的机理如下:
NO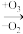 NO2
NO2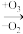 NO3
NO3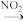 N2O5
N2O5 HNO3。
HNO3。
①NO3分子内存在两个过氧键,且氧均满足8电子稳定结构,NO3中N的化合价为___________ 。
②N2O5与O3作用也能生成NO3与氧气,根据反应前后同种元素价态相同,不参与氧化还原反应的原则,请分析反应N2O5+O3=2NO3+O2中,N2O5的作用是___________ (填“作氧化剂”、“作还原剂”或“既作氧化剂,又作还原剂”)。
③写出在有水存在时,O3与NO以物质的量之比3∶2完全反应的总化学方程式:___________ 。
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为___________ ,若反应中有0.3 mol 电子发生转移时,生成亚硝酸的质量为___________ g。
(1)下图是氮元素的“价-类二维图”的部分信息。

①共价化合物A的化学式
②图中氮的氧化物中,属于酸性氧化物的有
③工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,写出其化学方程式:
(2)目前我国锅炉烟气脱硝技术有新发现,科学家对O3氧化烟气脱硝同时制硝酸进行了实验研究,其生产硝酸的机理如下:
NO
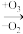 NO2
NO2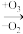 NO3
NO3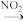 N2O5
N2O5 HNO3。
HNO3。①NO3分子内存在两个过氧键,且氧均满足8电子稳定结构,NO3中N的化合价为
②N2O5与O3作用也能生成NO3与氧气,根据反应前后同种元素价态相同,不参与氧化还原反应的原则,请分析反应N2O5+O3=2NO3+O2中,N2O5的作用是
③写出在有水存在时,O3与NO以物质的量之比3∶2完全反应的总化学方程式:
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求完成下面小题。
(1)有以下转化关系:
反应①:___________
 在上述有序号的反应中,除了①⑥外,需用氧化剂的是
在上述有序号的反应中,除了①⑥外,需用氧化剂的是___________ (填序号)。
(2) 。该反应中,生成物M是
。该反应中,生成物M是___________ (填化学式)。
(3)针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅作氧化剂的反应是___________ (填序号,下同)。
(4)取少量NaH放入水中,剧烈反应放出一种无色、无味的气体,并形成一种碱性溶液。NaH与水反应的化学方程式为___________ 。
(5) 与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:
与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:___________ 。
(6)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药是将硫磺、木炭、硝酸钾按照一定比例混合,在发生爆炸时,没有产生污染性物质。请书写出该反应方程式并配平___________ 。
(1)有以下转化关系:

反应①:
 在上述有序号的反应中,除了①⑥外,需用氧化剂的是
在上述有序号的反应中,除了①⑥外,需用氧化剂的是(2)
 。该反应中,生成物M是
。该反应中,生成物M是(3)针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅作氧化剂的反应是
(4)取少量NaH放入水中,剧烈反应放出一种无色、无味的气体,并形成一种碱性溶液。NaH与水反应的化学方程式为
(5)
 与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:
与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:(6)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药是将硫磺、木炭、硝酸钾按照一定比例混合,在发生爆炸时,没有产生污染性物质。请书写出该反应方程式并配平
您最近半年使用:0次
【推荐3】完成下列问题
(1)配平该方程式:_______ ,_______KMnO4+_______HCl(浓)=_______KCl+_______MnCl2+_______Cl2↑+_______H2O
(2)维生素C能使食物中的Fe3+转化为Fe2+,即Fe3+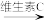 Fe2+。在此变化中,Fe3+被
Fe2+。在此变化中,Fe3+被_______ (填“氧化”或“还原”,下同),维生素C是_______ 剂。
(3)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
①写出该反应的离子方程式:_______ 。
②用单线桥法表示电子转移的方向和数目_______ 。由反应方程式可知,被还原的HNO3和参加反应的HNO3的物质的量比为_______ 。
(4)二氧化氯是世卫组织确认的A级新型高效安全的消毒剂,其安全性远高于氯气。制备方法之一为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,氧化产物与还原产物的物质的量之比为_______ 。
(1)配平该方程式:
(2)维生素C能使食物中的Fe3+转化为Fe2+,即Fe3+
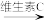 Fe2+。在此变化中,Fe3+被
Fe2+。在此变化中,Fe3+被(3)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
①写出该反应的离子方程式:
②用单线桥法表示电子转移的方向和数目
(4)二氧化氯是世卫组织确认的A级新型高效安全的消毒剂,其安全性远高于氯气。制备方法之一为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,氧化产物与还原产物的物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.海带中含有丰富的碘,某学习小组设计并进行以下实验:
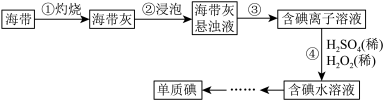
(1)步骤③的实验操作所用。用到的玻璃仪器有___________ 。步骤④的离子反应方程式为: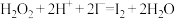 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是___________ ,还原剂是___________ 。步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现蓝色,说明有碘单质产生。
II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失, 被氧气氧化成碘单质(I2),同时得到强碱性物质。
被氧气氧化成碘单质(I2),同时得到强碱性物质。
(2)写出潮湿环境下KI与氧气反应的化学方程式:___________ 。
III.现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:
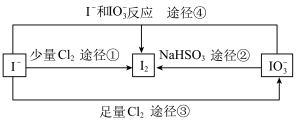
(3)四个途径中属于氧化还原反应的是___________ (填序号)。
(4)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为: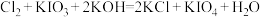 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(5)比较I2、 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:___________ 。

(1)步骤③的实验操作所用。用到的玻璃仪器有
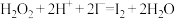 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失,
 被氧气氧化成碘单质(I2),同时得到强碱性物质。
被氧气氧化成碘单质(I2),同时得到强碱性物质。(2)写出潮湿环境下KI与氧气反应的化学方程式:
III.现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:

(3)四个途径中属于氧化还原反应的是
(4)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为:
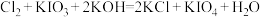 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(5)比较I2、
 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)氯碱工业的反应原理为 ,该反应中的氧化剂是
,该反应中的氧化剂是___________ 。
(2)为了防止食品变质而添加的抗氧化剂应具有___________ 性。(填“氧化”或“还原”)
(3)电子工业中常用 溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板,其反应的离子方程式为
溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板,其反应的离子方程式为___________ 。
(4) 可用于制备铬矾、铬颜料等,也是制造火柴头的原料之一。已知反应:
可用于制备铬矾、铬颜料等,也是制造火柴头的原料之一。已知反应: ,由此可知
,由此可知 的氧化性
的氧化性___________ (填“>”或“<”) 。该反应中氧化剂与还原剂的物质的量之比为
。该反应中氧化剂与还原剂的物质的量之比为___________ 。
(1)氯碱工业的反应原理为
 ,该反应中的氧化剂是
,该反应中的氧化剂是(2)为了防止食品变质而添加的抗氧化剂应具有
(3)电子工业中常用
 溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板,其反应的离子方程式为
溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板,其反应的离子方程式为(4)
 可用于制备铬矾、铬颜料等,也是制造火柴头的原料之一。已知反应:
可用于制备铬矾、铬颜料等,也是制造火柴头的原料之一。已知反应: ,由此可知
,由此可知 的氧化性
的氧化性 。该反应中氧化剂与还原剂的物质的量之比为
。该反应中氧化剂与还原剂的物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】比较下列各组反应,回答问题:
(1)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质,则在Cu、Fe、Ag中,___________ 还原性最强;在Cu2+、Fe2+、Ag+中,_________ 氧化性最强。
(2)已知氯气与氯化亚铁溶液反应的离子方程式是2Fe2++Cl2=2Fe3++2Cl−;氯化铁溶液与碘化钾溶液反应的离子方程式是2Fe3++2I−=2Fe2++I2。则Fe3+、Cl2、I2的氧化性由强到弱的顺序是________ ;若将氯气通入物质的量浓度相同的氯化亚铁、碘化钾的混合溶液中,则先被氧化的离子是____________ 。
(3)铁丝可在氯气中燃烧:2Fe+3Cl2 2FeCl3,也可在硫蒸气中燃烧:Fe+S
2FeCl3,也可在硫蒸气中燃烧:Fe+S FeS。由此可推知,氯气的氧化性比硫的氧化性
FeS。由此可推知,氯气的氧化性比硫的氧化性__________ 。
(1)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质,则在Cu、Fe、Ag中,
(2)已知氯气与氯化亚铁溶液反应的离子方程式是2Fe2++Cl2=2Fe3++2Cl−;氯化铁溶液与碘化钾溶液反应的离子方程式是2Fe3++2I−=2Fe2++I2。则Fe3+、Cl2、I2的氧化性由强到弱的顺序是
(3)铁丝可在氯气中燃烧:2Fe+3Cl2
 2FeCl3,也可在硫蒸气中燃烧:Fe+S
2FeCl3,也可在硫蒸气中燃烧:Fe+S FeS。由此可推知,氯气的氧化性比硫的氧化性
FeS。由此可推知,氯气的氧化性比硫的氧化性
您最近半年使用:0次
填空题
|
适中
(0.64)
【推荐1】建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:

(1)配平上述反应方程式______________ 。
(2)上述反应的氧化剂是_______ ,若反应中有5 mol电子转移,则生成NO在标准状况下的体积是_______ L。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水;②碘化钾淀粉试纸;③淀粉;④白酒;⑤食醋,进行实验,下列几组合适的是_______ 。
A.③⑤ B.①②④ C.①②⑤ D.①②③⑤

(1)配平上述反应方程式
(2)上述反应的氧化剂是
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水;②碘化钾淀粉试纸;③淀粉;④白酒;⑤食醋,进行实验,下列几组合适的是
A.③⑤ B.①②④ C.①②⑤ D.①②③⑤
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁有许多重要的化合物,除中学化学常见的三种氧化物和两种氢氧化物外,还有许多盐。FeSO4·7H2O是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子Cr2O72-)进行处理。
(1)绿矾除用铁粉与硫酸反应生成外,工业上还可用空气、水、黄铁矿(主要成分为FeS2)来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式___________________________________ 。
(2)试配平:_____ Fe2++______Cr2O72-+_______H+=_____Fe3++_____Cr3++_____H2O。
(3)若该废水经处理后Cr3+的含量为1×10−2mol·m−3,理论上83.4 kg绿矾可以处理该废水_____ 吨(已知废水的密度为1 g·cm−3)。
(1)绿矾除用铁粉与硫酸反应生成外,工业上还可用空气、水、黄铁矿(主要成分为FeS2)来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式
(2)试配平:
(3)若该废水经处理后Cr3+的含量为1×10−2mol·m−3,理论上83.4 kg绿矾可以处理该废水
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为2种无毒气体。T℃时,将0.8 mol NO和0.6 mol CO充入容积为2 L的密闭容器中,模拟尾气转化,容器中NO物质的量随时间变化如图。
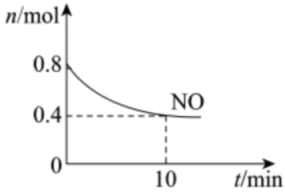
(1)将NO、CO转化为2种无毒气体的化学方程式是___________ 。
(2)反应开始至10 min,v(NO)=___________ mol/(L·min)。
II.某有机物由碳、氢、氧、氮4种元素组成,其中含碳32%,氢6.7%,氮18.7%(均为质量分数)。该有机物的相对分子质量为75。
(3)通过计算写出该有机物的分子式___________ 。
(4)该有机物是蛋白质水解的产物,它与乙醇反应生成的酯可用于合成医药和农药,请写出生成该酯的化学方程式___________ 。

(1)将NO、CO转化为2种无毒气体的化学方程式是
(2)反应开始至10 min,v(NO)=
II.某有机物由碳、氢、氧、氮4种元素组成,其中含碳32%,氢6.7%,氮18.7%(均为质量分数)。该有机物的相对分子质量为75。
(3)通过计算写出该有机物的分子式
(4)该有机物是蛋白质水解的产物,它与乙醇反应生成的酯可用于合成医药和农药,请写出生成该酯的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】做某溶液的焰色反应实验,火焰呈黄色,则溶液中一定存在钠元素,不存在钾元素,该判断是否正确?为什么_______ 。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是______ 。
A.钠燃烧时发出黄色的火焰
B.过氧化钠能与酸反应生成盐和水,所以过氧化钠是碱性氧化物
C.过氧化钠能与水反应,所以过氧化钠可以作气体的干燥剂
D.过氧化钠中阴阳离子个数比为1:1
E.钠是一种很强的还原剂,钠可以把锆、铌等金属从它们的化合物的水溶液中置换出来
F.Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
G.可用水来确定某Na2O粉末中是否含有Na2O2
H.将足量的Na2O2、Na2O分别加到酚酞试液中,最终溶液均为红色
I.Na2CO3受热难分解
J.Na2O常温下为浅黄色固体
A.钠燃烧时发出黄色的火焰
B.过氧化钠能与酸反应生成盐和水,所以过氧化钠是碱性氧化物
C.过氧化钠能与水反应,所以过氧化钠可以作气体的干燥剂
D.过氧化钠中阴阳离子个数比为1:1
E.钠是一种很强的还原剂,钠可以把锆、铌等金属从它们的化合物的水溶液中置换出来
F.Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
G.可用水来确定某Na2O粉末中是否含有Na2O2
H.将足量的Na2O2、Na2O分别加到酚酞试液中,最终溶液均为红色
I.Na2CO3受热难分解
J.Na2O常温下为浅黄色固体
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组在课外活动中,对某溶液进行了多次检验,其中三次检验结果如下表所示,请回答下列问题。
(1)三次检验结果中第___________ 次检验结果不正确。
(2)检验时,为了确定溶液中是否存在 、
、 、
、 进行下列实验:
进行下列实验:
第一,向溶液中滴加___________ (填化学式)溶液,其目的是___________ ;
第二,继续加入过量的___________ (填化学式)溶液,其目的是___________ ;
第三:向溶液中滴加___________ (填化学式)溶液,其目的是___________ ;
第四:过滤,再向滤液中加入___________ (填化学式)溶液,其目的是___________ 。
(3)为了确定 的存在,写出
的存在,写出 鉴定的实验方法和现象:
鉴定的实验方法和现象:___________ 。
| 检验次数 | 溶液中检验出的物质 |
| 第一次 |  、 、 、 、 、 、 |
| 第二次 |  、 、 、 、 、 、 |
| 第三次 |  、 、 、 、 、 、 |
(2)检验时,为了确定溶液中是否存在
 、
、 、
、 进行下列实验:
进行下列实验:第一,向溶液中滴加
第二,继续加入过量的
第三:向溶液中滴加
第四:过滤,再向滤液中加入
(3)为了确定
 的存在,写出
的存在,写出 鉴定的实验方法和现象:
鉴定的实验方法和现象:
您最近半年使用:0次



