某研究小组以工厂废渣( 、
、 )为原料制取
)为原料制取 工艺流程如图。回答下列问题:
工艺流程如图。回答下列问题:
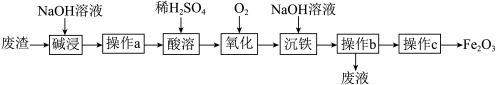
(1)“碱浸”时将固体磨碎的目的是_______ ,发生反应的离子方程式为_______ 。
(2)“操作a”需要的玻璃仪器有_______ 、_______ 、_______ 。
(3)“氧化”过程的离子方程式是_______ 。
(4)操作c的名称是_______ ;从分类的角度, 属于
属于_______ 。
(5)向 、Cu的混合物中加入盐酸,反应后的溶液中检验不出
、Cu的混合物中加入盐酸,反应后的溶液中检验不出 。检验
。检验 试剂名称是
试剂名称是_______ ,反应后溶液中没有 的原因是
的原因是_______ (用离子方程式表示)。
 、
、 )为原料制取
)为原料制取 工艺流程如图。回答下列问题:
工艺流程如图。回答下列问题:
(1)“碱浸”时将固体磨碎的目的是
(2)“操作a”需要的玻璃仪器有
(3)“氧化”过程的离子方程式是
(4)操作c的名称是
 属于
属于(5)向
 、Cu的混合物中加入盐酸,反应后的溶液中检验不出
、Cu的混合物中加入盐酸,反应后的溶液中检验不出 。检验
。检验 试剂名称是
试剂名称是 的原因是
的原因是
更新时间:2024-03-21 20:00:13
|
相似题推荐
【推荐1】工厂烟气(主要污染物SO2、NO)直接排放会造成空气污染,需处理后才能排放。
(1)O3氧化。O3氧化过程中部分反应的能量变化如图所示。
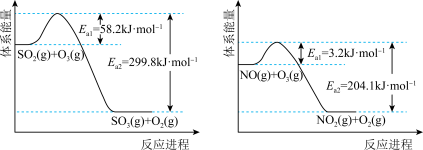
①已知2SO2(g)+O2(g) =2SO3(g) ΔH =−198 kJ·mol−1。则反应2O3(g)=3O2(g)的 ΔH=_______ kJ·mol−1。
②其他条件不变时,增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是_______ 。
(2)NaClO2氧化。40 ℃时向一定量NaClO2溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。

①写出NO与ClO 反应的离子方程式:
反应的离子方程式:_______ 。
②烟气中含有少量SO2,能提高NO的脱除率,可能原因是_______ 。
(3)TiO2光催化。主要是利用TiO2光催化剂在紫外线作用下产生的高活性自由基(·OH、·O )和h+(h+代表空位,空位有很强的得电子能力),将烟气中的SO2、NO等氧化除去。TiO2光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知TiO2中电子跃迁的能量hv=3.2eV。
)和h+(h+代表空位,空位有很强的得电子能力),将烟气中的SO2、NO等氧化除去。TiO2光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知TiO2中电子跃迁的能量hv=3.2eV。
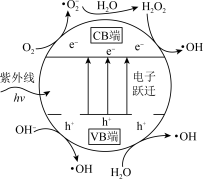
①TiO2光催化剂在紫外线作用下产生·OH的过程可描述为_______ 。
②在TiO2中掺杂一定量的金属离子可提高光催化活性。对所掺杂金属离子的要求是_______ 。
(1)O3氧化。O3氧化过程中部分反应的能量变化如图所示。

①已知2SO2(g)+O2(g) =2SO3(g) ΔH =−198 kJ·mol−1。则反应2O3(g)=3O2(g)的 ΔH=
②其他条件不变时,增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是
(2)NaClO2氧化。40 ℃时向一定量NaClO2溶液中按一定流速持续通入工厂烟气,溶液的pH与ORP值(氧化还原电位)随时间变化如图所示。

①写出NO与ClO
 反应的离子方程式:
反应的离子方程式:②烟气中含有少量SO2,能提高NO的脱除率,可能原因是
(3)TiO2光催化。主要是利用TiO2光催化剂在紫外线作用下产生的高活性自由基(·OH、·O
 )和h+(h+代表空位,空位有很强的得电子能力),将烟气中的SO2、NO等氧化除去。TiO2光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知TiO2中电子跃迁的能量hv=3.2eV。
)和h+(h+代表空位,空位有很强的得电子能力),将烟气中的SO2、NO等氧化除去。TiO2光催化剂粒子表面产生·OH的机理如图所示(图中部分产物略去)。已知TiO2中电子跃迁的能量hv=3.2eV。
①TiO2光催化剂在紫外线作用下产生·OH的过程可描述为
②在TiO2中掺杂一定量的金属离子可提高光催化活性。对所掺杂金属离子的要求是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】海带、紫菜等藻类植物中含有丰富的碘元素,海带提碘的实验流程如下:

(1)步骤①中用到的硅酸盐材质的仪器为_______ (写名称)。
(2)步骤③用酸化的H2O2氧化I- 的离子方程式为_______ 。
(3)实验小组根据元素周期律研究氧化I- 的氧化剂 (见下图),A、B两种盐溶液分别为_______ 、_______ , 添加C、D两处溶液的作用是_______ 。实验得出结论:氧化性强弱为Cl2>Br2>I2
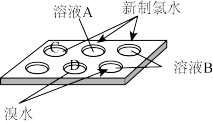
(4)实验小组还设计了下表实验,对金属阳离子氧化I- 进行研究。
已知:常温下,CuI(白色)、AgI(黄色)的Ksp分别为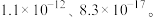
①实验2中a为_______ 溶液。
甲同学根据现象得出结论:Ag+氧化性比Cu2+弱且不能氧化I-。
乙同学对甲同学的结论提出质疑,查阅资料(常温下,反应2Ag+(aq)+2I-(aq)⇌2Ag(s)+I2(aq)的平衡常数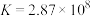 ,当c(Ag+)、c(I-)大于等于1mol·L-1时,Ag+可以氧化I-),借助原电池原理优化实验设计,证实了自己的观点。
,当c(Ag+)、c(I-)大于等于1mol·L-1时,Ag+可以氧化I-),借助原电池原理优化实验设计,证实了自己的观点。
②请你补充画完整原电池装置示意图(如图),并作相应标注_______ 。

③根据以上实验过程,试分析实验2中Ag+ 没能氧化I- 的可能原因是_______ 。

(1)步骤①中用到的硅酸盐材质的仪器为
(2)步骤③用酸化的H2O2氧化I- 的离子方程式为
(3)实验小组根据元素周期律研究氧化I- 的氧化剂 (见下图),A、B两种盐溶液分别为

(4)实验小组还设计了下表实验,对金属阳离子氧化I- 进行研究。
已知:常温下,CuI(白色)、AgI(黄色)的Ksp分别为
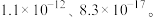
| 序号 | 实验步骤 | 实验现象 | 结论 |
| 1 | 往CuSO4溶液中滴加KI溶液,然后加入少量苯,振荡 | 产生白色沉淀,溶液分层,上层为紫红色 | Cu2+可以氧化I- 为I2 |
| 2 | 往AgNO3中滴加KI溶液,滴加几滴a溶液,振荡 | 产生黄色沉淀,溶液无色 | Ag+与I-只发生沉淀反应 |
甲同学根据现象得出结论:Ag+氧化性比Cu2+弱且不能氧化I-。
乙同学对甲同学的结论提出质疑,查阅资料(常温下,反应2Ag+(aq)+2I-(aq)⇌2Ag(s)+I2(aq)的平衡常数
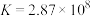 ,当c(Ag+)、c(I-)大于等于1mol·L-1时,Ag+可以氧化I-),借助原电池原理优化实验设计,证实了自己的观点。
,当c(Ag+)、c(I-)大于等于1mol·L-1时,Ag+可以氧化I-),借助原电池原理优化实验设计,证实了自己的观点。②请你补充画完整原电池装置示意图(如图),并作相应标注

③根据以上实验过程,试分析实验2中Ag+ 没能氧化I- 的可能原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海水资源的利用具有非常广阔的前景。下面是海水综合利用联合工业体系的简图:

回答下列问题:
I.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法主要有_______ 、_______ 等。
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是_______ ;
(3)粗盐中可溶性的杂质离子主要有SO 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是_______ 。
Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为_______ ;从理论上考虑下列也能吸收Br2的是_______ 。
A.NaCl B.FeCl2 C. Na2SO3 D. H2O
(5)经过步骤①②已获得Br2,不直接用含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、通入氯气”后再蒸馏,其目的是_______ ;
(6)溴在元素周期表中的位置是_______ 。
Ⅳ.海水提镁
(7)该工业生产过程中,为了使MgCl2转化为Mg(OH)2,应加入的试剂为_______ ;
(8)写出电解MgCl2冶炼金属Mg的化学方程式_______ 。

回答下列问题:
I.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法主要有
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是
(3)粗盐中可溶性的杂质离子主要有SO
 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为
A.NaCl B.FeCl2 C. Na2SO3 D. H2O
(5)经过步骤①②已获得Br2,不直接用含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、通入氯气”后再蒸馏,其目的是
(6)溴在元素周期表中的位置是
Ⅳ.海水提镁
(7)该工业生产过程中,为了使MgCl2转化为Mg(OH)2,应加入的试剂为
(8)写出电解MgCl2冶炼金属Mg的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】高砷煤中含有砷硫铁(FeAsS)等物质。燃煤产生的烟气中含NO、SO2、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
(1)燃煤固硫
①燃用高砷煤时加入生石灰将大部分硫元素转化为___________ (填化学式)留在煤渣中。
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成As2O3释放到烟气中,该反应的化学方程式为___________ 。
(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将NH3、NO、O2转化为N2.烟气中含有的As2O3会使钒氧化物催化剂中毒。
①在SCR脱硝的反应中还原剂为___________ (填化学式)。
②研究发现砷中毒机理主要是As2O3分子破坏了催化剂的Lewis酸位点,使V=O数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构。___________ 。
(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量(NH3或铵盐)会影响水泥的性能。
取50.00 g粉煤灰加入NaOH蒸出NH3,用20 mL 0.100 0 mol·L-1的H2SO4溶液吸收NH3,用0.200 0 mol·L-1 NaOH溶液滴定过量的H2SO4至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以NH3计的氨含量(用mg·g-1表示,写出计算过程)。___________
(1)燃煤固硫
①燃用高砷煤时加入生石灰将大部分硫元素转化为
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成As2O3释放到烟气中,该反应的化学方程式为
(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将NH3、NO、O2转化为N2.烟气中含有的As2O3会使钒氧化物催化剂中毒。
①在SCR脱硝的反应中还原剂为
②研究发现砷中毒机理主要是As2O3分子破坏了催化剂的Lewis酸位点,使V=O数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构。
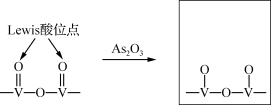
(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量(NH3或铵盐)会影响水泥的性能。
取50.00 g粉煤灰加入NaOH蒸出NH3,用20 mL 0.100 0 mol·L-1的H2SO4溶液吸收NH3,用0.200 0 mol·L-1 NaOH溶液滴定过量的H2SO4至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以NH3计的氨含量(用mg·g-1表示,写出计算过程)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】纯橄岩为含镁的硅酸盐矿物,并含有MnO、Fe2O3、FeO、SiO2和一些有机物等杂质。工业上利用纯橄岩制备一水硫酸镁(MgSO4·H2O)的工艺流程如下:
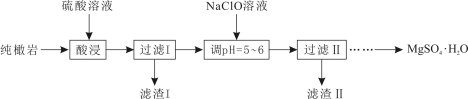
(1)酸浸时温度控制在90℃~100℃之间,并且要连续搅拌2小时。
①连续搅拌2小时的目的是_________________ 。
②酸浸时适宜的酸度及用量对酸浸工艺十分重要,浓度过低,浸取不完全,浓度过高(>5mol/L)造成浆料黏度过大,出现“包团现象”,根据酸浸反应原理分析,造成浆料黏度过大的物质是________ (填名称)。
(2)实验室中过滤所需玻璃仪器有烧杯、玻璃棒和_______ 。
(3)向过滤Ⅰ的滤液中加入NaClO溶液,将溶液中的Mn2+氧化成MnO2,反应的离子方程式为_______ 。
(4)滤渣Ⅱ中主要成分为MnO2和______ (填化学式)。
(5)已知硫酸镁的溶解度随温度变化的曲线如下图,且溶液的沸点随压强增大而升高。为了从滤液中充分回收MgSO4·H2O,采取将滤液蒸发浓缩、加压升温的方法结晶,需要加压升温的原因是_______ 。


(1)酸浸时温度控制在90℃~100℃之间,并且要连续搅拌2小时。
①连续搅拌2小时的目的是
②酸浸时适宜的酸度及用量对酸浸工艺十分重要,浓度过低,浸取不完全,浓度过高(>5mol/L)造成浆料黏度过大,出现“包团现象”,根据酸浸反应原理分析,造成浆料黏度过大的物质是
(2)实验室中过滤所需玻璃仪器有烧杯、玻璃棒和
(3)向过滤Ⅰ的滤液中加入NaClO溶液,将溶液中的Mn2+氧化成MnO2,反应的离子方程式为
(4)滤渣Ⅱ中主要成分为MnO2和
(5)已知硫酸镁的溶解度随温度变化的曲线如下图,且溶液的沸点随压强增大而升高。为了从滤液中充分回收MgSO4·H2O,采取将滤液蒸发浓缩、加压升温的方法结晶,需要加压升温的原因是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】中国沿海某城市采用反渗透法将海水淡化,得到淡水供市民使用,剩余母液继续加工获得其他产品。某实验小组同学模拟工业生产流程,进行如下实验。
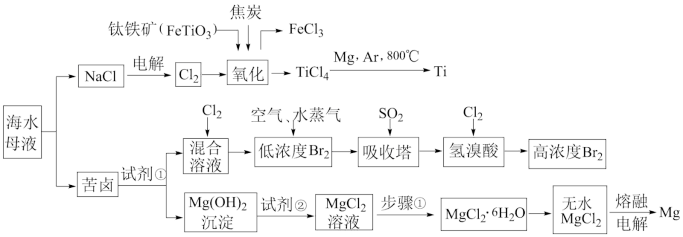
回答下列问题:
(1)海水淡化的方法还有_______ (写出一种)。
(2)吸收塔中反应的离子方程式是_______ 。
(3)步骤①包括加热蒸发浓缩、_______ 、过滤。
(4)若要验证所得无水MgCl2中不含NaCl,最简单的方法是_______ 。
(5)通电时无水MgCl2在熔融状态下反应的化学方程式是_______ 。
(6)写出钛铁矿在高温下经氧化得到四氯化钛的化学方程式_______ 。
(7)由TiCl4→Ti需要在Ar气中进行的理由是_______ 。反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于_______ ℃即可。

回答下列问题:
(1)海水淡化的方法还有
(2)吸收塔中反应的离子方程式是
(3)步骤①包括加热蒸发浓缩、
(4)若要验证所得无水MgCl2中不含NaCl,最简单的方法是
(5)通电时无水MgCl2在熔融状态下反应的化学方程式是
(6)写出钛铁矿在高温下经氧化得到四氯化钛的化学方程式
(7)由TiCl4→Ti需要在Ar气中进行的理由是
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】聚合硫酸铁、明矾可用作净水剂。某课题组拟以废弃的铝铁合金为原料制备聚合硫酸铁和明矾,设计化工流程如下:

(1)聚合硫酸铁能溶于水,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①在聚合硫酸铁中,x、y之间的关系是_______ 。试剂X中溶质的电子式为________ 。
②流程图中,氧化剂稀硝酸应换为双氧水,其原因是____________ ;为了降低聚合硫酸铁的溶解度,在浓缩过程中加入适量的溶剂是________ (填化学式)。
③若Y为氧化物,用离子方程式表示加入试剂Y的目的:________ ;溶液的pH对[Fe2(OH)x(SO4)y]n中x的值有较大影响(如图A所示),试分析pH过小(pH≤3.0)导致聚合硫酸铁中x的值减小的原因:________ 。


图 A 图B
(2)明矾的化学式为KAl(SO4)2·12H2O。图B为明矾的溶解度随温度变化的曲线,由滤液Ⅰ制备明矾晶体的流程如下(供选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):

①试剂1是____ ;操作1的名称是________ 。
②“溶解”恰好完全的标志是____ ;结晶措施是________ 。

(1)聚合硫酸铁能溶于水,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①在聚合硫酸铁中,x、y之间的关系是
②流程图中,氧化剂稀硝酸应换为双氧水,其原因是
③若Y为氧化物,用离子方程式表示加入试剂Y的目的:


图 A 图B
(2)明矾的化学式为KAl(SO4)2·12H2O。图B为明矾的溶解度随温度变化的曲线,由滤液Ⅰ制备明矾晶体的流程如下(供选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):

①试剂1是
②“溶解”恰好完全的标志是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】氯化亚铜(CuCI)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。工业上采用如下工艺流程,从某酸性废液(主要含Cu2+、Fe3+、H+、Cl-中制备氯化亚铜。

请回答下列问题:
(1)出步骤①中发生的两个主要反应的离子方程式:________________________ 。
(2)步骤②的操作名称是___________ 。
(3)步骤④中所加物质X为___________ 。
(4)步骤⑤的操作是___________ 。
(5)步骤⑥应调节溶液pH呈酸性,且用乙醇洗涤CuCl晶体,目的是___________ 。
(6)在CuCl的生成过程中,可以循环利用的物质是______ ,理论上______ (填“是”或“否”)需要补充(不考虑调节等消耗):理由是________________________ 。

请回答下列问题:
(1)出步骤①中发生的两个主要反应的离子方程式:
(2)步骤②的操作名称是
(3)步骤④中所加物质X为
(4)步骤⑤的操作是
(5)步骤⑥应调节溶液pH呈酸性,且用乙醇洗涤CuCl晶体,目的是
(6)在CuCl的生成过程中,可以循环利用的物质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程如下图所示
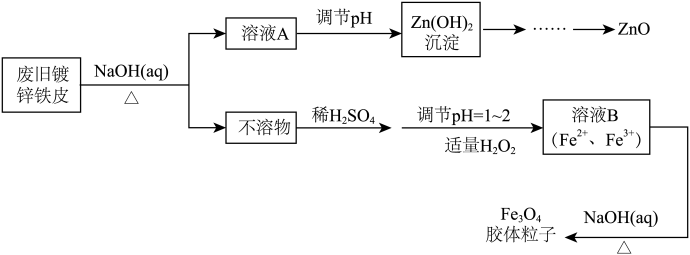
(1)从流程图可知,Zn、Fe中能与NaOH溶液反应的是_______________________ 。
(2)向不溶物中加入稀硫酸发生反应的离子方程式是____________________________________ 。
(3)加入适量H2O2的目的是__________________________________ 。
(4)如何证明已生成了Fe3O4胶体?_____________________________________________________ 。
(5)流程中所需的硫酸溶液由焦硫酸(H2SO4·SO3)溶于水配制而成,其中的SO3都转化为硫酸,若将445g焦硫酸溶于水配成4.00L硫酸,该硫酸的物质的量浓度为__________________ mol/L。
(6)稀硫酸也可以用浓硫酸和水配制。已知4 mol/L的硫酸溶液密度为ρ1g/cm3,2 mol/L的硫酸溶液密度为ρ2g/cm3。100g物质的量浓度为4 mol/L的硫酸溶液与___________ mL水混合,使硫酸的物质的量浓度减小到2 mol/L(用含ρ1、ρ2的式子表示)

(1)从流程图可知,Zn、Fe中能与NaOH溶液反应的是
(2)向不溶物中加入稀硫酸发生反应的离子方程式是
(3)加入适量H2O2的目的是
(4)如何证明已生成了Fe3O4胶体?
(5)流程中所需的硫酸溶液由焦硫酸(H2SO4·SO3)溶于水配制而成,其中的SO3都转化为硫酸,若将445g焦硫酸溶于水配成4.00L硫酸,该硫酸的物质的量浓度为
(6)稀硫酸也可以用浓硫酸和水配制。已知4 mol/L的硫酸溶液密度为ρ1g/cm3,2 mol/L的硫酸溶液密度为ρ2g/cm3。100g物质的量浓度为4 mol/L的硫酸溶液与
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】工业上用含有Fe、Cu、Al的合金废料进行一系列化工处理,制胆矾、绿矾(FeSO4·7H2O),并回收得到金属铝,流程如图。
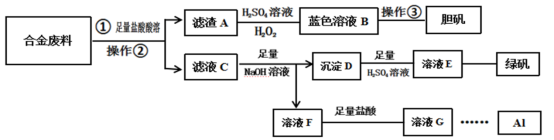
回答下列问题:
(1)操作②为_______ ,用到的玻璃仪器有_______
(2)操作③为_______
(3)能否通过电解溶液G制得金属Al,_______ (填“能”或“不能”)。
(4)沉淀D暴露在空气中容易被空气氧化而使最后制得的绿矾不纯,可以向溶液E中加入过量_______ ,过滤后取滤液再制得绿矾。沉淀D被空气氧化的现象为_______
(5)写出由滤渣A得到蓝色溶液B的化学反应方程式_______
(6)若将①改为加足量的NaOH溶液,发生反应的离子方程式为_______

回答下列问题:
(1)操作②为
(2)操作③为
(3)能否通过电解溶液G制得金属Al,
(4)沉淀D暴露在空气中容易被空气氧化而使最后制得的绿矾不纯,可以向溶液E中加入过量
(5)写出由滤渣A得到蓝色溶液B的化学反应方程式
(6)若将①改为加足量的NaOH溶液,发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
真题
名校
【推荐2】下图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。回答下列问题:
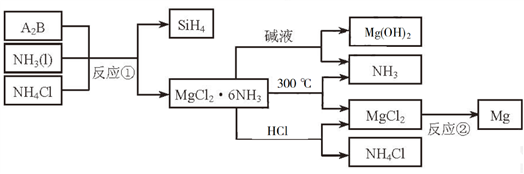
(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H-除外):_________________________ ,Mg在元素周期表中的位置:_____________________ ,Mg(OH)2的电子式:____________________ 。
(2)A2B的化学式为_______________ 。反应②的必备条件是_______________ 。上图中可以循环使用的物质有_______________ 。
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料_______________ (写化学式)。
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式:_______________ 。
(5)用Mg制成的格氏试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:

依据上述信息,写出制备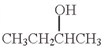 所需醛的可能结构简式:
所需醛的可能结构简式:_______________ 。

(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H-除外):
(2)A2B的化学式为
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式:
(5)用Mg制成的格氏试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:

依据上述信息,写出制备
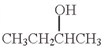 所需醛的可能结构简式:
所需醛的可能结构简式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】明矾[KAl(SO4)2·12H2O]在生产、生活中有广泛用途:饮用水的净化、食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、Al2O3及少量SiO2和FeO·xFe2O3)可制备明矾。工艺流程如下。回答下列问题:

(1)明矾净水的原理是____________________________ (用离子方程式表示)。
(2)操作Ⅰ是_____________ ,操作Ⅱ是蒸发浓缩、_____________ 、过滤、洗涤、干燥。
(3)检验滤液A中是否存在Fe2+的试剂是________________ (只用一种试剂)。
(4)将铝灰投入氢氧化钠溶液中生成气体的化学方程式是____________________________________ ,在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下MnO 转化为Mn2+)
转化为Mn2+)___________ 。
(5)已知:在pH=3、加热条件下, MnO 可与Mn2+反应生成MnO2,加入MnSO4发生反应的离子方程式为
可与Mn2+反应生成MnO2,加入MnSO4发生反应的离子方程式为___________________________________________ 。

(1)明矾净水的原理是
(2)操作Ⅰ是
(3)检验滤液A中是否存在Fe2+的试剂是
(4)将铝灰投入氢氧化钠溶液中生成气体的化学方程式是
 转化为Mn2+)
转化为Mn2+)(5)已知:在pH=3、加热条件下, MnO
 可与Mn2+反应生成MnO2,加入MnSO4发生反应的离子方程式为
可与Mn2+反应生成MnO2,加入MnSO4发生反应的离子方程式为
您最近一年使用:0次



